Đáp án: D
Giả sử số hiệu nguyên tử và số nơtron của R lần lượt là Z, N.
Ta có hpt: 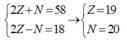
R có số hạt mang điện = 2Z = 38.
Cấu hình electron của R là 19R: 1s22s22p63s23p64s1.
R có 4 lớp electron, có 1 electron lớp ngoài cùng → R là kim loại.
Đáp án: D
Giả sử số hiệu nguyên tử và số nơtron của R lần lượt là Z, N.
Ta có hpt: 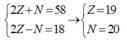
R có số hạt mang điện = 2Z = 38.
Cấu hình electron của R là 19R: 1s22s22p63s23p64s1.
R có 4 lớp electron, có 1 electron lớp ngoài cùng → R là kim loại.
Cho nguyên tử R có tổng số hạt là 115, hạt mang điện nhiều hơn hạt không mang điện là 25 hạt. Cấu hình electron nguyên tử của R là
A. [Ne] 3s23p3.
B. [Ne] 3s23p5.
C. [Ar] 4s24p5.
D. [Ar] 3d104s24p5.
Cho nguyên tử R có tổng số hạt là 115, hạt mang điện nhiều hơn hạt không mang điện là 25 hạt. Cấu hình electron nguyên tử R là
A. [Ne]3s23p3
B. [Ne]3s23p5
C. [Ne]4s24p5
D. [Ne]3d104s24p5
Một nguyên tử R có tổng số hạt là 58. Số hạt mang điện nhiều hơn số hạt không mang điện là 18. Tìm kết luận không đúng:
A. Số hạt mang điện trong R là 38
B. R là kim loại
C. Ion tương ứng của R có cấu trúc electron giống như cấu trúc e của Argon
D. Nguyên tử R có 3 lớp electron
Câu 2: Tổng hạt proton, nơtron và electron trong nguyên tử của nguyên tố R là 40.
a) Xác định số hiệu nguyên tử và số khối của R? Biết trong nguyên tử R số hạt mang điện nhiều hơn số hạt không mang điện là 12.
b) Viết cấu hình electron nguyên tử của nguyên tố đó. Biểu diễn sự phân bố các electron trên các obitan của R?
. Nguyên tử của một nguyên tố R có cấu tạo bởi 115 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 25 hạt. Tìm số hạt proton ,electron, nơtron của nguyên tử R . ( Đáp số : P=35=E, N=45 )
chỉ mình với các bạn
Một nguyên tử R có tổng số hạt mang điện và không mang điện là 34, trong đó số hạt mang điện gấp 1,833 lần số hạt không mang điện.
Nguyên tố R và cấu hình electron là
A. Na, 1s22s22p63s1.
B. Mg, 1s22s22p63s1.
C. Na, 1s22s22p63s2.
D. Mg, 1s22s22p63s2.
Một nguyên tử R có tổng số hạt mang điện và không mang điện là 34, trong đó số hạt mang điện gấp 1,833 lần số hạt không mang điện. Nguyên tố R và cấu hình electron là
A. Na, 1s22s22p63s1
B. Mg, 1s22s22p63s2
C. F, 1s22s22p5
D. Ne, 1s22s22p6
Một nguyên tử R có tổng số hạt mang điện và không mang điện là 34, trong đó số hạt mang điện gấp 1,833 lần số hạt không mang điện. Nguyên tố R và cấu hình electron là:
A. Na, 1s2 2s2 2p6 3s1 .
B. .Mg, 1s2 2s2 2p6 3s2 .
C. F, 1s2 2s2 2p5
D. Ne, 1s2 2s2 2p6
Câu 7: Nguyên tử của một nguyên tố R có tổng số các loại hạt proton, electron, nơtron bằng 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Tìm điện tích hạt nhân của R. Câu 8: Tổng số các hạt proton, electron, nơtron của một nguyên tử X là 28. Số hạt mang điện nhiều hơn số hạt không mang điện là 8. Tìm điện tích hạt nhân của X. Câu 9: Nguyên tử của một nguyên tố X có tổng số các loại hạt proton, electron, nơtron bằng 115. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 25 hạt. Viết kí hiệu nguyên tử của X. Câu 10: Khối lượng của nguyên tử nguyên tố X là 27u. Số hạt không mang điện nhiều hơn số hạt mang điện là dương là 1. Viết kí hiệu nguyên tử của X. Câu 11: Tính nguyên tử khối trung bình của nguyên tố Oxi, biết Oxi có 3 đồng vị : 99,757% 816O; 0,039% 817O; 0,204% 818O