Chọn: B
Hướng dẫn: Áp dụng công thức định luật Fara-đây là với I = 1 (A), A = 108, n = 1, t = 965 (s), F = 96500 (g/mol.C)
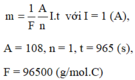
Chọn: B
Hướng dẫn: Áp dụng công thức định luật Fara-đây là với I = 1 (A), A = 108, n = 1, t = 965 (s), F = 96500 (g/mol.C)
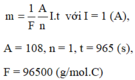
Một bình điện phân đựng dung dịch bạc nitrat ( A g N O 3 ) với anốt bằng bạc (Ag). Sau khi điện phân 30 phút có 5,04 gam bạc bám vào catốt. Xác định cường độ dòng điện đi qua bình điện phân. Cho biết đối với bạc A = 108 và n = 1
Điện phân dung dịch AgNO3với dương cực là Ag, biết khối lượng mol của Ag là 108. trong thời gian 1h có 27g Ag bám vào cực âmcủa bình điện phân( biết A = 108 , n=1)
a. Nêu cơ chế điện phân
b. Tínhcường độdòng điện chạy qua bình điện phân.
c. Bình điện phân có điện trở Rp= 2Ω, tính hiệu điện thế giữa 2 cực của bình điện phân.
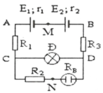
V ; r 1 = r 2 = 0 , 4 Ω ; Đèn Đ loại 6V-3W; R 1 = 0 , 2 Ω ; R 2 = 3 Ω ; R 3 = 4 Ω ; R B = 1 Ω và là bình điện phân đựng dung dịch A g N O 3 , có cực dương bằng Ag. Tính:
a) Cường độ dòng điện chạy trong mạch chính
b) Lượng Ag giải phóng ở cực âm của bình điện phân trong thời gian 2 giờ 8 phút 40 giây. Biết Ag có n=1 và có A=108.
c) Hiệu điện thế giữa hai điểm M và N
Một bình điện phân chứa dung dịch bạc nitrat ( AgNO 3 ) có anôt bằng bạc và điện trở là 2,5 Ω . Hiệu điện thế giữa hai điện cực của bình này là 10 V. Bạc (Ag) có khối lượng mol là A = 108 g/mol và hoá trị n = 1. Xác định khối lượng bạc bám vào catôt sau 16 phút 5 giây.
A. 4,32 g. B. 4,32 kg.
C.2,16g. D. 2,16 kg.
Một bình điện phân chứa dung dịch A g N O 3 có điện trở 2,5W. Anốt của bình bằng Ag và hiệu điện thế đặt vào hai điện cực của bình là 10V. Sau 16 phút 5 giây, khối lượng m của Ag bám vào catôt bằng bao nhiêu? Bạc có khối lượng mol nguyên tử là A = 108 g/mol, hóa trị n = 1
A. 2,16 g
B. 4,32 mg
C. 4,32 g
D. 2,16 mg
Một bình điện phân chứa dung dịch muối niken với hai điện cực bằng niken. Xác định khối lượng niken bám vào catôt khi cho dòng điện cường độ I = 5,0 A chạy qua bình này trong khoảng thời gian t = 1 giờ. Đương lượng điện hoá của niken là 0,3. 10 - 3 g/C.
A. 1,5 kg. B. 5,4 g.
C. 1,5 g. D. 5,4 kg.
Một bình điện phân chứa dung dịch A g N O 3 có điện trở 2 , 5 Ω . Anốt của bình bằng Ag và hiệu điện thế đặt vào hai điện cực của bình là 10 V. Sau 16 phút 5 giây, khối lượng m của Ag bám vào catôt bằng bao nhiêu? Bạc có khối lượng mol nguyên tử là A = 108 g/mol, hóa trị n = 1.
A. 2,16 g
B. 4,32 mg
C. 4,32 g
D. 2,16 mg
Cho mạch điện như hình vẽ.
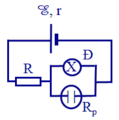
Trong đó E = 8 V , r = 1 Ω , R = 0 , 6 Ω , Đ là bóng đèn loại 6V – 6W, R p = 4 Ω và là bình điện phân đựng dung dịch CuSO4 có cực dương bằng đồng. Biết đồng có khối lượng mol nguyên tử là A = 64 g/mol, có hoá trị n = 2.
a) Tính cường độ dòng điện chạy qua từng linh kiện trong mạch.
b) Tính khối lượng đồng bám vào catốt sau 32 phút 10 giây và điện năng tiêu thụ trên bình điện phân trong thời gian đó.
Khi điện phân dung dịch A g N O 3 với cực dương là Ag biết khối lượng mol của bạc là 108. Cường độ dòng điện chạy qua bình điện phân để trong 1 h để có 27 gam Ag bám ở cực âm là
A. 6,7 A
B. 3,35 A
C. 24124 A
D. 108 A