Đáp án A. Áp công thức của 2 định luật Faraday suy ra I = m n F A t = 27 . 1 . 96500 108 . 3600 = 6 , 7 A
Đúng 0
Bình luận (0)
Các câu hỏi tương tự
Khi điện phân dung dịch A g N O 3 với cực dương là Ag biết khối lượng mol của bạc là 108. Cường độ dòng điện chạy qua bình điện phân để trong 1 h để có 27 gam Ag bám ở cực âm là
A. 6,7 A
B. 3,35 A
C. 24124 A
D. 108 A
Khi điện phân dung dịch A g N O 3 với cực dương là Ag biết khối lượng mol của bạc là 108. Cường độ dòng điện chạy qua bình điện phân để trong 1h để có 27 gam Ag bám ở cực âm là
A. 6,7A
B. 3,35A
C. 2412A
D. 108A
Khi điện phân dung dịch A g N O 3 với cực dương là Ag biết khối lượng mol của bạc là 108. Cường độ dòng điện chạy qua bình điện phân để trong 2 h để có 54 gam Ag bám ở cực âm là
A. 6,7 A
B. 3,35 A
C. 24124 A
D. 108 A
Điện phân dung dịch AgNO3với dương cực là Ag, biết khối lượng mol của Ag là 108. trong thời gian 1h có 27g Ag bám vào cực âmcủa bình điện phân( biết A 108 , n1)a. Nêu cơ chế điện phânb. Tínhcường độdòng điện chạy qua bình điện phân.c. Bình điện phân có điện trở Rp 2Ω, tính hiệu điện thế giữa 2 cực của bình điện phân.
Đọc tiếp
Điện phân dung dịch AgNO3với dương cực là Ag, biết khối lượng mol của Ag là 108. trong thời gian 1h có 27g Ag bám vào cực âmcủa bình điện phân( biết A = 108 , n=1)
a. Nêu cơ chế điện phân
b. Tínhcường độdòng điện chạy qua bình điện phân.
c. Bình điện phân có điện trở Rp= 2Ω, tính hiệu điện thế giữa 2 cực của bình điện phân.
Một bình điện phân chứa dung dịch bạc nitrat có anôt bằng bạc, cường độ dòng điện chạy qua bình điện phân là 5A. Lượng bạc bám vào cực âm của bình điện phân trong 2 giờ là bao nhiêu, biết bạc có A 108, n l: A. 40,29g B.
40
,
29
.
10
-
3
g
C. 42,9g D.
42
,
9
.
10
-
3...
Đọc tiếp
Một bình điện phân chứa dung dịch bạc nitrat có anôt bằng bạc, cường độ dòng điện chạy qua bình điện phân là 5A. Lượng bạc bám vào cực âm của bình điện phân trong 2 giờ là bao nhiêu, biết bạc có A = 108, n = l:
A. 40,29g
B. 40 , 29 . 10 - 3 g
C. 42,9g
D. 42 , 9 . 10 - 3 g
Điện phân dung dịch CuSO4 với cực dương là Cu. Biết khối lượng mol của Cu là 64. Cường độ dòng điện chạy qua bình điện phân là 4 A. Lấy F = 96500 (C/mol). Để khối lượng Cu bám ở catot là 1,28g thì cần cho dòng điện chạy qua bình điện phân trong bao lâu.
V
;
r
1
r
2
0
,
4
Ω
; Đèn Đ loại 6V-3W;
R
1
0
,
2
Ω
;
R
2
3
Ω
;
R
3
4
Ω
;
R
B...
Đọc tiếp
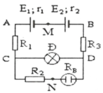
V ; r 1 = r 2 = 0 , 4 Ω ; Đèn Đ loại 6V-3W; R 1 = 0 , 2 Ω ; R 2 = 3 Ω ; R 3 = 4 Ω ; R B = 1 Ω và là bình điện phân đựng dung dịch A g N O 3 , có cực dương bằng Ag. Tính:
a) Cường độ dòng điện chạy trong mạch chính
b) Lượng Ag giải phóng ở cực âm của bình điện phân trong thời gian 2 giờ 8 phút 40 giây. Biết Ag có n=1 và có A=108.
c) Hiệu điện thế giữa hai điểm M và N
Một bình điện phân chứa dung dịch bạc nitrat (
AgNO
3
) có anôt bằng bạc và điện trở là 2,5
Ω
. Hiệu điện thế giữa hai điện cực của bình này là 10 V. Bạc (Ag) có khối lượng mol là A 108 g/mol và hoá trị n 1. Xác định khối lượng bạc bám vào catôt sau 16 phút 5 giây.A. 4,32 g. B. 4,32 kg.C.2,16g. D. 2,16 kg.
Đọc tiếp
Một bình điện phân chứa dung dịch bạc nitrat ( AgNO 3 ) có anôt bằng bạc và điện trở là 2,5 Ω . Hiệu điện thế giữa hai điện cực của bình này là 10 V. Bạc (Ag) có khối lượng mol là A = 108 g/mol và hoá trị n = 1. Xác định khối lượng bạc bám vào catôt sau 16 phút 5 giây.
A. 4,32 g. B. 4,32 kg.
C.2,16g. D. 2,16 kg.
Một bình điện phân chứa dung dịch
A
g
N
O
3
có điện trở 2,5W. Anốt của bình bằng Ag và hiệu điện thế đặt vào hai điện cực của bình là 10V. Sau 16 phút 5 giây, khối lượng m của Ag bám vào catôt bằng bao nhiêu? Bạc có khối lượng mol nguyên tử là A 108 g/mol, hóa trị n 1 A. 2,16 g B. 4,32 mg C. 4,32 g D. 2,16 mg
Đọc tiếp
Một bình điện phân chứa dung dịch A g N O 3 có điện trở 2,5W. Anốt của bình bằng Ag và hiệu điện thế đặt vào hai điện cực của bình là 10V. Sau 16 phút 5 giây, khối lượng m của Ag bám vào catôt bằng bao nhiêu? Bạc có khối lượng mol nguyên tử là A = 108 g/mol, hóa trị n = 1
A. 2,16 g
B. 4,32 mg
C. 4,32 g
D. 2,16 mg





