MnO2 + 4HCL ==to=> MnCl2 + Cl2 + 2H2O
H2 + CL2 ==to==> 2HCl\(\uparrow\)
HCL\(\uparrow\) + H2O ===> HCL loãng
8HCL + Fe3O4 ====> FeCl2 + 2FeCl3 + 4H2O
MnO2 + 4HCL ==to=> MnCl2 + Cl2 + 2H2O
H2 + CL2 ==to==> 2HCl\(\uparrow\)
HCL\(\uparrow\) + H2O ===> HCL loãng
8HCL + Fe3O4 ====> FeCl2 + 2FeCl3 + 4H2O
Viết các phương trình phản ứng xảy ra cho các sơ đồ sau:
1. HCl -> Cl2 -> FeCl3 -> NaCl -> HCl -> CuCl2 -> AgCl
2. KMnO4 ->Cl2->HCl ->FeCl3 -> AgCl -> Cl2->Br2->I2
3. KMnO4 → Cl2 → HCl →FeCl2 → AgCl → Ag
4. HCl → Cl2→ FeCl3 → Fe(OH)3 → Fe2(SO4)3
Cho sơ đồ phản ứng sau: X + H 2 S O 4 d , n → C u S O 4 + S O 2 + H 2 O
Hoàn thành sơ đồ phản ứng và cho biết tổng hệ số các chất phản ứng là bao nhiêu?
A. 1
B. 4
C. 2
D. 3
Cho các phản ứng sau:
1 . M n O 2 + ( A ) → M n C l 2 + ( B ) + ( C )
2 . ( B ) + H 2 → H C l
3 . ( A ) + ( D ) → F e C l 2 + H 2
4 . ( B ) + ( D ) → F e C l 3
5 . ( B ) + ( C ) → ( A ) + ( E )
Các chất A, B, C và E lần lượt là
A. C l 2 , H C l , H 2 , H C l O .
B. H C l , C l 2 , H 2 O , H C l O .
C. H C l , O 2 , H 2 , H C l O .
D. C l 2 , H 2 , H 2 O , H C l O .
Hoàn thành chuỗi phản ứng hoá học sau: ( ghi điều kiện phản ứng nếu có ) A. Ca --> CaC2 --> C2H2 --> C2H2Br4. B. MnO2 --> Cl2 --> FeCl --> Cl2
Điền công thức hoá học thích hợp vào chỗ trống trong các sơ đồ phản ứng sau và hoàn thành các phương trình hoá học : a) Al+O2—>....... b) .........+CuSO4 —>MgSO4+Cu c) ......+HCl —>CuCl2 + H2O d).........—>Fe2O3 +H2O. e) Fe(NO3)3 +.......—>Fe(OH3)+ ........
Câu 1: hoàn thành sơ đồ phản ứng sau và ghi rõ điều kiện phản ứng (nếu có) Fe(OH)3 -> Fe2O3 -> Để -> FeCl2 -> Fe (OH)2 Câu 2: cho 32,5 gam kẽm tác dụng vừa đủ với 400ml dung dịch HCl a, viết phương trình phản ứng xảy ra b, Tính thể tích khí sinh ra ở điều kiện tiêu chuẩn c, Số gam muối tạo thành d, Nồng độ mol của dung dịch HCl ban đầu
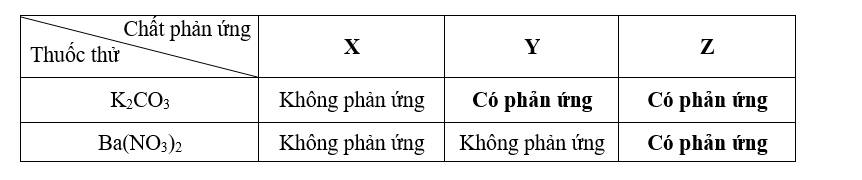 a. Xác định công thức hóa học của chất X, Y và Z.b. Nêu hiện tượng và viết phương trình hóa học của thí nghiệm có phản ứng xảy ra.Câu 4: (2,0 điểm) 4.1) Hòa tan hoàn toàn 6,5 gam kẽm bằng dung dịch H2SO4 loãng 19,6% vừa đủ.a. Viết phương trình hóa học.b. Tính thể tích khí hidro sinh ra (đktc).c. Cần bao nhiêu gam dung dịch H2SO4 loãng nói trên để hoà tan với kẽm. 4.2) Hòa tan 0,95 gam muối clorua của kim loại hóa trị II vào dung dịch AgNO3 dư thu được 2,87 gam chất kết tủa. Xác định công thức phân tử muối clorua.Câu 5: (2,0 điểm) Hòa tan hoàn toàn 14,2 gam gồm hỗn hợp bột CuO và Al2O3 cần 200ml dung dịch HCl 3,5M.a. Viết các phương trình hóa học. b. Tính thành phần phần trăm về khối lượng mỗi oxit trong hỗn hợp ban đầu ? Cho Zn = 65 ; Cl = 35,5 ; O = 16 ; H = 1; Al = 27 ; S = 32; Cu = 64 ; Mg = 24 ; Ag = 108 ; N = 14
a. Xác định công thức hóa học của chất X, Y và Z.b. Nêu hiện tượng và viết phương trình hóa học của thí nghiệm có phản ứng xảy ra.Câu 4: (2,0 điểm) 4.1) Hòa tan hoàn toàn 6,5 gam kẽm bằng dung dịch H2SO4 loãng 19,6% vừa đủ.a. Viết phương trình hóa học.b. Tính thể tích khí hidro sinh ra (đktc).c. Cần bao nhiêu gam dung dịch H2SO4 loãng nói trên để hoà tan với kẽm. 4.2) Hòa tan 0,95 gam muối clorua của kim loại hóa trị II vào dung dịch AgNO3 dư thu được 2,87 gam chất kết tủa. Xác định công thức phân tử muối clorua.Câu 5: (2,0 điểm) Hòa tan hoàn toàn 14,2 gam gồm hỗn hợp bột CuO và Al2O3 cần 200ml dung dịch HCl 3,5M.a. Viết các phương trình hóa học. b. Tính thành phần phần trăm về khối lượng mỗi oxit trong hỗn hợp ban đầu ? Cho Zn = 65 ; Cl = 35,5 ; O = 16 ; H = 1; Al = 27 ; S = 32; Cu = 64 ; Mg = 24 ; Ag = 108 ; N = 14Viết các PTHH hoàn thành sơ đồ biến đổi sau : Fe--->FeCl2--->Fe(OH)2--->FeSO4--->Fe--->FeCl3
Để loại khí HCl thoát ra cùng với khí C l 2 trong phản ứng M n O 2 + 4 H C l → t o M n C l 2 + C l 2 + 2 H 2 O người ta dùng
A. dung dịch NaOH
B. dung dịch NaCl bão hòa
C. H 2 S O 4 đặc
D. dung dịch nước vôi trong