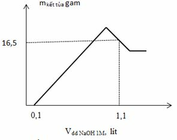
Hòa tan hoàn toàn m (gam) hỗn hợp gồm Al và Mg trong V (ml) dung dịch HNO3 2M. Kết thúc phản ứng, thu được dung dịch E (không chứa muối amoni) và 0,1 mol hỗn hợp khí gồm N2 và N2O có tỉ khối so với oxi là 1,125. Cho từ từ dung dịch NaOH 1M vào dung dịch E thì lượng kết tủa biến thiên theo đồ thị bên. Xác định các giá trị của m và V.
Tóm tắt:
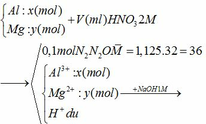
Gọi số mol của N2 và N2O lần lượt là
a và b (mol)
Ta có:
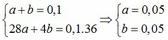


ne (KL nhường) = ne(N+5 nhận)
=> 2x + 3y = 0,5 + 0,4 (1)
Từ đồ thị ta thấy tại giá trị V= 0,1 (lít) tức nNaOH = 0,1 (mol) mới bắt đầu xuất hiện kết tủa=> lượng NaOH này chính là lượng để trung hòa HNO3 dư sau phản ứng=> nHNO3 dư = nNaOH0,1 (mol) Ta thấy tại giá trị V= 1,1 (lít) tức nNaOH = 1,1 (lít) đồ thị đi lên cực đại sau đó lại đi xuống => kết tủa đạt cực đại sau đó bị hòa tan 1 phần ( chỉ có Al(OH)3 bị hoàn tan) Khi cho NaOH từ từ vào dung dich .Z xảy ra phản ứng:
H+ + OH- → H2O
0,1 → 0,1 (mol)
Mg2+ + 2OH- → Mg(OH)2↓
x → 2x (mol)
Al3+ + 3OH- → Al(OH)3↓
y → 3y →y (mol)
Al(OH)3↓ + OH- → AlO2- + 2H2O
(y – z ) → (y –z) (mol)
Gọi số mol của Al(OH)3 còn lại không bị hoàn tan là z (mol)
=> ta có: ∑ nNaOH = nH+dư + 2nMg2+ + 4nAl3+ - nAl(OH)3
=> 0,1 +2x + 4y – z = 1,1 (2)
Mặt khác: ∑ mkết tủa = mMg(OH)2 + mAl(OH)3 chưa hòa tan
=> 58x + 78z = 16,5 (3)
Từ (1), (2) và (3) => x = 0,2 ; y = 0,15 và z = 0,1 (mol)
=> m = mAl + mMg = 0,2.27 + 0,15.24 = 9 (g)
nHNO3 = nHNO3 dư + 2nN2 + 2nN2O + 3nAl(NO3)3 + 2nMg(NO3)2 = 0,1 + 2.0,05 + 2. 0,05 + 3.0,2 + 2.0,15 = 1,2 (mol)
=> VHNO3 = n : CM = 1,2 : 2 = 0,6 (lít) = 600 (ml)





