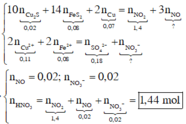Đáp án B
Theo giả thiết và áp dụng bảo toàn electron cho phản ứng của X với HNO3, ta có :
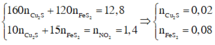
Dung dịch Y gồm Fe3+, Cu2+, SO 4 2 - , NO 3 - , H+. Khi cho Cu (tối đa) vào Y, Cu bị oxi hóa bởi (H+, NO 3 - ) và Fe3+. Vậy bản chất của bài toán là: Hỗn hợp Cu2S, FeS2 và Cu tác dụng với dung dịch HNO3, giải phóng hỗn hợp khí NO, NO2 và tạo ra dung dịch Z. Dung dịch Z có các ion Fe2+, Cu2+, SO 4 2 - , ion còn lại là H+ hoặc NO 3 - . Vì
![]()
nên ion còn lại trong dung dịch Z là ion âm để cân bằng điện tích, đó là ion NO 3 - .
Áp dụng bảo toàn electron và bảo toàn điện tích trong dung dịch Z và bảo toàn nguyên tố N, ta có :