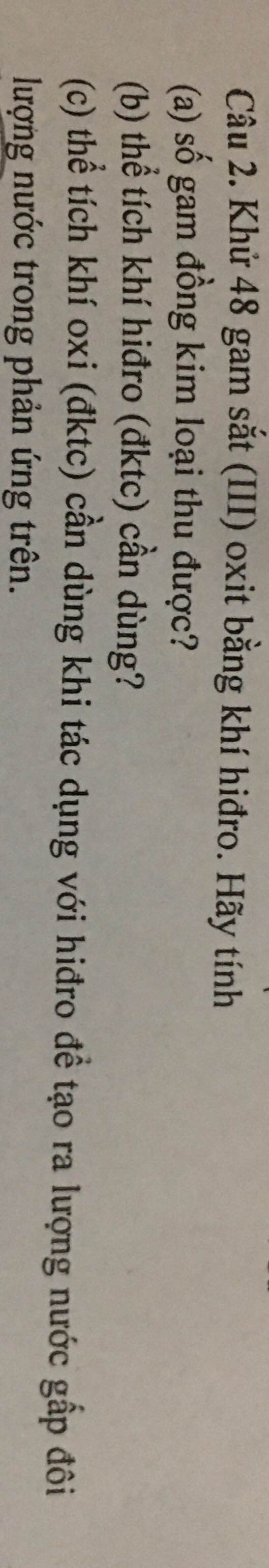Câu 4:nFe=0,15mol
a,3Fe+2O2->Fe3O4
0,15 0,05mol
b,a=0,05.232=11,6g
C, Fe3O4+8HCl->2FeCl3+FeCl2+4H2O
n(HCl)=8n(Fe3O4)=8.0,05=0,4mol
V(HCl)=0,4/1,2=0,3333lit=333,3ml
Câu 3:
n(Ba(OH)2)=0,15mol
n(H2SO4)=0,2mol
Ba(OH)2+H2SO4->BaSO4+2H2O
ta có 0,15/1 <0,2/1
=>H2SO4 dư
m(BaSO4)=0,15.233=34,95g
C, dd còn lại bao gồm
H2SO4: 0,05mol
C(H2SO4)=0,05/0,5=0,1M
A,
Fe+H2SO4->FeSO4+H2
Zn+H2SO4->ZnSO4+H2
B, m(H2SO4)=19,6g
n(h2so4)=0,2mol
a=nFe
b=nZn
=>56a+65b=12,1 (1)
a+b=0,2 (2)
(1);(2)=> a=0,1=b
%mFe=0,1.56.100%/12,1=46,28%
%mZn=53,72%
C, mdd=12,1+200-0,2.2=211,7g
C%(FeSO4)=0,1.152.100%/211,7=7,18%
C%(ZnSO4)=7,605%
Gọi n là hóa trị của kim loại M
2M+2nHCl->2MCln +nH2
a a
Ta có a=6,75/M
6,75/M .(M+35,5n)=33,375
=>M=9n
Chọn n=3=> M=27(Al)
B, nH2=1,5nAl=1,5.6,75/27=0,375mol
V=8,4lit








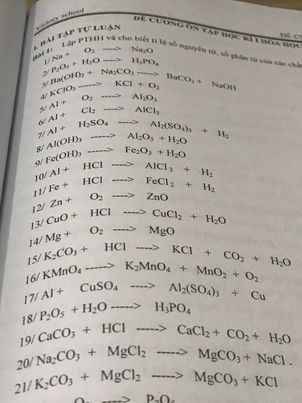



 Giúp mình giải các câu hỏi trên trừ 2 câu khoanh tròn vì mình đã làm r giúp mik với :3 cảm ơn nhiều ( lưu ý : giải chi tiết vì mình đang bắt đầu học )
Giúp mình giải các câu hỏi trên trừ 2 câu khoanh tròn vì mình đã làm r giúp mik với :3 cảm ơn nhiều ( lưu ý : giải chi tiết vì mình đang bắt đầu học )


 giúp mình với mình chỉ cần 2 câu 8 với câu 9 thôi nha
giúp mình với mình chỉ cần 2 câu 8 với câu 9 thôi nha