Đốt cháy hoàn toàn m gam hỗn hợp (H) gồm ba este đơn chức X, Y, Z (trong đó X và Y mạch hở, MX < MY ; Z chứa vòng benzen) cần vừa đủ 2,22 mol O2, thu được 20,16 gam H2O. Mặt khác m gam (H) tác dụng vừa đủ với 200 gam dung dịch NaOH 9,2%, cô cạn dung dịch sau phản ứng thu được m + 5,68 gam muối khan (gồm 3 muối trong đó có hai muối cùng số C) và hỗn hợp T chứa hai ancol có số nguyên tử cacbon liên tiếp nhau. Tỉ khối của T so với He bằng 9,4. Phần trăm khối lượng của Y có giá trị gần nhất với
A. 29%.
B. 30%.
C. 31%.
D. 32%.
Đáp án B
● Giả sử không có este của phenol
⇒ nH = nNaOH = nhh Ancol = 0,46 mol.
+ Bảo toàn khối lượng
⇒ nhh Ancol = mH + mNaOH – mMuối = 12,72 gam.
⇒ MTrung bình ancol = ![]() = 27,65
= 27,65
⇒ Vô lý vì ancol bé nhất là CH3OH (32).
⇒ Có este của phenol.
+ Giải hỗn hợp T ta có:
Từ tỉ khối hơi ⇒ 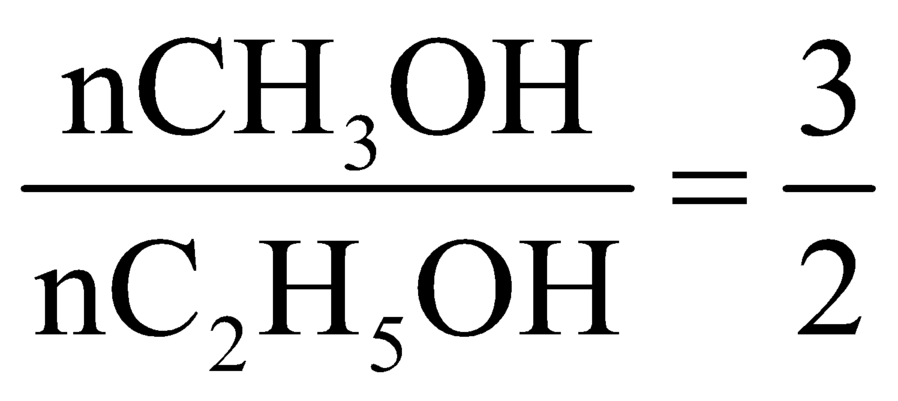
⇒ Đặt nCH3OH = 3a và nC2H5OH) = 2a.
+ Vì có muối của phenol
⇒ Có tạo ra H2O ⇒ Đặt nH2O = b.
⇒ 32×3a + 46×2a + 18b = 12,72
⇔ 156a + 18b = 12,72 (1).
⇒ 3a + 2a + 2b = nNaOH
⇔ 5a + 2b = 0,46 mol (2).
+ Giải hệ (1) và (2) ⇒ a = 0,06 và b = 0,08 mol
⇒ nhh este = 0,46 – 0,08 = 0,36 mol.
+ Bảo toàn oxi
⇒ nO/CO2 = 0,38×2 + 2,22×2 – 1,12 = 4,08
⇒ nCO2 = 2,04 mol
● Giải theo kinh nghiệm: X và Y sẽ cho cùng 1 muối và riêng Z sẽ tạo 2 muối.
+ Gọi số cacbon trong X, Y và Z lần lượt là a b và c
⇒ PT theo số mol CO2:
0,18a + 0,12b + 0,08c = 2,04.
⇒ Giải PT nghiệm nguyên ta có: a = 4, b = 5 và c = 9.
+ Gọi số nguyên tử hiđro trong X Y và Z lần lượt là a b và c
⇒ PT theo số mol H: 0,18a + 0,12b + 0,08c = 2,24.
⇒ Giải Pt nghiệm nguyên ta có: a = 4, b = 6 và c = 10.
● Vậy hỗn hợp H chứa
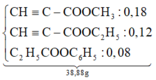
⇒ %mY = 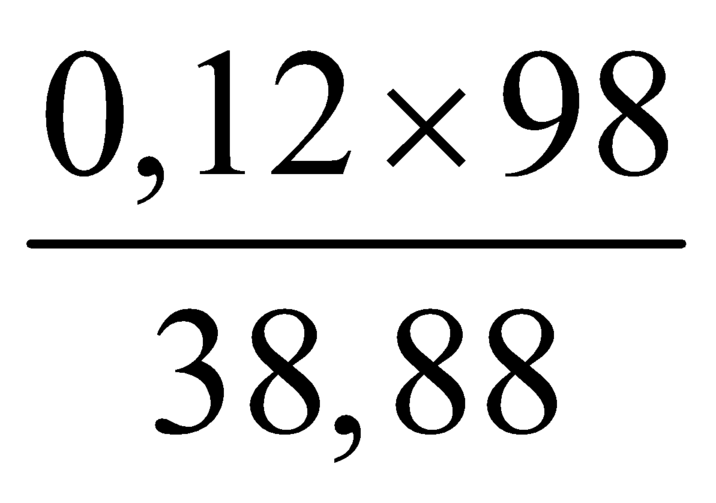 ≈ 30,35%
≈ 30,35%



