Chọn đáp án C
Trong các halogen, chỉ Flo có số oxi hóa -1 trong mọi hợp chất.
Clo, brom, iot ngoài số oxi hóa – 1, còn có số oxi hóa +1, +3, +5, +7 trong hợp chất.
Chọn đáp án C
Trong các halogen, chỉ Flo có số oxi hóa -1 trong mọi hợp chất.
Clo, brom, iot ngoài số oxi hóa – 1, còn có số oxi hóa +1, +3, +5, +7 trong hợp chất.
Đặc điểm nào dưới đây không phải là đặc điểm chung của các nguyên tố halogen (F, Cl, Br, I)?
A. Nguyên tử chỉ có khả năng thu thêm 1e.
B. Tạo ra với hidro hợp chất có liên kết cộng hóa trị có cực.
C. Có số oxi hóa – 1 trong mọi hợp chất.
D. Lớp electron ngoài cùng của nguyên tử có 7 electron.
Tính chất nào sau đây không phải là tính chất chung của các nguyên tử halogen
A. Nguyên tử có khả năng thu thêm 1 electron
B. Tác dụng với hidro tạo thành hợp chất có liên kết cộng hóa trị có cực
C. Có số oxi hóa -1 trong mọi hợp chất
D. Lớp electron ngoài đều có 7 electron
Nguyên tử nguyên tố X có electron cuối cùng thuộc phân lớp s, nguyên tử nguyên tố Y có electron cuối cùng thuộc phân lớp p. Biết rằng tổng số electron trong nguyên tử của X và Y là 20. Bản chất của liên kết hóa học trong hợp chất X – Y là:
A. Sự góp chung đôi electron.
B. Sự góp đôi electron từ một nguyên tử.
C. Sự tương tác yếu giữa hai nguyên tử có chênh lệch độ âm điện lớn.
D. Lực hút tĩnh điện giữa hai ion trái dấu
Nguyên tố X và Y thuộc nhóm A;nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p.Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là:
A. XY; liên kết ion.
B. Y2X; liên kết ion.
C. X5Y; liên kết cộng hoá trị.
D. X7Y; liên kết cộng hoá trị.
Bài 1/ Nguyên tố X có STT 20, chu kì 4, nhóm IIA. Hãy cho biết:
- Số proton, số electron trong nguyên tử X?
- Số lớp electron trong nguyên tử X?
- Số eletron lớp ngoài cùng trong nguyên tử X?
Bài 2/ Cấu hình electron nguyên tử của một nguyên tố Y là: 1s22s22p63s23p5.
Hãy cho biết vị trí của nguyên tố Y trong bảng tuần hoàn (ô, chu kỳ, nhóm) của Y trong bảng tuần hoàn (có giải thích)?
Bài tập 3/ Nguyên tố X có STT 7, chu kì 2, nhóm VA và nguyên tố Y có STT 13, chu kì 3, nhóm III A
Hãy cho biết các tính chất của nguyên tố X và Y:
- Là kim loại hay phi kim? Vì sao?
- Hóa trị cao nhất trong hợp chất với oxi?
- Hóa trị trong hợp chất với hidro (nếu có)?
- Công thức oxit cao nhất?
- Công thức hợp chất khí với hidro (nếu có) ?
- Công thức hidroxit tương ứng?
X là nguyên tố hóa học có số điện tích hạt nhân là 1,76.10-18 (C). Y là nguyên tố có số electron lớp ngoài cùng bằng 7. Hợp chất tạo bởi X, Y có công thức và liên kết hóa học là
A. X2Y, liên kết cộng hóa trị.
B. XY2, liên kết cho – nhận.
C. XY, liên kết cộng hóa trị.
D. XY, liên kết ion.
X là nguyên tố hóa học có số điện tích hạt nhân 1 , 76 . 10 - 18 . Y là nguyên tố có số electron lớp ngoài cùng bằng 7. Hợp chất tạo bởi X, Y có công thức và liên kết hóa học là
A. X 2 Y , liên kết cộng hóa trị
B. X Y 2 , liên kết cho – nhận
C. XY, liên kết cộng hóa trị
D. XY, liên kết ion
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3 s 2 , nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 2 s 2 2 p 3 . Công thức phân tử của hợp chất tạo bởi X và Y có dạng
![]()
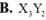
![]()
![]()
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3s2, nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 2s22p3. Công thức phân tử của hợp chất tạo bởi X và Y có dạng
A. X2Y3.
B. X3Y2.
C. X5Y2.
D. X2Y2.
X là nguyên tố thuộc nhóm IVA, chu kì 5 của bảng tuần hoàn. Có các phát biểu sau:
(1) X có 4 lớp electron và có 20 electron p.
(2) X có 5 electron hóa trị và 8 electron s.
(3) X có thể tạo được hợp chất bền với oxi có công thức hóa học X O 2 v à X O 3 .
(4) X có tính kim loại mạnh hơn so với nguyên tố có số thứ tự 33.
(5) X ở cùng nhóm với nguyên tố có số thứ tự 14.
Trong các phát biểu trên, số phát biểu đúng là
A. 2
B. 3
C. 4
D. 5