Chọn B
Số khối A = 12 + 12 = 24.
Số hiệu nguyên tử Z = số proton = 12.
Kí hiệu nguyên tử là
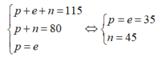
Chọn B
Số khối A = 12 + 12 = 24.
Số hiệu nguyên tử Z = số proton = 12.
Kí hiệu nguyên tử là
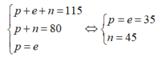
Nguyên tử magie (số hiệu nguyên tử là 12, số khối là 24) có
A. 12 proton, 12 nơtron, 12 electron.
B. 24 proton, 12 nơtron, 12 electron.
C. 12 proton, 12 nơtron, 24 electron.
D. 12 proton, 24 natron, 24 electron.
Nguyên tử nguyên tố X có 12 proton và 12 nơtron. Kí hiệu nguyên tử của X là
A. X 12 24
B. X 12 12
C. X 24 24
D. X 24 12
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3s², có A=24 a)Viết cấu hình electron nguyên tử đầy đủ của X b) số proton,số electron, số nơtron? c) viết kí hiệu nguyên tử ? d) số lớp electron và electron trong mỗi lớp? e) lớp nào có mức năng lượng cao nhất? f) cho biết phân lớp electron có mức năng lượng cao nhất? g) Nêu tính chất hoá học cơ bản của X và giải thích? h)Nguyên tố s,p,d hay f? Vì sao?
Câu 10: Số hạt proton có trong 0,125 mol nguyên tử là
A. 2,03175.1024. B. 1,9565.1024. C. 1,0535. 1024. D. 9,7825. 1023.
Câu 11: Nguyên tử X có cấu hình electron là 1s22s22p63s2. Số hạt proton của X là
A. 10. B. 12. C. 20. D. 24.
Câu 12: Nguyên tử X có 6 electron. Điện tích hạt nhân của nguyên tử X là
A. -6. B. 6+. C. 6. D. 0
Câu 13: Dãy thứ tự mức năng lượng nào sau đây không đúng?
A. 2p < 3s < 3p. B. 3s < 3p < 3d. C. 3p < 3d < 4s. D. 3p < 4p < 4d.
Câu 14: Nguyên tử X và Y có đặc điểm sau:
- X có 2 lớp electron, có 4 electron ở phân mức năng lượng cao nhất.
- Y có 3 lớp electron, có 2 electron ở lớp ngoài cùng.
Phát biểu nào sau đây đúng?
A. X và Y đều là kim loại. B. X và Y đều là phi kim.
C. X là kim loại, Y là phi kim. D. X là phi kim, Y là kim loại.
Câu 15: Nguyên tử X có 4 lớp electron. Số electron tối đa có thể có ở lớp thứ N của X là
A. 6. B. 8. C. 18. D. 32.
Câu 16: Nguyên tử X có tổng số hạt cơ bản là 46 và có số khối bằng 31. Tổng số hạt mang điện của nguyên tử X là
A. 14. B. 15. C. 28. D. 30.
Câu 17: Trong tự nhiên, nitơ có hai đồng vị bền: 14N, 15N và oxi có ba đồng vị bền: 16O, 17O, 18O. Số loại phân tử N2O tối đa có thể được tạo nên từ các đồng vị trên là
A. 6. B. 9. C. 12. D. 18.
Câu 18: Mg có 2 đồng vị là X và Y. Đồng vị X có số khối là 24. Nguyên tử khối trung bình của Mg là 24,4. Tỉ lệ số nguyên tử giữa X và Y là 3/2. Số khối của đồng vị Y là
A. 27. B. 28. C. 25. D. 26.
Câu 19: Nguyên tử 26Fe có số electron trên phân lớp p là
A. 26. B. 20. C. 12. D. 8.
Câu 20: Cho cấu hình electron của các nguyên tử sau:
(X) 1s2 (Y) 1s22s22p5 (Z) 1s22s22p63s23p1
(R) 1s22s22p63s23p6 (T) 1s22s22p63s23p64s2
(M) 1s22s22p63s23p63d54s1
Số nguyên tử kim loại là
A. 2. B. 3. C. 4. D. 5.d
Câu 21:coi hình

Có 11 proton 12 notron Viết kí hiệu nguyên tử X
Chỉ mik bài này với ạ tổng số hạt proton, nơtron, electron của 1 nguyên tử của nguyên tố x là 40, trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 12. hãy xác định số hiểu nguyên tử, số khối và viết kí hiểu nguyên tử, số khối và viết kí hiệu nguyên tử X
. Nguyên tử của nguyên tố X có tổng số hạt là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12 hạt. Nguyên tố X có số proton là: * 4 điểm 13 14 12 27
Nguyên tố X có tổng số hạt trong nguyên tử là 28. Trong hạt nhân nguyên tử thì số hạt không mang điện nhiều hơn số hạt mang điện là 1. Vậy số khối và kí hiệu hóa học của X là:
A. 7 và Li. B.9 và F. C. 12 và C. D. 16 và O
Nguyên tử nguyên tố X có tổng số hạt là 58, tỉ số giữa số nơtron và số khối là 11/20. Tìm số proton, nơtron, electron, điện tích hạt nhân và kí hiệu nguyên tử của X