Các câu hỏi tương tự
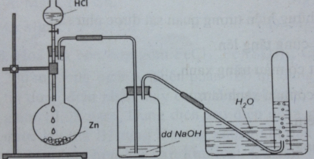
Cho hình vẽ mô tả thí nghiệm điều chế khí X khi cho dung dịch axit tác dụng với chất rắn (kim loại hoặc muối). Hình vẽ dưới minh họa phản ứng nào sau đây? A. CaCO3 + 2HCl → CaCl2 + CO2 + H2O B. Zn + 2HCl → ZnCl2 + H2 C. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O D. Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
Đọc tiếp
Cho hình vẽ mô tả thí nghiệm điều chế khí X khi cho dung dịch axit tác dụng với chất rắn (kim loại hoặc muối). Hình vẽ dưới minh họa phản ứng nào sau đây?
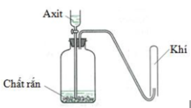
A. CaCO3 + 2HCl → CaCl2 + CO2 + H2O
B. Zn + 2HCl → ZnCl2 + H2
C. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
D. Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
Cho hình vẽ mô tả thí nghiệm điều chế khí X khi cho dung dịch axit tác dụng với chất rắn (kim loại hoặc muối). Hình vẽ dưới minh họa phản ứng nào sau đây? A. CaCO3 + 2HCl → CaCl2 + CO2 + H2O B. Zn + 2HCl → ZnCl2 + H2 C. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O D. Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
Đọc tiếp
Cho hình vẽ mô tả thí nghiệm điều chế khí X khi cho dung dịch axit tác dụng với chất rắn (kim loại hoặc muối). Hình vẽ dưới minh họa phản ứng nào sau đây?
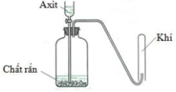
A. CaCO3 + 2HCl → CaCl2 + CO2 + H2O
B. Zn + 2HCl → ZnCl2 + H2
C. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
D. Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
Cho hình vẽ mô tả thí nghiệm điều chế khí X khi cho dung dịch axit tác dụng với chất rắn (kim loại hoặc muối). Hình vẽ dưới minh họa phản ứng nào sau đây? A.
C
u
+
4
H
N
O
3
→
C
u
N
O
3
2
+
...
Đọc tiếp
Cho hình vẽ mô tả thí nghiệm điều chế khí X khi cho dung dịch axit tác dụng với chất rắn (kim loại hoặc muối). Hình vẽ dưới minh họa phản ứng nào sau đây?

A. C u + 4 H N O 3 → C u N O 3 2 + 2 N O 2 + 2 H 2 O
B. C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O
C. F e + 2 H C l → F e C l 2 + H 2
D. 2 K M n O 4 + 16 H C l → 2 K C l + 2 M n C l 2 + 5 C l 2 + 8 H 2 O
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M
→
M
n
+
+
n
e
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong...
Đọc tiếp
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M → M n + + n e
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí nghiệm 1: Tiến hành thí nghiệm theo các bước sau: Bước 1: Rót dung dịch H 2 S O 4 loãng vào cốc thủy tinh.
Bước 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch H 2 S O 4 loãng.
Bước 3: Nối thanh kẽm với thanh đồng bằng dây dẫn (có mắc nối tiếp với một điện kế).
Thí nghiệm 2: Để 3 thanh hợp kim: Cu-Fe (1); Fe-C (2); Fe-Zn (3) trong không khí ẩm
Trong Thí nghiệm 1, thanh kẽm và thanh đồng được nối với nhau bằng dây dẫn cùng nhúng trong dung dịch chất điện li tạo thành một cặp pin điện hóa. Quá trình xảy ra tại anot của pin điện này là
A. Z n → Z n 2 + + 2 e
B. C u → C u 2 + + 2 e
C. 2 H + + 2 e → H 2
D. C u 2 + + 2 e → C u
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M
→
M
n
+
+
n
e
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong...
Đọc tiếp
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M → M n + + n e
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí nghiệm 1: Tiến hành thí nghiệm theo các bước sau: Bước 1: Rót dung dịch H 2 S O 4 loãng vào cốc thủy tinh.
Bước 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch H 2 S O 4 loãng.
Bước 3: Nối thanh kẽm với thanh đồng bằng dây dẫn (có mắc nối tiếp với một điện kế).
Thí nghiệm 2: Để 3 thanh hợp kim: Cu-Fe (1); Fe-C (2); Fe-Zn (3) trong không khí ẩm
Trong Thí nghiệm 2, hợp kim có sắt bị ăn mòn là
A. (1), (2)
B. (2), (3)
C. (1), (3)
D. (1), (2), (3)
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M
→
M
n
+
+
n
e
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong...
Đọc tiếp
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
M → M n + + n e
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí nghiệm 1: Tiến hành thí nghiệm theo các bước sau: Bước 1: Rót dung dịch H 2 S O 4 loãng vào cốc thủy tinh.
Bước 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch H 2 S O 4 loãng.
Bước 3: Nối thanh kẽm với thanh đồng bằng dây dẫn (có mắc nối tiếp với một điện kế).
Thí nghiệm 2: Để 3 thanh hợp kim: Cu-Fe (1); Fe-C (2); Fe-Zn (3) trong không khí ẩm
Từ Thí nghiệm 1, một bạn học sinh đã đưa ra các phát biểu sau
(1) Sau bước 2, chưa có bọt khí thoát ra tại bề mặt của hai thanh kim loại. (2) Sau bước 3, kim điện kế quay chứng tỏ xuất hiện dòng điện. (3) Trong dây dẫn, dòng electron di chuyển từ anot sang catot. (4) Sau bước 3, bọt khí thoát ra ở cả hai điện cực kẽm và đồng. (5) Sau bước 3, thanh đồng bị ăn mòn điện hóa đồng thời với sự tạo thành dòng điện
Số phát biểu đúng là
A. 2
B. 4
C. 3
D. 5
Tiến hành các thí nghiệm sau đây: a) Ngâm một lá kẽm vào dung dịch CuSO4 b) Để thép cacbon ngoài không khí ẩm c) Cho sắt vào dung dịch axit clohidric d) Cho sắt vào dung dịch chứa CuSO4 vào H2SO4 Trong các thí nghiệm trên có bao nhiêu trường hợp xảy ra ăn mòn điện hóa A. 2 B. 3 C. 4 D. 5
Đọc tiếp
Tiến hành các thí nghiệm sau đây:
a) Ngâm một lá kẽm vào dung dịch CuSO4
b) Để thép cacbon ngoài không khí ẩm
c) Cho sắt vào dung dịch axit clohidric
d) Cho sắt vào dung dịch chứa CuSO4 vào H2SO4
Trong các thí nghiệm trên có bao nhiêu trường hợp xảy ra ăn mòn điện hóa
A. 2
B. 3
C. 4
D. 5
Tiến hành các thí nghiệm sau(a) Nhúng dây sắt nguyên chất vào dung dịch
A
g
N
O
3
(b) Cắt miếng tôn (sắt tráng kẽm) để trong không khí ẩm(c) Nhúng dây sắt vào dung dịch
H
2
S
O
4
loãng có nhỏ vài giọt dung dịch
C
u
S
O
4
.(d) Quấn dây đồng vào đinh sắt rồi nhúng vào dung dịch
F
e
C
l...
Đọc tiếp
Tiến hành các thí nghiệm sau
(a) Nhúng dây sắt nguyên chất vào dung dịch A g N O 3
(b) Cắt miếng tôn (sắt tráng kẽm) để trong không khí ẩm
(c) Nhúng dây sắt vào dung dịch H 2 S O 4 loãng có nhỏ vài giọt dung dịch C u S O 4 .
(d) Quấn dây đồng vào đinh sắt rồi nhúng vào dung dịch F e C l 3 Số thí nghiệm Fe bị ăn mòn điện hóa học là
A. 1
B. 2
C. 4
D. 3
Tiến hành các thí nghiệm sau(a) Nhúng thanh đồng nguyên chất vào dung dich
F
e
C
l
3
(b) Cắt nguyên miếng sắt tây ( sắt tráng thiếc), để trong không khí ẩm(c) Nhúng thanh kẽm vào dung dịch
H
2
S
O
4
loãng có nhỏ vài giọt dung dịch
C
u
S
O
4
(d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối Trong các thí nghiệm trê...
Đọc tiếp
Tiến hành các thí nghiệm sau
(a) Nhúng thanh đồng nguyên chất vào dung dich F e C l 3
(b) Cắt nguyên miếng sắt tây ( sắt tráng thiếc), để trong không khí ẩm
(c) Nhúng thanh kẽm vào dung dịch H 2 S O 4 loãng có nhỏ vài giọt dung dịch C u S O 4
(d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối Trong các thí nghiệm trên số thí nghiệm chỉ xảy ra ăn mòn điện hóa là
A. 3
B. 4
C. 2
D. 1
Cho các thí nghiệm sau: (1) Đốt thanh thép–cacbon trong bình khí clo. (2) Nhúng thanh kẽm nguyên chất vào dung dịch FeSO4. (3) Hợp kim đồng thau (Cu–Zn) để trong không khí ẩm. (4) Sắt tây bị xây xước sâu đến lớp bên trong để ngoài không khí ẩm. Thí nghiệm nào xảy ra ăn mòn điện hóa học? A. 2, 3, 4. B. 3, 4. C. 4. D. 1, 3, 4.
Đọc tiếp
Cho các thí nghiệm sau:
(1) Đốt thanh thép–cacbon trong bình khí clo.
(2) Nhúng thanh kẽm nguyên chất vào dung dịch FeSO4.
(3) Hợp kim đồng thau (Cu–Zn) để trong không khí ẩm.
(4) Sắt tây bị xây xước sâu đến lớp bên trong để ngoài không khí ẩm.
Thí nghiệm nào xảy ra ăn mòn điện hóa học?
A. 2, 3, 4.
B. 3, 4.
C. 4.
D. 1, 3, 4.