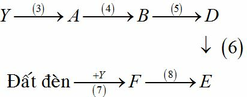Câu I (2,0 điểm): Đơn chất của nguyên tố A là nguyên liệu trong sản xuất phân lân. X và Y là hai hợp chất khí của nguyên tố A. X và Y phản ứng trực tiếp được với nhau tạo thành đơn chất A. X và Y đều phản ứng được với nước vôi trong và dung dịch thuốc tím. Khi sục X hoặc Y cùng với khí clo vào nước đều có phản ứng hóa học xảy ra. Chọn các chất X, Y thích hợp (biết MX > MY) và viết phương trình hóa học của các phản ứng xảy ra.
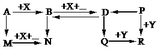
Câu II (4,0 điểm): 1. Xác định các chất A, B, D, E rồi viết phương trình hóa học để thực hiện các biến đổi sau. Biết rằng A là chất tan có nhiều trong nước biển, D và E là chất có tính tẩy màu. A B D E 2. a) Khi sản xuất bánh bao, người ta thường trộn bột mì với một ít bột chất A màu trắng rồi thêm nước và trộn kỹ, sau đó làm thành nhiều chiếc bánh nhỏ. Những chiếc bánh này cho vào lò và nung ở nhiệt độ cao, sau một thời gian nung sẽ thu được những chiếc bánh bao to hơn, thơm ngon và rất hấp dẫn người ăn. Em hãy cho biết công thức hóa học của chất A và giải thích vai trò của nó trong sản xuất bánh bao bằng phương trình hóa học của phản ứng xảy ra. b) Khi chúng ta rót bia ra cốc, thường thấy có bọt khí sủi lên. Em hãy cho biết bọt khí đó là chất gì? Hãy giải thích tác dụng của bọt khí đó. 3. Trong phòng thí nghiệm chỉ có cốc không chia độ, ống đong, bơm khí CO2, Khí CO2 và dung dịch NaOH. Em hãy trình bày cách tạo ra dung dịch chứa đồng thời 2 muối NaHCO3 và Na2CO3 có cùng nồng độ CM.
Câu III (3,0 điểm): 1. Xác định các chất rồi hoàn thành các phương trình hóa học sau CaC2 + A → B + C (1) C + A → D (2) D , , o ⎯⎯⎯⎯→ xt p t C PVC (3) C + G ⎯⎯⎯→NH3 J↓ + H (4) J + A → M↓(trắng) + C (5) 2. Một hỗn hợp X chứa 4 chất khí gồm: CH4; C2H4; C2H2; SO2. Hãy trình bày phương pháp hóa học để chứng minh sự tồn tại của mỗi khí trong hỗn hợp X.
Câu IV (5,0 điểm): 1. Nhỏ từ từ 200 ml dung dịch HCl 2M vào 100 ml dung dịch Na2CO3 3M và NaHCO3 1M thu được dung dịch X và V lít CO2 (ở đktc). Thêm 200 ml dung dịch Ba(OH)2 2M vào dung dịch X thì thu được m gam kết tủa. Tính giá trị của m và V 2. Cho 18,0 gam hỗn hợp A gồm Mg và Al vào bình kín chứa 11,2 lít hỗn hợp khí Cl2 và O2, nung nóng bình đến phản ứng hoàn toàn thì thu được 45,7 gam hỗn hợp chất rắn B. Hòa tan hết chất rắn B vào dung dịch HCl dư thu được dung dịch C và 4,48 lít khí H2. Tính % khối lượng mỗi kim loại trong hỗn hợp A (biết các khí đo ở đktc). 3. Hòa tan 14,2 gam hỗn hợp X gồm MgCO3 và một muối cacbonat của kim loại M vào một lượng vừa đủ dung dịch HCl 7,3% thu được dung dịch Y và 3,36 lít khí CO2 (ở đktc). Nồng độ của MgCl2 trong Y là 6,028%. Cho dung dịch NaOH dư vào Y, lọc kết tủa đem nung ngoài không khí đến khối lượng không đổi thu được m gam chất rắn. Xác định tên kim loại M và tính giá trị của m.
Câu V (3,0 điểm): 1. Cho 3 hidrocacbon X, Y, Z đều có công thức phân tử dạng CnH2n + 2. Tỉ khối hơi của mỗi hiđrocacbon so với N2 đều nhỏ hơn 4,0. Khi tiến hành phản ứng thế với Cl2 theo tỉ lệ số mol là 1: 1 thì mỗi chất chỉ tạo ra được một dẫn xuất thế monoclo. Xác định CTCT của X, Y, Z và các dẫn xuất monoclo của chúng. Biết MX < MY < MZ 2. Cho hỗn hợp X gồm CO2 và O2 có 100 3 M = . Lấy 20,16 lít X (ở đktc) trộn với một lượng hiđrocacbon A được hỗn hợp khí Y có tỉ khối đối với hiđro là 17,5 rồi cho vào một bình kín, áp suất khí trong bình lúc này là P atm, nhiệt độ là 00C. Đốt cháy hỗn hợp khí Y đến phản ứng hoàn toàn rồi đưa bình về nhiệt độ ban đầu thì áp suất khí trong bình lúc này là P/3. (Biết thể tích chất rắn trong bình là không đáng kể). Xác định công thức phân tử của A và viết các công thức cấu tạo có thể có của A.
Câu VI (3,0 điểm): Trong phòng thí nghiệm để điều chế một số khí tinh khiết người ta lắp dụng cụ như hình vẽ sau (Bình A, C, D chứa chất lỏng, B chứa chất rắn, E chứa chất khí). 1. Hãy cho biết sơ đồ dụng cụ trên dùng để điều chế và thu khí nào trong những khí sau đây: CH4; CO2; Cl2. 2. Viết phương trình hóa học của phản ứng điều chế khí đó. 3. Cho biết vai trò của các bình C và D ứng với mỗi khí được xác nhận. -------HẾT ------
ai có thời gian chữa giúp em đề này vs ạ ![]()
cho mình hỏi xíu, bạn ở nghệ an đúng không?