Protein
Nội dung lý thuyết
Các phiên bản khácPROTEIN
I. TỔNG QUAN VỀ PROTEIN
1. Cấu trúc hóa học của protein
- Protein là hợp chất hữu cơ gồm 4 nguyên tố cơ bản C, H, O, N và có thể có thêm S.
- Protein thuộc loại đại phân tử, phân tử lớn nhất dài 0,1 micromet, khối lượng phân tử có thể đạt tới 1,5 triệu đ.v.C.
- Protein được cấu tạo theo nguyên tắc đa phân, các đơn phân là các axit amin.
- Cấu tạo 1 axit amin: NH2 - R – COOH (Gồm 3 thành phần)
 + nhóm amin (_NH2),
+ nhóm amin (_NH2),
+ nhóm carboxyl (-COOH)
+ và cuối cùng là nguyên tử C trung tâm đính với các nguyên tử H và 1 gốc R (Gốc hydro cacbon: CxHy - R).

- Khối lượng 1 phân tử aa bằng 110đvC
- Các axit amin sắp xếp và liên kết nhau tạo thành chuỗi polypeptid (protein). Liên kết peptit được tạo thành do nhóm COOH của axit amin này liên kết với nhóm NH2 của axit amin tiếp theo và giải phóng 1 phân tử H2O (phản ứng trùng ngưng).


- Có 20 loại axit amin khác nhau => có khoảng 20 gốc R khác nhau. Gốc R quyết định tính chất của axit amin.
- Từ 20 loại axit amin kết hợp với nhau theo những cách khác nhau tạo nên vô số loại prôtêin khác nhau (trong các cơ thể động vật, thực vật ước tính có khoảng 1014 – 1015 loại prôtêin). Mỗi loại prôtêin đặc trưng bởi số lượng, thành phần và trình tự sắp xếp các axit amin trong phân tử. Vì vậy, trong thiên nhiên các prôtêin vừa rất đa dạng, lại vừa mang tính chất đặc thù.
2. Cấu trúc không gian của Protein
- Protein có 4 bậc cấu trúc không gian cơ bản:
Cấu trúc bậc 1
 |
- Thành phần, số lượng, trình tự sắp xếp của các axit amin trong chuỗi polypeptit thể hiện cấu trúc bậc 1 của protein. Các axit amin liên kết với nhau bằng các liên kết peptit tạo nên chuỗi polypeptit. Đầu mạch polypeptit là nhóm amin của axit amin thứ nhất và cuối mạch là nhóm cacboxyl của axit amin cuối cùng.
- Cấu trúc bậc 1 của protein có vai trò tối quan trọng vì trình tự các axit amin trên chuỗi polypeptit sẽ thể hiện tương tác giữa các phần trong chuỗi polypeptit, là cơ sở cho việc hình thành cấu trúc không gian của protein và từ đó quy định đặc tính của protein. Phân tử protein ở bậc 1 chưa có hoạt tính sinh học vì chưa hình thành nên các trung tâm hoạt động. Phân tử protein ở cấu trúc bậc 1 chỉ mang tính đặc thù về thành phần axit amin, trật tự các axit amin trong chuỗi. Sự sai lệch trong trình tự sắp xếp của các axit amin có thể dẫn đến sự biến đổi cấu trúc và tính chất của protein.
- Trong tế bào protein thường tồn tại ở các bậc cấu trúc không gian. Sau khi chuỗi polypeptit - protein bậc 1 được tổng hợp tại ribosome, nó rời khỏi ribosome và hình thành cấu trúc không gian (bậc 2, 3, 4) rồi mới di chuyển đến nơi sử dụng thực hiện chức năng của nó.
Cấu trúc bậc 2
- Cấu trúc bậc 2 của protein là sự sắp xếp đều đặn các chuỗi polypeptit trong không gian. Chuỗi polypeptit thường không ở dạng thẳng mà xoắn lại tạo nên cấu trúc xoắn α và cấu trúc nếp gấp β, được cố định bởi các liên kết hydro giữa những axit amin ở gần nhau. kiểu chuỗi anpha một vòng xoắn có 3,7 axit amin, kiểu chuỗi bêta mỗi vòng xoắn có 5,1 axit amin.
- Liên kết hydro được tạo thành giữa các nhóm cacboxyl của 1 liên kết peptit với nhóm –NH của liên kết peptide thứ tự sau nó (cách nhau 3 gốc axit amin) trên cùng một mạch polypeptit
- Ví dụ : Các protein sợi như keratin, Collagen... (có trong lông, tóc, móng, sừng) gồm nhiều xoắn α, trong khi các protein cầu (hemoglobin và mioglobin) có nhiều nếp gấp β hơn.
Cấu trúc bậc ba
 |
| Hình 1: Cấu trúc không gian của Protein |
- Các xoắn a hoặc gấp nếp b lại có thể cuộn lại với nhau thành búi có cấu hình không gian ba chiều đặc trưng cho từng loại protein. Đó là cấu trúc bậc 3 của protein. Cấu trúc không gian này quyết định hoạt tính chức năng của protein. Cấu trúc này lại đặc biệt phụ thuộc vào tính chất của nhóm -R trong các mạch polypeptit.
- Cấu trúc bậc 3 là dạng không gian của cấu trúc bậc 2, làm cho phân tử protein có hình dạng gọn hơn trong không gian, giúp cho phân tử protein ổn định trong môi trường sống. Cấu trúc bậc 3 đã tạo nên trung tâm hoạt động của phần lớn các loại enzym.
- Cấu trúc bậc 3 được giữ vững nhờ các liên kết cầu disunfit (-S-S-), tương tác VanderWaals, liên kết hydro, liên kết ion. Liên kết -S-S- được hình thành từ hai phân tử cystein nằm xa nhau trên mạch peptit nhưng gần nhau trong cấu trúc không gian do sự cuộn lại của mạch polypeptit. Đây là liên kết đồng hoá trị nên rất bền vững. Vì vậy khi phá vỡ các liên kết này phân tử duỗi ra đồng thời làm thay đổi một số tính chất của nó, đặc biệt là tính tan và hoạt tính xúc tác của nó.
Cấu trúc bậc bốn
- Là một trạng thái tổ hợp hình thành từ nhiều tiểu phần protein đã có cấu trúc bậc ba hoàn chỉnh. Khi protein có chứa từ 2 chuỗi polypeptit trở lên, chúng có cấu trúc bậc 4. Các chuỗi polypeptide liên kết với nhau nhờ các liên kết yếu như liên kết hyđro.
- Phân tử protein có cấu trúc bậc 4 có thể phân li thuận nghịch thành các tiểu phần đơn vị. Khi phân li, hoạt tính sinh học của nó bị thay đổi hoặc có thể mất hoàn toàn. Do tồn tại tương tác giữa các tiểu phần đơn vị nên khi kết hợp với một chất nào đó dù là phân tử bé cũng kéo theo những biến đổi nhất định trong cấu trúc không gian của chúng.
- Rất nhiều trường hợp protein phải tổ hợp lại mới có hoạt tính sinh học. Trong những trường hợp này, cấu trúc bậc bốn là điều kiện để hình thành nên tính năng mới của protein.
Ví dụ về cấu trúc bậc bốn:
- Hemoglobin (Huyết sắc tố) gồm 4 tiểu phần protein: hai tiểu phần α và hai tiểu phần β. Nếu 4 tiểu phần tách rời nhau thì mỗi tiểu phần không thể vận chuyển được một phân tử O2 Khi kết hợp lại thành trạng thái tetramer tạo thành một khối không gian đặc thù gần như hình tứ diện thì mới có khả năng kết hợp và vận chuyển khí oxy. Một phân tử hemoglobin (Hít) vận chuyển được 4 phân tử oxy.
- Tuỳ theo protein mà số lượng monomer có thể thay đổi từ 2,4,6,8 là phổ biến, cá biệt có thể lên tới trên 50 monomer.
- Sự hình thành cấu trúc bậc bốn tạo điều kiện cho quá trình điều tiết sinh học thêm tinh vi, chính xác.
* Lưu ý:
- Cấu trúc bậc 1 và bậc 2 chưa thực hiện các chức năng sinh học, chỉ có bậc 3 và 4 khi ở dạng cấu trúc không gian mới tham gia thực hiện chức năng sinh học.
- Khi nói polypeptid tức là vẫn còn acid amin mở đầu: aamđ - aa1 - aa2 - ... - aan
- Khi nói protein (protein hoàn chỉnh) tức là không có acid amin mở đầu: aa1 - aa2 - ... – aan
3. Tính chất của Protein
- Protein có tính đa dạng và đặc thù: được quy định bởi số lượng + thành phần + trật tự sắp xếp của các aa trong chuỗi pôlipeptit.
4. Chức năng của protein
Prôtêin đảm nhiệm nhiều chức năng liên quan đến toàn bộ hoạt động sống của tế bào, quy định các tính trạng và các tính chất của cơ thể sống.
|
Loại protein |
Chức năng |
Ví dụ |
|
Protein cấu trúc |
- Cấu trúc, nâng đỡ |
- Collagen và Elastin tạo nên cấu trúc sợi rất bền của mô liên kết, dây chẳng, gân. Keratin tạo nên cấu trúc chắc của da, lông, móng. Protein tơ nhện, tơ tằm tạo nên độ bền vững của tơ nhện, vỏ kén |
|
Protein Enzyme |
- Xúc tác sinh học: tăng nhanh, chọn lọc các phản ứng sinh hóa |
- Các Enzyme thủy phân trong dạ dày phân giải thức ăn, Enzyme Amylase trong nước bọt phân giải tinh bột chín, Enzyme Pepsin phân giải Protein, Enzyme Lipase phân giải Lipid |
|
Protein Hormone |
- Điều hòa các hoạt động sinh lý |
- Hormone Insulin và Glucagon do tế bào đảo tụy thuộc tuyến tụy tiết ra có tác dụng điều hòa hàm lượng đường Glucose trong máu động vật có xương sống |
|
Protein vận chuyển |
- Vận chuyển các chất |
- Huyết sắc tố Hemoglobin có chứa trong hồng cầu động vật có xương sống có vai trò vận chuyển Oxy từ phổi theo máu đi nuôi các tế bào |
|
Protein vận động |
- Tham gia vào chức năng vận động của tế bào và cơ thể |
- Actinin, Myosin có vai trò vận động cơ. Tubulin có vai trò vận động lông, roi của các sinh vật đơn bào |
|
Protein thụ quan |
- Cảm nhận, đáp ứng các kích thích của môi trường |
- Thụ quan màng của tế bào thần kinh khác tiết ra (chất trung gian thần kinh) và truyền tín hiệu |
|
Protein dự trữ |
- Dự trữ chất dinh dưỡng |
- Albumin lòng trắng trứng là nguồn cung cấp axit amin cho phôi phát triển. Casein trong sữa mẹ là nguồn cung cấp Axit amin cho con. Trong hạt cây có chứa nguồn protein dự trữ cần cho hạt nảy mầm. |
II. CÔNG THỨC VÀ BÀI TẬP
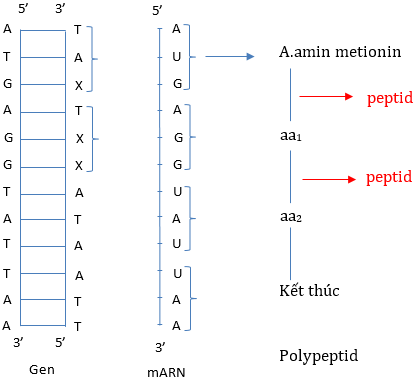
1. Tính số axit amin
- Tính số axit amin trong chuỗi polipeptid: \(\frac{N}{2.3} - 1 = \frac{rN}{3} - 1\)
- Tính số axit amin trong phân tử protein (polypeptid hoàn chỉnh, protein hoàn chỉnh): \(\frac{N}{2.3} - 2 = \frac{rN}{3} - 2\)
Ví dụ 1: Một chuỗi polypetid có ℓ = 1500Å. Biết một axit amin có độ dài trung bình 3Å. Hãy xác định:
a) Số axit amin có trong mỗi chuỗi polypetid đó.
b) Số nu có trong mARN đã tổng hợp chuỗi polypetid đó.
Giải:
a. Polypetid = 1500Å (1aa = 3Å)
⇒ Số aa trong polypetid: \(\frac{1500}{3} = 500\) (aa)
b. Số rN của mARN: \(\frac{rN}{3} - 1 = 500\)
⇔ rN = 501*3 = 1503
2. Xác định số liên kết peptid
- Số LK peptid trong chuỗi: aamđ – aa1 – aa2 – ... – aan
Gọi a số aa có trong chuỗi polypetid ⇒ Số LK peptid: (a – 1)
- Số LK peptid trong phân tử protein
Gọi d là số aa trong chuỗi polypetid ⇒ Số LK peptid: (b – 1)
Ví dụ 2: Một chuỗi polypetid hoàn chỉnh có 248 axit amin.
a) Xác định số bộ ba trên mARN.
b) Xác định số nu trên gen quy định để tổng hợp protein đó.
c) Xác định số liên kết peptid có trong chuỗi polypetid đó.
Giải:
Polypetid hoàn chỉnh có 248 aa
Ta có: \(\frac{N}{2.3} - 2 = \frac{rN}{3} - 2 = 248\)
a) Số bộ ba trên mARN: \(\frac{rN}{3} = 250\)
b) Số nu trên gen quy định để tổng hợp protein:
Ta có: \(\frac{N}{2.3} -2 = 248\)
⇔ N = 1500 (nu)
c) Số LK peptid có trong chuỗi polypeptid = 248 – 1 = 247 (LK)