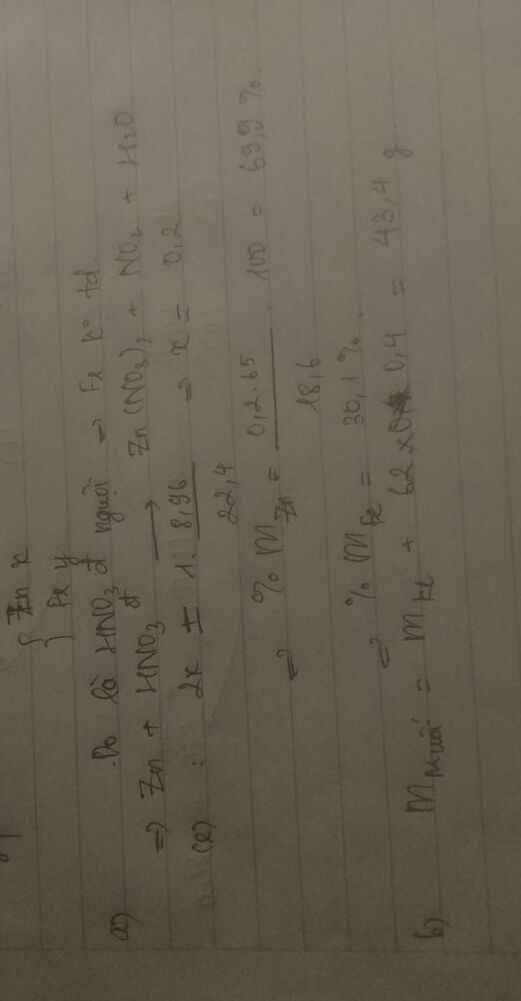Bài 23: Hiđro Clorua - Axit Clohidric và muối Clorua
cho 23,75g hỗn hợp gồm zn và Fe tác dụng hết với dung dịch HCl,thoát ra 8,96 lít H_2 a. Tính khối lượng và phần trăm mỗi khối lượng b. Khối lượng muối tạo thành Biết Fe là 56 Zn 65 Cl là 35,5
Gọi số mol Zn, Fe là a, b (mol)
=> 65a + 56b = 23,75 (1)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a--------------->a------->a
Fe + 2HCl --> FeCl2 + H2
b----------------->b----->b
=> a + b = 0,4 (2)
(1)(2) => a = 0,15 (mol); b = 0,25 (mol)
=> mZn = 0,15.65 = 9,75 (g); mFe = 0,25.56 = 14 (g)
\(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{9,75}{23,75}.100\%=41,05\%\\\%m_{Fe}=\dfrac{14}{23,75}.100\%=58,95\%\end{matrix}\right.\)
b) mZnCl2 = 0,15.136 = 20,4 (g)
mFeCl2 = 0,25.127 = 31,75 (g)
=> mmuối = 20,4 + 31,75 = 52,15 (g)
Đúng 1
Bình luận (0)
Cho 5,475 g HCl vào 500ml Ca(OH)2 0,2 M Thu được dung dịch A thể tích thay đổi không đáng kể a Viết phương trình phản ứng xảy ra B Tính CM các chất sau phản ứng
2HCl+Ca(OH)2->CaCl2+2H2O
0,15------0,075-----0,075-----0,15
n HCl=\(\dfrac{5,475}{36,5}\)=0,15 mol
n Ca(OH)2=0,2.0,5 =0,1 mol
=>Ca(OH)2 dư
CM Ca(OH)2 dư =\(\dfrac{0,025}{0,5}\)=0,05M
CM CaCl2 = \(\dfrac{0,075}{0,5}\)=0,15 M
Đúng 1
Bình luận (0)
Cho 11g hỗn hợp sắt và nhôm tác dụng với 200ml HCl ( vừa đủ). Sau phản ứng thu được dung dịch chứa 39,4g muối và V lít H2.
a. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b. Tìm V và nồng độ dd HCl đã dùng
\(\left\{{}\begin{matrix}Fe\\Al\end{matrix}\right.+HCl->\left\{{}\begin{matrix}FeCl2\\AlCl3\end{matrix}\right.+H2\)
Ta có số mol Fe là x , Al là y (mol)
\(\left\{{}\begin{matrix}56x+27y=11\\127x+133,5y=39,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%mFe=\dfrac{0,1.56}{11}=50,9\%\\\%mAl=\dfrac{0,2.27}{11}=49,09\%\end{matrix}\right.\)
Bảo toàn e :
\(2.nH2=2.nFe+3.nAl\Rightarrow nH2=0,4\left(mol\right)\)
\(V=0,4.22,4=8,96\left(l\right)\)
\(nFe=nFeCl2=0,1\left(mol\right)\)
\(nAl=nAlCl3=0,2\left(mol\right)\)
\(\Rightarrow nHCl\left(pứ\right)=2.0,1+3.0,2=0,8\left(mol\right)\)
\(Cm=\dfrac{n}{V}=\dfrac{0,8}{0,2}=4\left(M\right)\)
Đúng 2
Bình luận (1)
Hòa tan M gam hỗn hợp Zn và Fe trong dd HCl dư thu đc 39g muối và 6,72 lít khí (đktc).
a. Tính % khối lượng từng chất trong hỗn hợp ban đầu.
b. Tính nồng độ phần trăm của 200g dd HCl.
Vì sao lại sử dụng phương pháp sufat để điều chế Hcl trong công nghiệp?
Giúp em với ạ @@
phương pháp sunfat rẻ, dễ thực hiện , có thể tạo axit đặc
H2SO4+2NaCl->Na2SO4+2HCl
Đúng 2
Bình luận (2)
Cho 11,2 gam hỗn hợp Cu và kim loại M tác dụng với dung dịch HCl dư thu được 3,136 lít (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch HNO3 loãng thu được 3,92 lít khí NO (đktc, sản phẩm khử duy nhất). Kim loại M là :
A. Mg B. Fe C. Mg hoặc Fe D. Mg hoặc Zn
Gọi số mol Cu, M là a, b (mol)
=> 64a + b.MM = 11,2 (1)
\(n_{NO}=\dfrac{3,92}{22,4}=0,175\left(mol\right)\)
Cu0 - 2e --> Cu+2
a--->2a
M0 - ne --> M+n
b--->bn
N+5 + 3e --> N+2
0,525<-0,175
Bảo toàn e: 2a + bn = 0,525 (2)
(1)(2) => 32bn - bMM = 5,6 (3)
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: 2M + 2xHCl --> 2MClx + xH2
\(\dfrac{0,28}{x}\)<---------------------0,14
=> \(\dfrac{0,28}{x}=b\) (4)
(3)(4) => MM = 32n - 20x (g/mol)
Và \(0< x\le n\)
TH1: x = n = 1 => MM = 12 (Loại)
TH2: x = n = 2 => MM = 24 (Mg)
TH3: x = n = 3 => MM = 36 (Loại)
TH4: x = 1; n = 2 => MM = 44 (Loại)
TH5: x = 1; n = 3 => MM = 76 (Loại)
TH6: x = 2; n = 3 => MM = 56 (Fe)
Vậy M có thể là Mg hoặc Fe
=> C
Đúng 1
Bình luận (0)
Nung 16 gam hỗn hợp X gồm Al, Mg, Zn, Cu trong bình đựng oxi dư thu được m gam hỗn hợp các oxit Y. Hòa tan hoàn toàn m gam Y thì cần 160 ml dung dịch HCl 3,5M. Tính m.
\(n_{HCl}=0,16.3,5=0,56\left(mol\right)\)
=> \(n_{H_2O}=\dfrac{0,56}{2}=0,28\left(mol\right)\)
=> nO = 0,28 (mol)
=> m = 16 + 0,28.16 = 20,48 (g)
Đúng 1
Bình luận (0)
\(n_{HCl}=0,16.3,5=0,56\left(mol\right)\\ n_{O\left(trong.oxit\right)}=n_{H_2O}=\dfrac{n_{HCl}}{2}=\dfrac{0,56}{2}=0,28\left(mol\right)\\ m=m_{hh.oxit}=m_{hhX}+0,28.16=16+4,48=20,48\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 3,425 gam hỗn hợp gồm 5 oxit FeO; CuO; Al2O3; ZnO; Fe2O3 tác dụng vừa đủ với 300 ml dung dịch HCl 0,1M. Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Tính m
\(n_{HCl}=0,1.0,3=0,03\left(mol\right)\)
=> \(n_{H_2O}=\dfrac{0,03}{2}=0,015\left(mol\right)\)
Theo ĐLBTKL: \(m_{oxit}+m_{HCl}=m_{muối}+m_{H_2O}\)
=> mmuối = 3,425 + 0,03.36,5 - 0,015.18 = 4,25(g)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 4,8 gam hỗn hợp X gồm CuO và Fe2O3 trong 200ml dung dịch HCl 1M thu được dung dịch Y. Trung hòa dung dịch Y cần vừa đủ 40 ml dung dịch NaOH 1M.a. Tính % khối lượng mỗi oxit trong hỗn hợp ban đầu.b. Cho từ từ đến dư dung dịch KOH vào dung dịch Y đến phản ứng hoàn toàn thu được kết tủa Z. Nung nóng kết tủa Z ngoài không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m.
Đọc tiếp
Hòa tan hoàn toàn 4,8 gam hỗn hợp X gồm CuO và Fe2O3 trong 200ml dung dịch HCl 1M thu được dung dịch Y. Trung hòa dung dịch Y cần vừa đủ 40 ml dung dịch NaOH 1M.
a. Tính % khối lượng mỗi oxit trong hỗn hợp ban đầu.
b. Cho từ từ đến dư dung dịch KOH vào dung dịch Y đến phản ứng hoàn toàn thu được kết tủa Z. Nung nóng kết tủa Z ngoài không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m.
a)
nNaOH = 0,04.1 = 0,04 (mol)
PTHH: NaOH + HCl --> NaCl + H2O
0,04--->0,04
=> nHCl(pư với X) = 0,2.1 - 0,04 = 0,16 (mol)
Gọi số mol CuO, Fe2O3 là a, b (mol)
=> 80a + 160b = 4,8 (1)
PTHH: CuO + 2HCl --> CuCl2 + H2O
a----->2a
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
b----->6b
=> 2a + 6b = 0,16 (2)
(1)(2) => a = 0,02; b = 0,02
=> \(\left\{{}\begin{matrix}\%m_{CuO}=\dfrac{0,02.80}{4,8}.100\%=33,33\%\\\%m_{Fe_2O_3}=\dfrac{0,02.160}{4,8}.100\%=66,67\%\end{matrix}\right.\)
b) Chất rắn thu được gồm CuO, Fe2O3
Bảo toàn Cu: nCuO = 0,02 (mol)
Bảo toàn Fe: nFe2O3 = 0,02 (mol)
=> m = 0,02.80 + 0,02.160 = 4,8 (g)
Đúng 2
Bình luận (0)