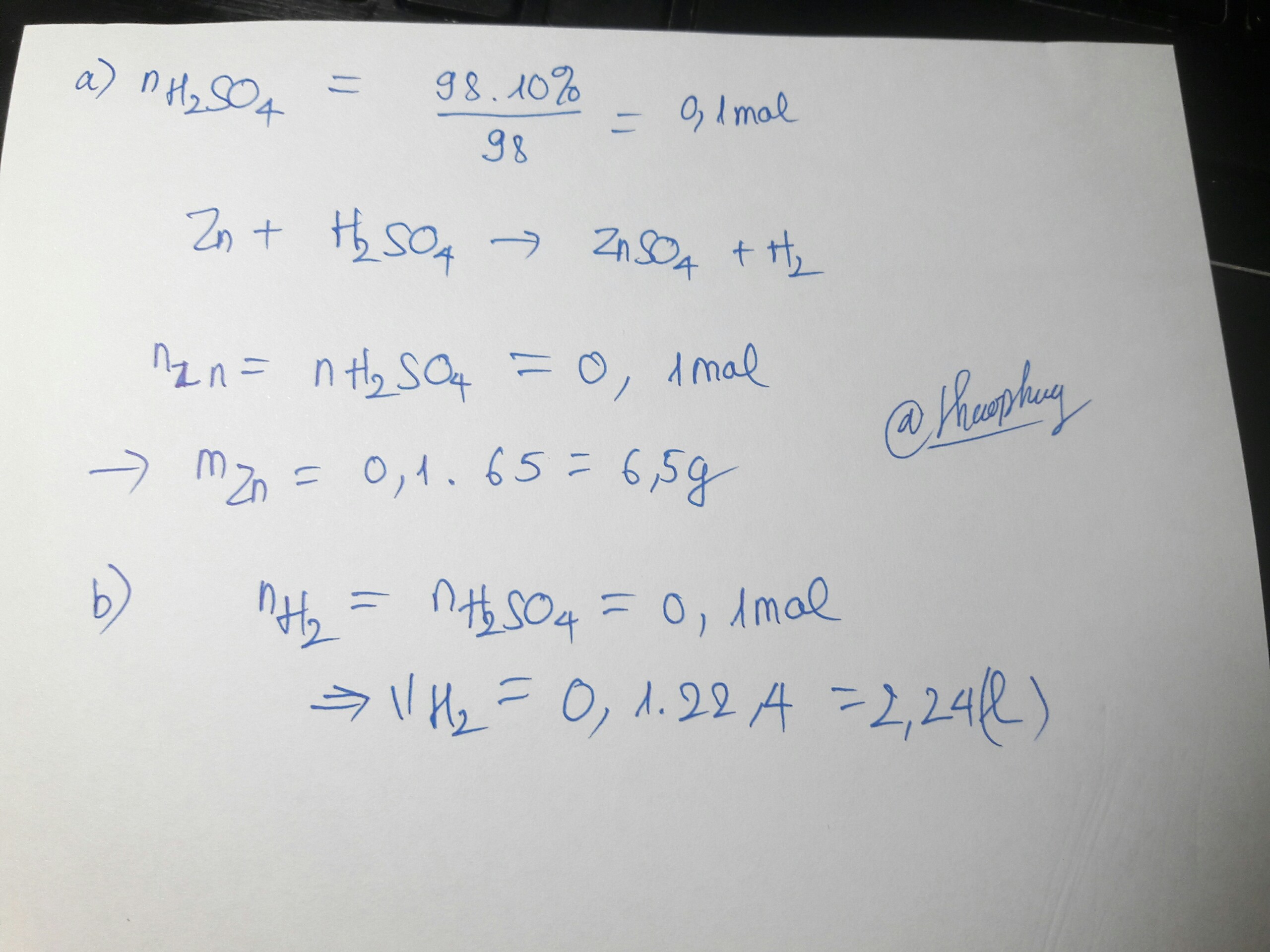Bài 22: Tính theo phương trình hóa học
\(n_{O_2}=\dfrac{7,437}{24,79}=0,3(mol)\\ 4Al+3O_2\xrightarrow{t^o}2Al_2O_3\\ \Rightarrow n_{Al}=0,4(mol)\\ \Rightarrow m_{Al}=0,4.27=10,8(g)\)
Đúng 1
Bình luận (0)
Hợp chất A có tỉ khối so với khí Hiđro là 22
a) Tính khói lượng mol của hợp chất
b) Hãy cho biết 6,1975 lít khí A (ở đk chuẩn) có khối lượng là bao nhiêu gam?
(giúp mik với ak, mai mik KT rồiT-T)
\(a,M_A=22.M_{H_2}=22.2=44(g/mol)\\ b,n_A=\dfrac{6,1975}{24,79}=0,25(mol)\\ \Rightarrow m_A=0,25.44=11(g)\)
Đúng 1
Bình luận (1)
Đốt 5,4 gam magie trong không khí, người ta thu được 10,2 gam magie oxit (MgxOy).
a) Xác định các chỉ số x, y.
b) Lập phương trình hóa học của phản ứng.
c) Tính khối lượng khí oxi đã dùng.
\(a,Mg_x^{II}O_y^{II}\Rightarrow x.II=y.II\Rightarrow \dfrac{x}{y}=1\\ \Rightarrow x=1;y=1\\ b,2Mg+O_2\xrightarrow{t^o}2MgO\\ c,BTKL:m_{O_2}=m_{MgO}-m_{Mg}=10,2-5,4=4,8(g)\)
Đúng 1
Bình luận (0)
điều chế hidro trong phòng thí nghiệm bằng cách hòa tan hết Zn vào 98 gam dung dịch H2SO4 10%. Hãy tính:
a) khối lượng Zn đã tan hết
b) Thể tích khí H2 thu được sau phản ứng
tính độ tan cẩu các chất cho sau đây ở 25'C
a) hòa tan 7,2 gam NaCl trong 20 gâm nước thì thu được dung dịch bão hòa
b) chỉ hòa tan được tối da 55,5 gam AgNO3 trong 25 gam nước
cho a(g) nhôm tác dụng vừa đủ với 300ml dd H2SO4 0,5M đc sản phẩm nhôm sunfat và khì hidro.Tính giá trị a và thể tích
Ta có: \(n_{H_2SO_4}=0,5.\dfrac{300}{1000}=0,15\left(mol\right)\)
\(PTHH:2Al+3H_2SO_4--->Al_2\left(SO_4\right)_3+3H_2\)
Theo PT: \(n_{Al}=\dfrac{2}{3}.n_{H_2SO_4}=\dfrac{2}{3}.0,15=0,1\left(mol\right)\)
\(\Rightarrow a=0,1.27=2,7\left(g\right)\)
Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,15.22,4=3,36\left(lít\right)\)
Đúng 1
Bình luận (0)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(n_{H2SO4_{ }}=0,3.0,5=0,15mol\)
\(\rightarrow n_{Al}=0,1mol\)
\(\rightarrow m_{Al}=0,1.27=2,7g\)
\(V_{H2}=0,15.22,4=3,36l\)
Đúng 1
Bình luận (0)
Lấy 10,2g Al2O3 cho vào 300g dd H2SO4 y% sau PƯ đc dd chứa muối sunfat và nước . tính giá trị y và nồng độ phần trăm của dd sau PƯ .
\(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1(mol)\\ Al_2O_3+3H_2SO_4\to Al_2(SO_4)_3+3H_2O\\ \Rightarrow n_{H_2SO_4}=0,3(mol)n_{Al_2(SO_4)_3}=0,1(mol)\\ \Rightarrow C\%_{H_2SO_4}=\dfrac{0,3.98}{300}.100\%=9,8\%\\ \Rightarrow C\%_{Al_2(SO_4)_3}=\dfrac{0,1.342}{10,2+300}.100\%=11,03\%\)
Đúng 0
Bình luận (2)
cho 2,4g cacbon tác dụng với 2,24 l oxi
a,tính số g cacbonnic sau phản ứng
b, tính số gam chất còn dư
giúp mình với
\(a.n_C=0,2\left(mol\right);n_{O_2}=0,1\left(mol\right)\\ C+O_2-^{t^o}\rightarrow CO_2\\ LTL:\dfrac{0,2}{1}< \dfrac{0,1}{1}\\ \Rightarrow Cdư\\ n_{CO_2}=n_{O_2}=0,1\left(mol\right)\\ \Rightarrow m_{CO_2}=0,1.44=4,4\left(g\right)\\ b.n_{C\left(pư\right)}=n_{O_2}=0,1\left(mol\right)\\ \Rightarrow n_{C\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\\ \Rightarrow m_{C\left(dư\right)}=0,1.12=1,2\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 6,2g Na20 tác dụng vớới 2,6g nước thu đc Natri hiđro xit
a, tính khối lượng NaOH sau phản ứng
b, tính số gam chất còn dư sau phản ứng
giúp mình với
Ta có:
\(n_{Na_2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\left(phần.này.mik.sửa.lại.đề\right)\)
a. \(PTHH:Na_2O+H_2O--->2NaOH\)
Ta thấy: \(\dfrac{0,1}{1}< \dfrac{0,2}{1}\)
Vậy H2O dư.
Theo PT: \(n_{NaOH}=2.n_{Na_2O}=2.0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{NaOH}=40.0,2=8\left(g\right)\)
b. Ta có: \(n_{H_2O_{PỨ}}=n_{Na_2O}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2O_{dư}}=0,2-0,1=0,1\left(mol\right)\)
\(\Rightarrow m_{H_2O_{dư}}=0,1.18=1,8\left(g\right)\)
Đúng 1
Bình luận (1)
tính nồng độ phần trăm của Mg(NO3)2 và MgSO4 trong 400g dd hh chứa lần lượt 0,1 mol Mg(NO3)2 và 0,05 mol MgSO4
\(C\%\left(MgSO_4\right)=\dfrac{0,05.120}{400}.100\%=1,5\%\)
\(C\%\left(Mg\left(NO_3\right)_2\right)=\dfrac{0,1.148}{400}.100\%=3,7\%\)
Đúng 1
Bình luận (0)