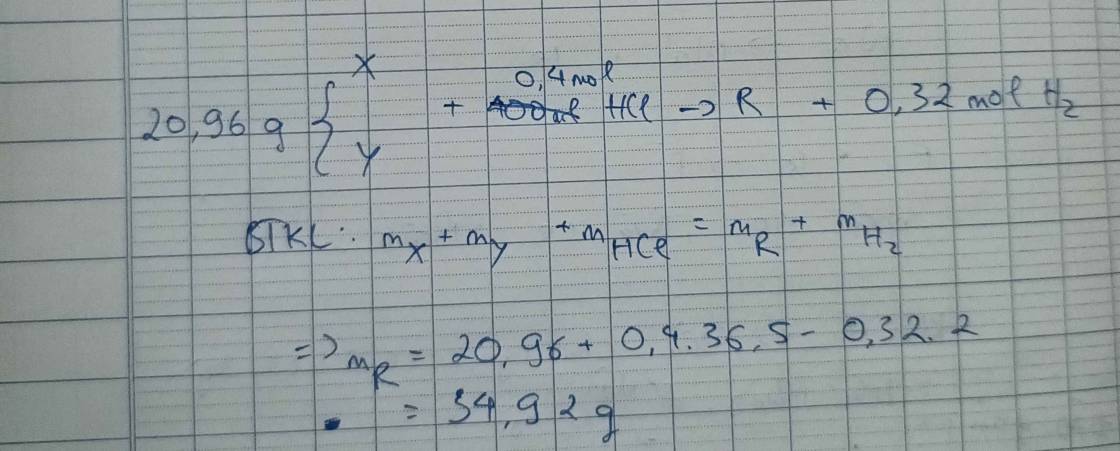Cho 0,85gam hỗn hợp 2 kim loại kiềm A, B thuộc hai chu kì kế tiếp tan hết trong nước thu được dung dịch X. Để trung hòa hết dung dịch X phải dùng 150ml dung dịch HCl 0,2M. Xác đihnj tên và khối lượng (gam) của A, B
Chương 2. Bảng tuần hoàn các nguyên tố hóa học và Định luật tuần hoàn
Gọi CTHH chung của A và B là R.
Ta có: nHCl = 0,15.0,2 = 0,03 (mol)
BTNT Cl: nRCl = nHCl = 0,03 (mol)
BTNT R: nR = nRCl = 0,03 (mol)
\(\Rightarrow M_R=\dfrac{0,85}{0,03}=28,33\)
→ A và B là Na và K.
Ta có: \(\left\{{}\begin{matrix}n_{Na}+n_K=0,03\\23n_{Na}+39n_K=0,85\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{Na}=0,02\left(mol\right)\\n_K=0,01\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Na}=0,02.23=0,46\left(g\right)\)
\(m_K=0,01.39=0,39\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 8,8 gam hỗn hợp X gồm hai kim loại A và B ở hai chu kỳ kế tiếp nhau của im IIA tác dụng hoàn toàn trong 200 ml dung dịch HC1 vừa đủ, sau phản ứng thu được 37 lít khí ( ở đkc) và dung dịch Y.
* Tìm tên 2 kim loại A, B.
* Tính nồng độ mol/lit của các chất trong dung dịch Y. Xem thể tích thay đổi ko đáng kể
bao nhiêu lít khí H2 thoát ra vậy bạn
Đúng 0
Bình luận (0)
1. **Tên hai kim loại A và B:**
- Kim loại A là Zinc (Zn).
- Kim loại B là Aluminum (Al).
2. **Nồng độ mol/lit của các chất trong dung dịch Y:**
- Số mol khí (H2) tạo ra từ phản ứng là 2 mol (theo phương trình phản ứng cân bằng).
- Do đó, nồng độ mol/lit của mỗi chất trong dung dịch Y là:
- Nồng độ mol/lit của ion Zn^2+ là 0.01 M (2 mol / 0.2 L).
- Nồng độ mol/lit của ion Al^3+ là 0.01 M (2 mol / 0.2 L).
- Nồng độ mol/lit của ion Cl^- là 0.02 M (2 mol / 0.2 L).
Lưu ý: Các giả định đã được sử dụng để tính toán, và các giả định này có thể không hoàn toàn chính xác tùy thuộc vào điều kiện cụ thể của bài toán.
Đúng 0
Bình luận (0)
Hai nguyên tố A và B ở 2 nhóm A liên tiếp trong bảng tuần hoàn,A thuộc nhóm VI ở trạng thái đơn chất A và B không phản ứng với nhau tổng số proton trong hạt nhân của A và B là 25. xác định A và B viết cấu hình electron và xác định tính chất hoá học cơ bản của chúng
Xem chi tiết
cho 20,96g hốn hợp gồm 2 kim loại X,Y tác dụng với 400ml dung dịch HCl 1M thu được dung dịch R và 7,168 lít H2(đktc).Cô cạn dung dịch R thu được bao nhiêu g chất rắn khan?
Biết 2,3,7,8 -TCDD là 1 trong những chất thuộc nhóm dioxin(chất màu da cam). 2,3,7,8 -TCDD có công thức C12H4Cl4O2 được mô tả như hình bên. a, Xác định vị trí các nguyên tố có trong 2,3,7,8 -TCDD trong bảng tuần hoàn b,so sánh tính phi kim của các nguyên tố trên với nguyên tố flo
Đọc tiếp
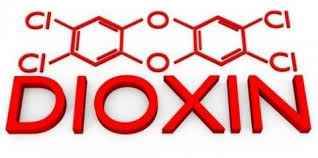
Biết 2,3,7,8 -TCDD là 1 trong những chất thuộc nhóm dioxin(chất màu da cam). 2,3,7,8 -TCDD có công thức C12H4Cl4O2 được mô tả như hình bên. a, Xác định vị trí các nguyên tố có trong 2,3,7,8 -TCDD trong bảng tuần hoàn b,so sánh tính phi kim của các nguyên tố trên với nguyên tố flo
Cho các phát biểu sau:(a) Sulfur là chất rắn, màu trắng, không tan trong nước(b) Sulfur và sulfur dioxide vừa có tính oxi hóa, vừa có tính khử(c) Khi phản ứng với hydrogen, sulfur thể hiện tính oxi hóa(d) Nước thải sinh hoạt là một trong các nguồn phát thải khí SO2(e) Sulfur dioxide được sử dụng để tẩy trắng vải sợi, bột giấy, sản xuất sulfuric acid và diệt nấm mốcCác phát biểu nào là phát biểu đúng ?
Đọc tiếp
Cho các phát biểu sau:
(a) Sulfur là chất rắn, màu trắng, không tan trong nước
(b) Sulfur và sulfur dioxide vừa có tính oxi hóa, vừa có tính khử
(c) Khi phản ứng với hydrogen, sulfur thể hiện tính oxi hóa
(d) Nước thải sinh hoạt là một trong các nguồn phát thải khí SO2
(e) Sulfur dioxide được sử dụng để tẩy trắng vải sợi, bột giấy, sản xuất sulfuric acid và diệt nấm mốc
Các phát biểu nào là phát biểu đúng ?
A và B là 2 nguyên tố thuộc cùng một chu kì. Tổng số proton trong hạt nhân nguyên tử A và B là 30, trong đó số proton của B nhiều hơn của A. A và B tạo với nhau hợp chất AB3. Viết phương trình phản ứng điều chế AB3.
Số hạt proton trung bình là $30 : 2 = 15$
Mặt khác B có số proton nhiều hơn A, suy ra :
+) Số proton của A là 14 ; số proton của B là 16
Suy ra A là Nito ; B là Lưu huỳnh
Mà A và B tạo với nhau hợp chất $AB_3 \Rightarrow $ loại
+) Số proton của A là 13 ; số proton của B là 17
Suy ra A là Al ; B là Clo
PTPU điều chế : $2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3$
Đúng 1
Bình luận (0)
Viết quá trình cho hoặc nhận electron của các nguyên tử sau: Na, Mg, K, Ca, Al, F, Cl, O, N, S.
- Hãy mô tả sự hình thành liên kết ion từ các nguyên tử tương ứng trong các hợp chất sau: NaF,
Na2O, MgO, MgF2.
- Các hợp chất ion có các đặc điểm gì?
1/ Quá trình nhường - nhận electron.
\(Na^0\rightarrow Na^++e\)
\(Mg^0\rightarrow Mg^{2+}+2e\)
\(Ca^0\rightarrow Ca^{2+}+2e\)
\(F^0+e\rightarrow F^-\)
\(Cl^0+e\rightarrow Cl^-\)
\(O^0+2e\rightarrow O^{2-}\)
\(N^0+3e\rightarrow N^{3-}\)
\(S^0+2e\rightarrow S^{2-}\)
2/ Sự hình thành liên kết ion.
- Trong NaF:
+ Nguyên tử Na nhường 1e.
+ Nguyên tử F nhận 1e.
+ Nguyên tử Na và F tích điện trái dấu nên chúng hút nhau tạo thành phân tử NaF.
- Na2O, MgO, MgF2 giải thích tương tự.
3/ Đặc điểm của các hợp chất ion:
- Các hợp chất ion hầu hết là thể rắn ở nhiệt độ thường, khó tan chảy, khó bay hơi. Chẳng hạn, nhiệt độ nóng chảy của NaCl là 801 oC, nhiệt độ sôi của NaCl là 1465 oC.
- Khi các hợp chất này nóng chảy, hoặc hoà tan trong nước, lực hút tĩnh điện giữa các ion này yếu đi, kết quả là chúng phân li ra các ion trần, nên chúng dẫn điện tốt.
- Ở trạng thái rắn, các hợp chất ion không dẫn được điện.
Đúng 2
Bình luận (0)
- Bản chất của liên kết ion ?
- Liên kết ion thưởng gặp giữa loại nguyên tố nào liên kết với nhau? Hình thành bằng cách nào?
- Lấy ví dụ về liên kết ion hình thành bằng cách cho – nhận electron giữa các nguyên tử?
- Lấy ví dụ về liên kết ion được hình thành không phải bằng cách cho nhận electron?
Để đạt được cấu hình electron bền vũng của khí hiếm, các nguyên tử có những cách nào?