Cho V ml dung dịch gồm NaOH 2M và Ba(OH)2 1M tác dụng với 150 ml dung dịch gồm HCl 2M và H2SO4 1M . Được dung dịch A , dung dịch A được trung hòa bởi 200 ml dung dịch HNO3 1M . Tìm giá trị V = ?
Bài 2: Axit - Bazơ - Muối
Cho 200 ml dung dịch gồm KOH 2M và Ca(OH)2 1M trung hòa V ml dung dịch H2SO4 0,5M . Giá trị V = ?
Trộn lẫn 200ml dung dịch h2 SO4 0,0 5M với 300 ml dung dịch HCl 0,1 M (coi h2 SO4 điện li hoàn toàn cả hai nấc)
Trộn 200 ml dung dịch H2SO4 0,1M với 100ml dung dịch Na2SO4 0,3M. Xác định nồng độ các ion có mặt trong dung dịch trên
\(n_{H^+}=0,1.2.0,2=0,04\Rightarrow\left[H^+\right]=\dfrac{0,04}{0,2+0,1}\approx0,13M\)
\(n_{SO_4^{2-}}=0,2.0,1+0,3.0,1=0,05\Rightarrow\left[SO_4^{2-}\right]=\dfrac{0,05}{0,2+0,1}\approx0,17M\)
\(n_{Na^+}=0,3.0,1.2=0,06\Rightarrow\left[Na^+\right]=\dfrac{0,06}{0,2+0,1}\approx0,2M\)
Đúng 0
Bình luận (0)
Tính nồng độ mol/lit của các ion trong dung dịch sau: 200 ml dung dịch chứa 49 gam H2SO4?
\(n_{H^+}=2.n_{H_2SO_4}=\dfrac{2.49}{98}=1\left(mol\right)\Rightarrow\left[H^+\right]=\dfrac{1}{0,2}=5M\)
\(n_{SO_4^{2-}}=n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\Rightarrow\left[SO_4^{2-}\right]=\dfrac{0,5}{0,2}=2,5M\)
Đúng 0
Bình luận (0)
Giải bài tập Hòa tan 14,7gam axitsunfuric vào nước thu được 500ml dung dịch D.Tính nồng độ cation có trong dung dịch D
\(n_{H_2SO_4}=\dfrac{14,7}{98}=0,15\left(mol\right)\\ \left[H_2SO_4\right]=\dfrac{0,15}{0,5}=0,3\left(M\right)\\ \Rightarrow\left[H^+\right]=0,3.2=0,6\left(M\right)\\ \left[SO^{2-}_4\right]=\left[H_2SO_4\right]=0,3\left(M\right)\)
Đúng 1
Bình luận (1)
Những ion nào dưới đây không thể tồn tại trong cùng một dung dịch? A. Na+, Mg2+, NO3-, SO42- B. Cu2+, Fe3+, SO42-, Cl- C. Ba2+, Al3+, Cl-, HSO4- D. K+, HSO4-, OH-, PO43-
Đọc tiếp
Những ion nào dưới đây không thể tồn tại trong cùng một dung dịch?
A. Na+, Mg2+, NO3-, SO42- B. Cu2+, Fe3+, SO42-, Cl-
C. Ba2+, Al3+, Cl-, HSO4- D. K+, HSO4-, OH-, PO43-
các ion có thể cùng tồn tại trong 1 dung dịch là :
A.Na++,Mg2+2+,NO−33−,SO2−4
Đúng 0
Bình luận (1)
Giải giúp mình né
Bảo toàn điện tích:
\(n_{Na^+}+n_{Al^{3+}}=n_{Cl^-}\)
\(\Leftrightarrow n_{Na^+}+0,02.3=0,08\)
\(\Rightarrow n_{Na^+}=0,02\left(mol\right)\)
\(\Rightarrow m=0,02.23+0,02.27+0,08.35,5=3,84\left(g\right)\)
Đúng 1
Bình luận (0)
Giúp mik nhanh câu 2 mình dò lại đáp án mình làm 
a)
Kim loại : $Pb$
Phi kim : $Cl_2,C$
b)
Axit : $CH_3COOH$
Oxit : $Fe_2O_3,CO,N_2O_5$
Bazo : $Ni(OH)_2$
Muối : $KMnO_4,MnSO_4,Na_2HPO_4,NH_4Cl$
Đúng 2
Bình luận (0)
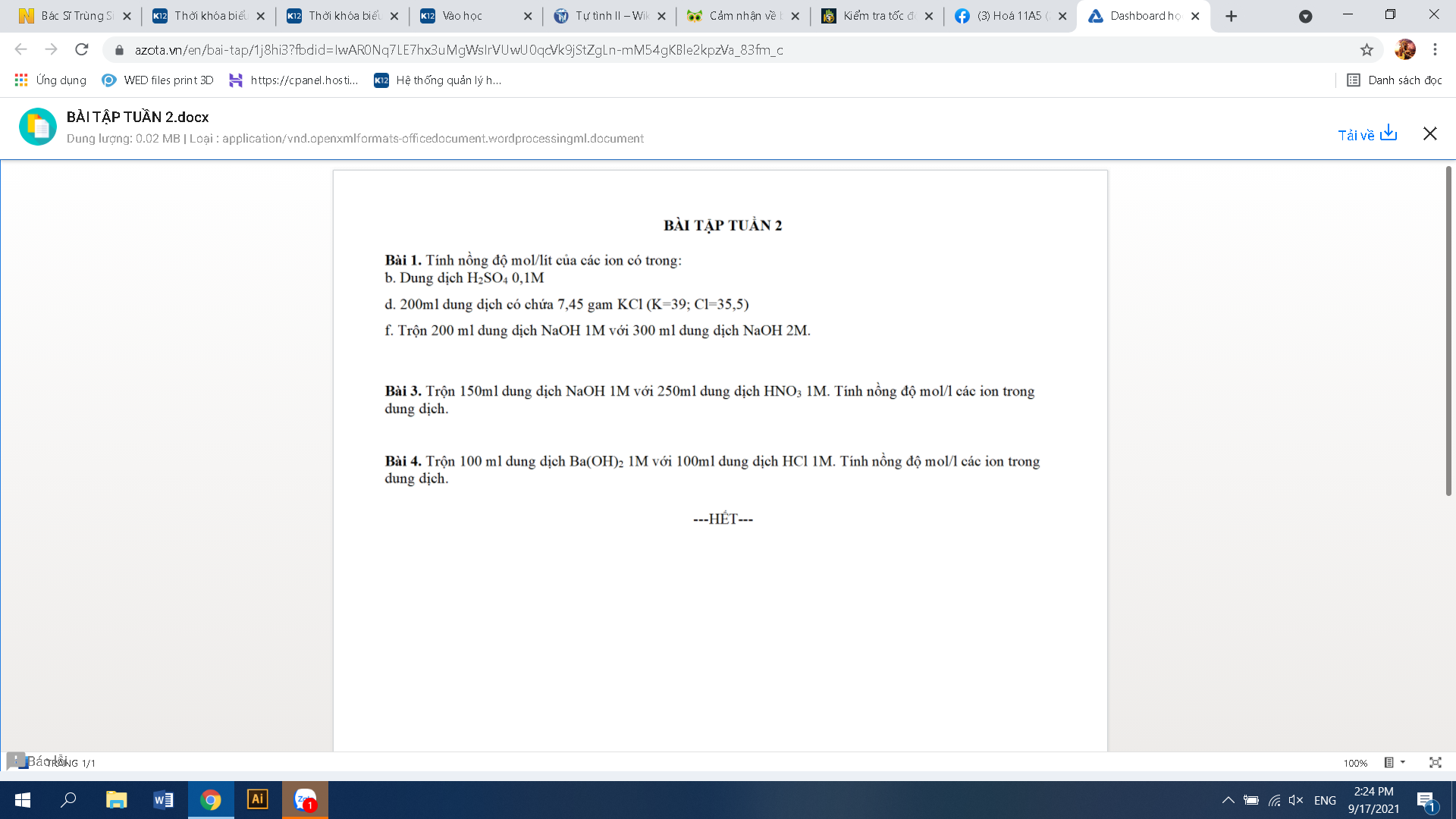
giải giúp em câu 1 2 3 với ạ
Bài 4:
\(n_{Ba\left(OH\right)_2}=1.0,1=0,1\left(mol\right)\\ n_{HCl}=1.0,1=0,1\left(mol\right)\\ Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\\ Vì:\dfrac{0,1}{2}< \dfrac{0,1}{1}\Rightarrow Ba\left(OH\right)_2dư\\ n_{BaCl_2}=n_{Ba\left(OH\right)_2\left(p.ứ\right)}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ n_{Ba\left(OH\right)_2\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\\ \left[OH^-\left(dư\right)\right]=\left[Ba\left(OH\right)_2\left(dư\right)\right]=\dfrac{0,05}{0,1+0,1}=0,25\left(M\right)\\ \left[Cl^-\right]=2.\left[BaCl_2\right]=2.\dfrac{0,05}{0,1+0,2}=0,5\left(M\right)\\ \left[Ba^{2+}\right]=\dfrac{0,25+0,5}{2}=0,375\left(M\right)\)
Đúng 2
Bình luận (0)
Bài 3:
\(n_{NaOH}=1.0,15=0,15\left(mol\right)\\ n_{HNO_3}=1.0,25=0,25\left(mol\right)\\ NaOH+HNO_3\rightarrow NaNO_3+H_2O\\ Vì:\dfrac{0,25}{1}>\dfrac{0,15}{1}\Rightarrow HNO_3dư\\ n_{HNO_3\left(dư\right)}=0,25-0,15=0,1\left(mol\right)\\ n_{NaNO_3}=n_{NaOH}=0,15\left(mol\right)\\ \left[OH^-\right]=\left[Na^+\right]=\left[NaOH\right]=\dfrac{0,15}{0,25+0,15}=0,375\left(M\right)\\ \left[NO^-_3\left(dư\right)\right]=\left[H^+\left(dư\right)\right]\left[HNO_3\left(dư\right)\right]=\dfrac{0,1}{0,15+0,25}=0,25\left(M\right)\)
Đúng 1
Bình luận (1)
Xem thêm câu trả lời

















