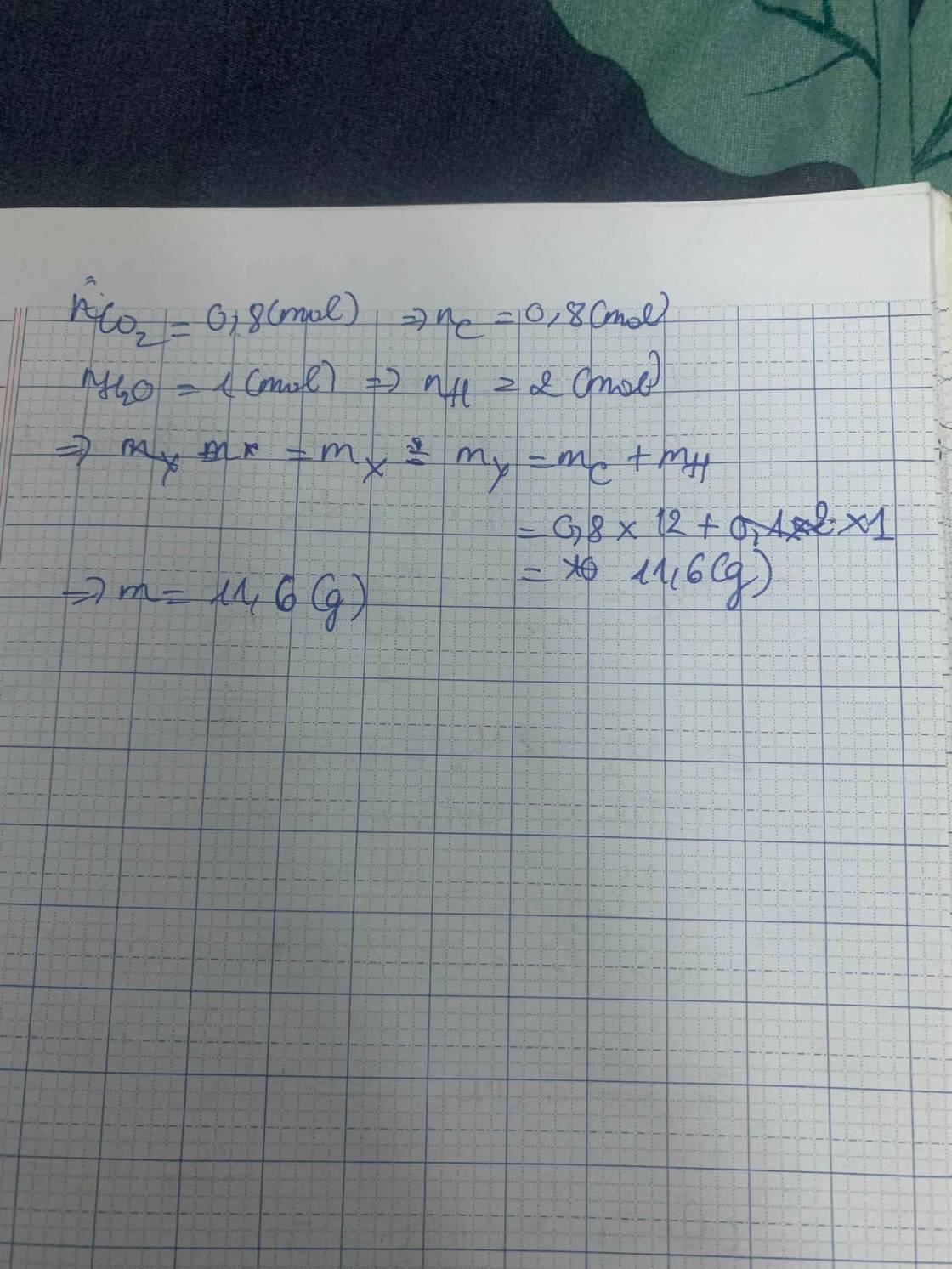Khi đốt cháy 1 lít hidrocacbon cần 6 lít O2 và sinh ra 4 lít CO2 . Xác định CTPT hidrocacbon . Bt các khí đo cùng điều kiện
Bài 20: Mở đầu về hóa học hữu cơ
Vì tỉ lệ thể tích cũng là tỉ lệ mol nên giả sử có: \(\left\{{}\begin{matrix}n_{hiđrocacbon}=1\left(mol\right)\\n_{O_2}=6\left(mol\right)\\n_{CO_2}=4\left(mol\right)\end{matrix}\right.\)
BTNT O: \(n_{H_2O}=2n_{O_2}-2n_{CO_2}=4\left(mol\right)\)
BTNT C: \(n_{CO_2}=n_C=4\left(mol\right)\)
BTNT H: \(n_H=2n_{H_2O}=8\left(mol\right)\)
=> CTPT là `C_4H_8`
Đúng 3
Bình luận (0)
Vì tỉ lệ thể tích cũng là tỉ lệ mol nên giả sử có:
BTNT O:
BTNT C:
BTNT H:
Đúng 0
Bình luận (0)
đốt cháy 200ml hơi 1 hợp chất hữu cơ X chứa C, H , O trong 900ml O2 , thể tích hỗn hợp khí thu đc là 1,3 lít . Sau khi ngưng tụ hơi nc chỉ còn 700ml . Tiếp theo cho qua dd KOH dư chỉ còn 100ml khí bay ra . Các thể tích khí đo ở cùng điều kiện nhiệt độ , áp suất . CTPT của Y là
100ml khí bay ra là O2
=> VO2 (phản ứng) = 900 - 100 = 800 (ml)
VH2O = 1300 - 700 = 600 (ml)
VCO2 = 700 - 100 = 600 (ml)
=> \(V_X:V_{O_2}:V_{CO_2}:V_{H_2O}=200:800:600:600=1:4:3:3\)
Vì tỉ lệ thể tích cũng là tỉ lệ mol nên ta giả sử có: \(\left\{{}\begin{matrix}n_X=1\left(mol\right)\\n_{O_2\left(pư\right)}=4\left(mol\right)\\n_{H_2O}=3\left(mol\right)\\n_{CO_2}=3\left(mol\right)\end{matrix}\right.\)
Theo BTNT: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=3\left(mol\right)\\n_H=2n_{H_2O}=6\left(mol\right)\\n_{O\left(X\right)}=2n_{CO_2}+n_{H_2O}-2n_{O_2}=1\left(mol\right)\end{matrix}\right.\)
=> X là `C_3H_6O`
Đúng 2
Bình luận (0)
1 hợp chất hữu cơ Y khi đốt cháy thu đc CO2 và H2O có số mol bằng nhau , đồng thời lg oxi cần dùng bằng 4 lần số mol Y . Công thức phân tử của Y là
Coi $n_{CO_2} = n_{H_2O} = 1(mol)$
$\Rightarrow n_C = n_{CO_2} = 1(mol) ; n_H = 2n_{H_2O} = 2(mol)$
Ta thấy :
$n_C : n_H = 1 : 2 $
Do đó, số nguyên tử H gấp 2 lần số nguyên tử C.
Gọi CTPT của Y là $C_nH_{2n}O_z$
Ta có :
\(C_nH_{2n}O_z+\dfrac{3n-z}{2}O_2\xrightarrow[]{t^o}nCO_2+nH_2O\)
Ta có :
$\dfrac{3n-z}{2} = 4 \Rightarrow 3n - z = 8$
Với z = 1 thì n = 3. Suy ra CTPT của Y là $C_3H_6O$
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 7,6g 1 chất hữu cơ A chỉ thu đc 7,2g nước và CO2 . Dẫn khí CO2 sinh ra vào dd nc vôi trong thì đc 20g kết tủa , nhỏ dd NaOH 1M vào dd thu đc kết tủa lớn nhất cần tối thiểu 50ml .Tìm công thức phân tử của A
$n_{CaCO_3} =\dfrac{20}{100} = 0,2(mol)$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$2CO_2 + Ca(OH)_2 \to Ca(HCO_3)_2$
$Ca(HCO_3)_2 + NaOH \to NaHCO_3 + CaCO_3 + H_2O$
$n_{Ca(HCO_3)_2} = n_{NaOH} = 0,05.1 = 0,05(mol)$
$n_{CO_2} = 2n_{Ca(HCO_3)_2} + n_{CaCO_3} = 0,05.2 + 0,2 = 0,3(mol)$
$n_{H_2O} = \dfrac{7,2}{18} = 0,4(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,3(mol)$
$n_H = 2n_{H_2O} = 0,8(mol)$
$\Rightarrow n_O = \dfrac{7,6 - 0,3.12 - 0,8}{16} = 0,2(mol)$
Ta có :
$n_C : n_H : n_O = 0,3 : 0,8 :0,2 = 3 : 8 : 2$
Vậy A có CT là $C_3H_8O_2$
Đúng 2
Bình luận (0)
\(n_H=2n_{H_2O}=2.\dfrac{7,2}{18}=0,8\left(mol\right)\)
\(n_{NaOH}=0,05.1=0,05\left(mol\right)\)
PTHH:
`Ca(OH)_2 + CO_2 -> CaCO_3 + H_2O` (1)
`Ca(OH)_2 + 2CO_2 -> Ca(HCO_3)_2` (2)
`Ca(HCO_3)_2 + NaOH -> CaCO_3 + NaHCO_3 + H_2O` (3)
Theo (3): \(n_{Ca\left(HCO_3\right)_2}=n_{NaOH}=0,05\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
BTNT C: \(n_C=n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=0,3\left(mol\right)\)
=> \(n_{O\left(A\right)}=\dfrac{7,6-0,8-0,3.12}{16}=0,2\left(mol\right)\)
Xét \(n_C:n_H:n_O=0,3:0,8:0,2=3:8:2\)
=> CTĐGN của A là `C_3H_8O_2`
Đúng 1
Bình luận (0)
Oxi hóa hoàn toàn 18g chất hữu cơ chứa (C,H,O) , sản phẩm sinh ra lần lượt đi qua 132g dd H2SO4 98% và bình đựng dd Ba(OH)2 . Sau thí nghiệm dd H2SO4 còn lại 90,588% ở dd Ba(OH)2 tạo ra 78,8g kết tủa và dd còn lại đc nung nóng đc thêm 19,7g kết tủa nx . Tìm CTPT của A , bt 4,5g A khi hóa hơi có thể tích của 1,6g oxi do cùng điều kiện .
$m_{H_2SO_4} = 132.98\% = 129,36(gam)$
Gọi $n_{H_2O} = a(mol)$
$C\%_{H_2SO_4} = \dfrac{129,36}{132 + 18a}.100\% = 90,588\%$
$\Rightarrow a = 0,6(mol)$
$CO_2 + Ba(OH)_2 \to BaCO_3 + H_2O(1)$
$2CO_2 + Ba(OH)_2 \to Ba(HCO_3)_2(2)$
$Ba(HCO_3)_2 \xrightarrow{t^o} BaCO_3 + CO_2 + H_2O(2)$
$n_{Ba(HCO_3)_2} = n_{BaCO_3(2)} = \dfrac{19,7}{197} = 0,1(mol)$
$n_{CO_2} = n_{BaCO_3(1)} + 2n_{Ba(HCO_3)_2} = 0,6(mol)$
Ta có :
$n_C = n_{CO_2} = 0,6(mol)$
$n_H = 2n_{H_2O} = 1,2(mol)$
$n_O = \dfrac{18 - 0,6.12 - 1,2}{16} = 0,6(mol)$
Ta có : $n_C : n_H : n_O = 0,6 : 1,2 : 0,6 = 1 : 2 : 1$
Vậy A có dạng : $(CH_2O)_n$
$n_A = \dfrac{1,6}{32} = 0,05(mol) \Rightarrow M_A = \dfrac{4,5}{0,05} = 90(g/mol)$
$M_A = (12 + 2 + 16)n = 90 \Rightarrow n = 3$
Vậy CTPT của A là $C_3H_6O_3$
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 3,81g chất hữu cơ X thu đc hh khí gồm CO2, H2O và HCl . Dẫn hh này qua bình chứa dd agno3/hno3 ở nhiệt độ thấp thấy có 2,87 g kết tủa và bình chứa tăng 2,17g . Cho bt chỉ có H2O và HCl bị hấp thụ . Dẫn khí thoát ra vào 100ml dd ba(oh)2 1M thu đc 15,76g kết tủa Y , lọc bỏ Y , lấy dd đem sôi lại có kết tủa nx. Lập CTPT của X bt khối lg phân tử của X<200
Sửa $3,81 \to 3,61$
$AgNO_3 + HCl \to AgCl +HNO_3$
$n_{HCl} = n_{AgCl} = \dfrac{2,87}{143,5} = 0,02(mol)$
$n_{H_2O} = \dfrac{2,17 - 0,02.36,5}{18} = 0,08(mol)$
$n_{Ba(OH)_2} = 0,1.1 = 0,1(mol) ; n_{BaCO_3} = 0,08(mol)$
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O$
$Ba(OH)_2 + 2CO_2 \to Ba(HCO_3)_2$
$n_{Ba(HCO_3)_2} = n_{Ba(OH)_2} - n_{BaCO_3} = 0,02(mol)$
$n_{CO_2} = 2n_{Ba(HCO_3)_2} + n_{BaCO_3} = 0,12(mol)$
Bảo toàn nguyên tố :
$n_C = n_{CO_2} = 0,12(mol)$
$n_H = 2n_{H_2O} +n_{HCl}= 0,18(mol)$
$n_{Cl} = n_{HCl} = 0,02(mol)$
$\Rightarrow n_O = \dfrac{3,61 - 0,12.12 - 0,18.1 - 0,02.35,5}{16} = 0,08(mol)$
Ta có : $n_C : n_H: n_O : n_{Cl} = 0,12 : 0,18 : 0,08 : 0,02 = 6 : 9 : 4 : 1$
Vậy CTPT của X là $(C_6H_9O_4Cl)_n$
$M_X = (12.6 + 9 + 16.4 + 35,5)n < 200 \Rightarrow n < 1,1$
$\Rightarrow n = 1$
Vậy X là $C_6H_9O_4Cl$
Đúng 2
Bình luận (0)
Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào 200 ml dd KOH 1M và NaOH 1,5M , thu đc dd X . Tìm m chất tan trong dd X là
$n_{KOH} = 0,2(mol) ; n_{NaOH} = 0,3(mol)$
$n_{CO_2} = 0,15(mol)$
Dung dịch X gồm :
$K^+ : 0,2(mol)$
$Na^+ : 0,3(mol)$
$OH^-: x(mol)$
$CO_3^{2-} : y(mol)$
Bảo toàn điện tích :$x + 2y = 0,2 + 0,3$
Bảo toàn nguyên tố với C : $ y = n_{CO_2} = 0,15$
Suy ra x = 0,2 ; y = 0,15
$\Rightarrow m_X = 0,2.39 + 0,3.23 + 0,2.17 + 0,15.60 = 27,1(gam)$
Đúng 2
Bình luận (0)
Nhỏ từ từ từng giọt đến hết 25ml dd HCl 1,2M vào 100ml dd chứa K2CO3 0,2M và KHCO3 0,2M sau phản ứng thu đc số mol CO2 là
$n_{K_2CO_3} = 0,02(mol) ; n_{KHCO_3} = 0,02(mol)$
Vì $K_2CO_3,KHCO_3$ phản ứng đồng thời với dung dịch $HCl$
nên ta gọi : $n_{K_2CO_3\ pư} = 0,02a(mol) ; n_{KHCO_3\ pư} = 0,02a(mol)$
$K_2CO_3 + 2HCl \to 2KCl + CO_2 + H_2O$
$KHCO_3 + HCl \to KCl + CO_2 + H_2O$
$n_{HCl} = 2n_{K_2CO_3} + n_{KHCO_3} = 0,02a.2 + 0,02a = 0,025.1,2$
Suy ra : a = 0,5
$n_{CO_2} = n_{K_2CO_3} + n_{KHCO_3} = 0,04a = 0,02(mol)$
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 1,16g Y cần dùng 2,912 lít O2 (đktc) . Xác định CTPT của ankan
Gọi CTPT của ankan là \(C_nH_{2n+2}\)
Ta có: \(\left\{{}\begin{matrix}n_{ankanY}=\dfrac{1,16}{14n+2}\left(mol\right)\\n_{O_2}=\dfrac{2,912}{22,4}=0,13\left(mol\right)\end{matrix}\right.\)
PTHH: \(2C_nH_{2n+2}+\left(3n+1\right)O_2\xrightarrow[]{t^o}2nCO_2+\left(2n+2\right)H_2O\)
Theo PT: \(\dfrac{n_{O_2}}{n_{C_nH_{2n+2}}}=\dfrac{3n+1}{2}\)
=> \(\dfrac{0,13}{\dfrac{1,16}{14n+2}}=\dfrac{3n+1}{2}\)
=> \(n=4\)
Vậy CTPT của ankan Y là C4H10
Đúng 1
Bình luận (0)
Crackinh m (g) C4H10 thu đc hh Y . Đốt cháy hoàn toàn Y thu đc 17,92 lít CO2 và 18g H2O . Giá trị m là ???