HCl phân ly mạnh, acetic acid phân ly yếu.
Bài 2. Cân bằng trong dung dịch nước
Đúng 1
Bình luận (0)
Các câu hỏi tương tự
Viết phương trình hóa học của phản ứng xảy ra trong thí nghiệm chuẩn độ dung dịch NaOH bằng dung dịch HCl.
Viết phương trình điện li (nếu có) của các chất sau khi hoà tan vào nước: HNO3, Ca(OH)2 và BaCl2.
Nhận xét về vai trò acid - base của phân tử H2O trong các cân bằng ở Hình 2.4, Hình 2.5 và cân bằng của ion HCO3-, trong nước.

Viết phương trình điện li của các chất: H2SO4, Ba(OH)2, Al2(SO4)3.
Hãy nêu vai trò của chất chỉ thị trong phương pháp chuẩn độ acid-base.
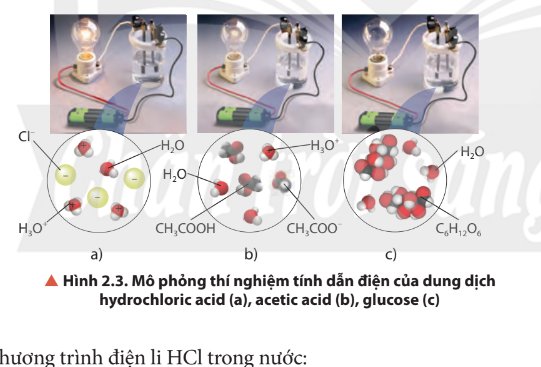
Quan sát Hình 2.3, nhận xét về độ sáng của bóng đèn ở các thí nghiệm. Biết rằng nồng độ mol của các dung dịch là bằng nhau, cho biết dung dịch nào dẫn điện mạnh, dẫn điện yếu và không dẫn điện.
a) Pha 500 mL dung dịch HCl 0,2 M vào 500 mL nước. Tính pH của dung dịch thu được.
b) Tính khối lượng NaOH cần để pha 100 mL dung dịch NaOH có pH = 12.
Khi mưa nhiều ngày liên tục có thể làm cho pH của nước ở ao, hồ giảm xuống dưới 6,5 và người ta thường rắc vôi bột để điều chỉnh pH. Giải thích.
Giải thích vì sao quá trình thuỷ phân ion CO32- trong nước làm tăng pH của nước.




