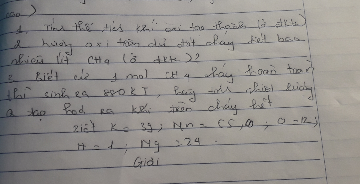Câu 1: Đốt cháy 3,36 lít khí metan trong bình kín có chứa 2,24 lít khí O2 ở đktc.
-Chất nào dư? Dư bao nhiêu gam?
-Chất nào tạo thành? Khối lượng mỗi chất là bao nhiêu gam?
Câu 2:Đốt cháy 22,4 gam Fe trong bình kín có chứa 2,24 lít khí O2 ở đktc. Chất nào dư? Dư bao nhiêu gam? Chất nào tạo thành? Khối lượng là bao nhiêu gam?
C1:
-Số mol CH4 : n\(CH_4\) = 3,36 : 22,4 =0,15 (mol)
-Số mol O2 : n\(O_2\) = 2,24 : 22,4 = 0,1 (mol)
-PTH2 : CH4 + 2O2 \(\underrightarrow{t^o}\) CO2 + 2H2O
Xét : \(\frac{0,15}{1}>\frac{0,1}{2}\)
=> CH4 dư
-theo PTH2 : nCH4<pứ> = \(\frac{1}{2}n_{O_2}=\frac{1}{2}.0,1=0,05\left(mol\right)\)
=> nCH4<dư>= 0,15 - 0,05 = 0,1 (mol)
=> mCH4<dư> = 0,1 . 16 = 1,6 (g)
- Chất tạo thành : CO2 và H2O
- theo PTH2 : nCO2 = \(\frac{1}{2}n_{O_2}=0,05\left(mol\right)\)
=> mCO2 = 0,05 . 44 = 2,2 (g)
-theo PTH2 : nH2O = nO2 = 0,1 (mol)
=> mH2O = 0,1 . 18 = 1,8 (g)
C2 :
-Số mol Fe : nFe = 22,4 : 56 = 0,4 (mol)
-Số mol O2 : nO2 = 2,24 : 22,4 = 0,1 (mol)
PTH2 : 4Fe + 3O2 \(\underrightarrow{t^o}\) 2Fe2O3
Xét : \(\frac{0,4}{4}>\frac{0,1}{3}\)
=> Fe dư
- theo PTH2 : nFe<pứ> = \(\frac{3}{4}n_{O_2}=\frac{3}{4}.0,1=0,075\left(mol\right)\)
=> nFe<dư>= 0,4 - 0,075 = 0,325 (mol)
=> mFe<dư> = 0,325 . 56 = 18,2 (g)
- Chất tạo thành là Fe2O3
- theo PTH2 : n\(Fe_2O_3=\frac{2}{3}.n_{O_2}=\frac{2}{3}.0,1=0,67\left(mol\right)\)
=>mFe2O3 = 0,67 . 160 = 107,2 (g)
Câu 1
CH4+2O2-->2H2O+CO2
Ta có
n CH4=3,36/22,4=0,15(mol)
n O2=2,24/22,4=0,1(mol)
--> CH4 dư
Theo pthh
n CH4=1/2n O2=0,05(mol)
n CH4 dư=0,15-0,05=0,1(mol)
m CH4 dư=0,1.18=1,8(g)
Chất tạo thành là H2O và CO2
Theo pthh
n H2O=n O2=0,1(mol)
m H2O=0,1.18=1,8(g)
n CO2=1/2n O2=0,05(mol)
m CO2=0,05.44=22(g)
Câu 2
3Fe+2O2--->Fe3O4
Ta có
n Fe=22,4/56=0,4(mol)
n O2=2,24/22,4=0,1(mol)
-->Fe dư
Theo pthh
n Fe=3/2n O2=0,15(mol)
n Fe dư=0,4-0,15=0,25(mol)
m Fe dư=0,25.56=14(g)
Chất tạo thành là Fe3O4
n Fe3O4=1/2 n O2=0,05(mol)
m Fe3O4=232.0,05=11,6(g)