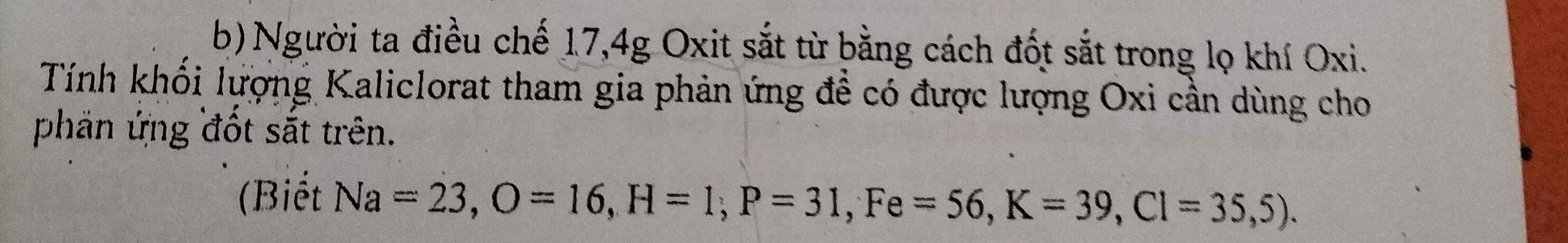b) \(n_{Fe_3O_4}=\dfrac{17,4}{232}=0,075\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,1<-----------------0,15
3Fe + 2O2 --to--> Fe3O4
0,15<-----0,075
=> mKClO3 = 0,1.122,5 = 12,25 (g)
\(n_{Fe_3O_4}=\dfrac{17,4}{232}=0,075mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,15 0,075 ( mol )
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
0,1 0,15 ( mol )
\(m_{KClO_3}=0,1.122,5=12,25g\)
3Fe+2O2-to>Fe3O4
0,15-------0,075
2KClO3-to>2KCl+3O2
0,1-------------------------0,15
n Fe3O4=0,075 mol
=>m KClO3=0,1.122,5=12,25g
\(n_{Fe_3O_4}=\dfrac{17,4}{232}=0,075\left(mol\right)\\
pthh:3Fe+2O_2\rightarrow Fe_3O_4\)
0,15 0,075
\(2KClO_3\xrightarrow[xtMnO_2]{t^o}2KCl+3O_2\)
0,1 0,15
\(m_{KClO_3}=0,1.122,5=12,25g\)