Học tại trường
Chưa có thông tin
Đến từ
Phú Yên , Chưa có thông tin
Số lượng câu hỏi
11
Số lượng câu trả lời
953
Điểm GP
335
Điểm SP
1032














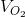 = 2 . 2 = 4 lít
= 2 . 2 = 4 lít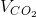 = 0,15 . 22,4 = 3,36 lít
= 0,15 . 22,4 = 3,36 lít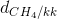 =
= 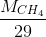 =
= 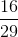 ≈ 0,55
≈ 0,55