Khí metan CH4 có trong khí tự nhiên hoặc trong khí bioga. Khí metan cháy trong không khí sinh ra khí cacbon đioxit và nước:
CH4 + 2O2 CO2 + 2H2O
a) Tính thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2lít khí metan. Các thể tích khí đo cùng điều kiện t0 và p
b) Tính thể tích khí CO2 (đktc) thu được sau khi đốt cháy hoàn toàn 0,15 mol khí metan.
c) Khí metan nặng hay nhẹ hơn không khí bằng bao nhiêu lần ?
\(PTHH: \) \(CH_4+2O_2-t^o->CO_2+2H_2O\)
\(nCH_4(đktc)=\dfrac{5}{56}(mol)\)
Theo PTHH: \(nO_2=2.nCH_4=\dfrac{5}{28}\left(mol\right)\)
Thể tích Oxi cần dùng để đốt cháy hết \(2(l)CH_4\)trên là:
\(VO_2(đktc)=nO_2.22,4=\dfrac{5}{28}.22,4=4(l)\)
\(b)\)
Khi đốt cháy hoàn toàn 0,15 mol CH4 thì:
\(nCH_4=0,15(mol)\)
Theo PTHH: \(nCO_2=nCH_4=0,15(mol)\)
Thể tích khí CO2 thu được là:
\(V_{CO_2}\left(đktc\right)=n_{CO_2}.22,4=0,15.22,4=3,36\left(l\right)\)
\(c)\)
Ta có: \(dCH_4/kk\)\(=\dfrac{M_{CH_4}}{29}=\dfrac{16}{29}\approx0,552\)
Vậy khí CH4 nhẹ hơn không khí 0,552 lần.
Bài giải:
a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2 . Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
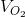 = 2 . 2 = 4 lít
= 2 . 2 = 4 lít
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
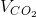 = 0,15 . 22,4 = 3,36 lít
= 0,15 . 22,4 = 3,36 lít
c) Tỉ khối của khí metan và không khí là:
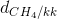 =
= 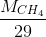 =
= 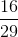 ≈ 0,55
≈ 0,55
Vậy khí metan nhẹ hơn không khí 0,55
PTHH: CH4 + 2O2 -> CO2 + 2H2O
a) Theo pt ta có: 1VCH4 cần dùng 2VO2->2 lít CH4 cần dùng 4 lít O2
b)Theo pt ta có: cần dùng 1VCH4 để có 1VCO2-> khi đốt cháy hoàn toàn 0,15 mol CH4 thì ta được 0,15 mol CO2
->VCO2= 0,15×22,4=3,36(l)
c) Thể tích khí metan nặng hơn không khí số lần là:
dkk/CH4= 29÷16=1,825(lần)
a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2 . Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
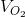 = 2 . 2 = 4 lít
= 2 . 2 = 4 lít
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
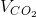 = 0,15 . 22,4 = 3,36 lít
= 0,15 . 22,4 = 3,36 lít
c) Tỉ khối của khí metan và không khí là:
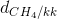 =
= 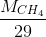 =
= 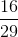 ≈ 0,55
≈ 0,55
Vậy khí metan nhẹ hơn không khí 0,55
a) PTHH:PTHH: CH4+2O2−to−>CO2+2H2OCH4+2O2−to−>CO2+2H2O
nCH4(đktc)=556(mol)nCH4(đktc)=556(mol)
Theo PTHH: nO2=2.nCH4=528(mol)nO2=2.nCH4=528(mol)
Thể tích Oxi cần dùng để đốt cháy hết 2(l)CH42(l)CH4trên là:
VO2(đktc)=nO2.22,4=528.22,4=4(l)VO2(đktc)=nO2.22,4=528.22,4=4(l)
b)b)
Khi đốt cháy hoàn toàn 0,15 mol CH4 thì:
nCH4=0,15(mol)nCH4=0,15(mol)
Theo PTHH: nCO2=nCH4=0,15(mol)nCO2=nCH4=0,15(mol)
Thể tích khí CO2 thu được là:
VCO2(đktc)=nCO2.22,4=0,15.22,4=3,36(l)VCO2(đktc)=nCO2.22,4=0,15.22,4=3,36(l)
c)c)
Ta có: dCH4/kkdCH4/kk=MCH429=1629≈0,552=MCH429=1629≈0,552
Vậy khí CH4 nhẹ hơn không khí 0,552 lần.













