Bài 45: Bài thực hành 7
Nội dung lý thuyết
Các phiên bản khácI. PHA CHẾ DUNG DỊCH
Tính toán và pha chế các dung dịch sau:
1. 50 g dung dịch đường có nồng độ 15%.
2. 100 ml dung dịch natri clorua có nồng độ 0,2M.
3. 50 g dung dịch đường 5% từ dung dịch đường có nồng độ 15% trở lên.
4. 50 ml dung dịch natri clorua có nồng độ 0,1M từ dung dịch natri clorua có nồng độ 0,2M ở trên.
1. Thực hành 1: Pha chế 50 g dung dịch đường có nồng độ 15%
| Phần tính toán | Phần thực hành |
mct = \(\dfrac{15.50}{100}\) = 7,5 (g)
50 - 7,5 = 42,5 (g) | Cân 7,5 g đường khan cho vào cốc có dung tích 100 ml, khuấy đều với 42,5 g nước, thu được 50 g dung dịch đường 15 %. |
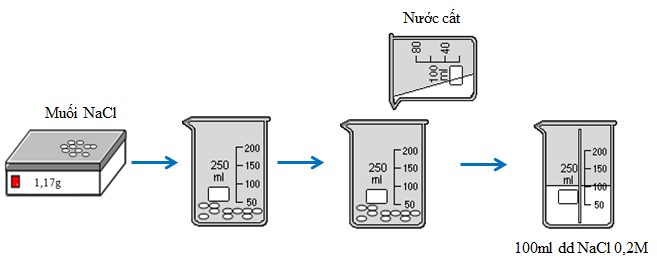
2. Thực hành 2: Tính toán và pha chế 100 ml dung dịch natri clorua có nồng độ 0,2M
| Phần tính toán | Phần thực hành |
nNaCl = \(\dfrac{0,2.100}{1000}\) = 0,02 (mol)
<=> mNaCl = 0,02 . 58,5 = 1,17 (g)
| Cân 1,17g NaCl khan cho vào cốc chia độ. Rót từ từ nước vào cốc và khuấy đều cho đến vạch 100ml, được 100ml dung dịch NaCl 0,2M. |
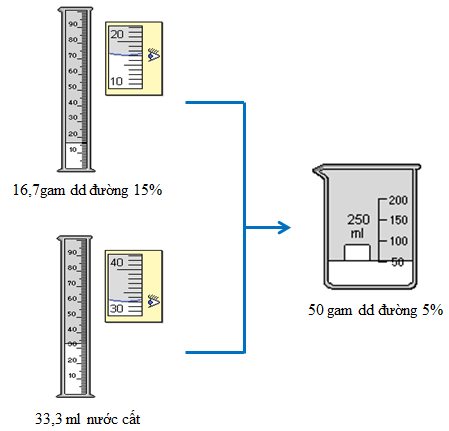
3. Thực hành 3: Tính toán và pha chế 50 g dung dịch đường 5% từ dung dịch đường có nồng độ 15% trở lên
| Phần tính toán | Phần thực hành |
mct = \(\dfrac{5.50}{100}\) = 2,5 gam
mdd = \(\dfrac{100.2,5}{15}\) ≃ 16,7 (g)
50 - 16,7 = 33,3 (g) | Cân 16,7 g dung dịch đường 15% cho vào cốc có dung tích 100ml. Thêm 33,3 g (hoặc 33,3ml) nước vào cốc, khuấy đều, được 50 g dung dịch đường 5%. |
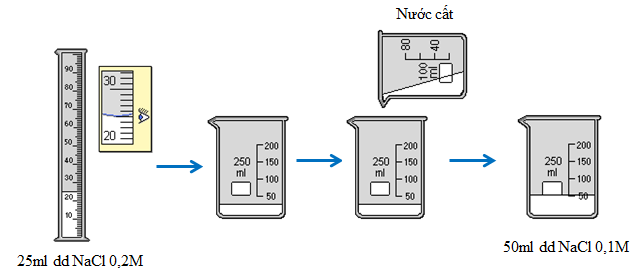
4. Thực hành 1: Pha chế 50 ml dung dịch natri clorua có nồng độ 0,1M từ dung dịch natri clorua có nồng độ 0,2M ở trên
| Phần tính toán | Phần thực hành |
mNaCl = \(\dfrac{0,1.50}{1000}\) = 0,005 (mol)
Vdd = \(\dfrac{1000.0,005}{0,2}\) = 25 (ml) | Đong 25 ml dung dịch NaCl 0,2M cho vào cốc chia độ. Rót từ từ nước vào đến vạch 50ml. Khuấy đều, được 50ml dung dịch NaCl 0,1M. |
II. TƯỜNG TRÌNH
| Thí nghiệm | Tính toán | Cách tiến hành |
Pha chế 50 g dung dịch đường có nồng độ 15% | Khối lượng chất tan (đường) cần dùng: 7,5 gam Khối lượng nước cần dùng: 42,5 gam | Cân 7,5 g đường khan cho vào cốc có dung tích 100 ml, khuấy đều với 42,5 g nước, thu được 50 g dung dịch đường 15 %. |
Tính toán và pha chế 100 ml dung dịch natri clorua có nồng độ 0,2M | Số mol chất tan (NaCl) cần dùng là 0,02 mol. Khối lượng chất tan (NaCl) cần dùng là 1,17 (g). | Cân 1,17g NaCl khan cho vào cốc chia độ. Rót từ từ nước vào cốc và khuấy đều cho đến vạch 100ml, được 100ml dung dịch NaCl 0,2M. |
Tính toán và pha chế 50 g dung dịch đường 5% từ dung dịch đường có nồng độ 15% trở lên | Khối lượng chất tan (đường) có trong 50 g dung dịch đường 5% là 2,5 gam. Khối lượng dung dịch đường 15% có chứa 2,5 g đường là 16,7 gam. Khối lượng nước cần dùng là 33,3 gam. | Cân 16,7 g dung dịch đường 15% cho vào cốc có dung tích 100ml. Thêm 33,3 g (hoặc 33,3ml) nước vào cốc, khuấy đều, được 50 g dung dịch đường 5%. |
Pha chế 50 ml dung dịch natri clorua có nồng độ 0,1M từ dung dịch natri clorua có nồng độ 0,2M ở trên | Số mol chất tan (NaCl) có trong 50ml dung dịch 0,1M cần pha chế là 0,005 mol. Thể tích dung dịch NaCl 0,2M trong đó có chứa 0,005 mol NaCl là 25 ml. | Đong 25 ml dung dịch NaCl 0,2M cho vào cốc chia độ. Rót từ từ nước vào đến vạch 50ml. Khuấy đều, được 50ml dung dịch NaCl 0,1M. |
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!