Bài 38. Axetilen
Nội dung lý thuyết
Các phiên bản khácCông thức phân tử: C2H2
Khối lượng phân tử: 26
I. TÍNH CHẤT VẬT LÍ
Axetilen là chất khí, không màu, không mùi, nhẹ hơn không khí (d = \(\dfrac{26}{29}\)), ít tan trong nước.
@90309@@90317@
II. CẤU TẠO PHÂN TỬ
Công thức cấu tạo của axetilen: ![]()
Viết gọn: HC≡CH.
Trong phân tử axetilen có một liên kết ba giữa cacbon với cacbon, trong liên kết đó có 2 liên kết kém bền, dễ bị đứt lần lượt trong phản ứng hóa học.
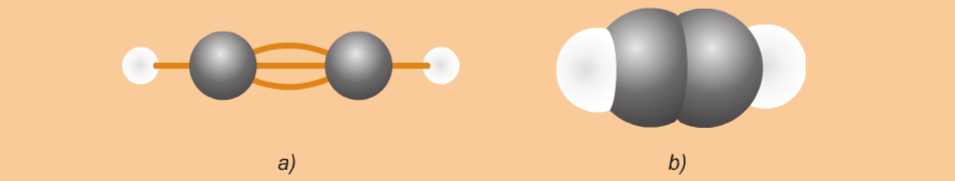
a) Dạng rỗng b) Dạng đặc
@90319@
III. TÍNH CHẤT HÓA HỌC
1. Phản ứng cháy
Tương tự metan và etilen, khi đốt, axetilen cháy tạo khí cacbonic, hơi nước và tỏa nhiệt mạnh.
Phương trình hóa học: 2C2H2 + 5O2 4CO2 + 2H2O
Khi axetilen cháy trong oxi, nhiệt độ ngọn lửa có thể lên đến 3000oC. Vì vậy, axetilen thường được sử dụng làm đèn xì để hàn cắt kim loại. Nhiệt độ lớn làm nóng chảy kim loại giúp quá trình hàn cắt dễ dàng được thực hiện.

2. Tác dụng với dung dịch brom
Trong liên kết ba của phân tử axetilen có 2 liên kết kém bền, dễ bị bẻ gãy. Vì vậy axetilen có thể tham gia phản ứng cộng với dung dịch brom tương tự như etilen.
HC≡CH(k) + Br - Br(dd) → Br-CH2=CH2-Br(L)
(màu cam) (không màu)
Sản phẩm sinh ra có liên kết đôi giống với etilen nên vẫn có thể tiếp tục phản ứng với một phân tử brom nữa.
Br-CH2=CH2-Br(L) + Br2(dd) → Br2CH-CHBr2(L)
.gif)
Trong điều kiện thích hợp, axetilen còn tham gia phản ứng cộng với nhiều chất khác như H2, Cl2...
HC≡CH + H2 \(\underrightarrow{t^o,Pd/PbCO_3}\) CH2=CH2
HC≡CH + 2H2 \(\underrightarrow{t^o,Ni}\) CH3-CH3
IV. ĐIỂU CHẾ , ỨNG DỤNG
1. Điều chế
Trong phòng thí nghiệm và trong công nghiệp axetilen được điều chế bằng cách thủy phân canxi cacbua CaC2 (đất đèn).
Phương trình điều chế: CaC2 + 2H2O → C2H2↑ + Ca(OH)2

Phương pháp hiện đại để điều chế axetilen hiện nay là nhiệt phân metan ở nhiệt độ cao.
2CH4 \(\underrightarrow{1500^oC}\) C2H2↑ + 3H2↑
.gif)
2. Ứng dụng
Trong công nghiệp dùng làm đèn xì oxi - axetilen để hàn cắt kim loại do axetilen cháy sinh ra ngọn lửa có nhiệt độ lớn. Là nguyên liệu để điều chế poli (vinyl clorua) dùng làm nhựa PVC, cao su, axit axetic và nhiều loại hóa chất khác...

V. TỔNG KẾT
1. Axetilen là chất khí, không màu, không mùi, nhẹ hơn không khí, ít tan trong nước.
2. Công thức cấu tạo của axetilen là CH\(\equiv\)CH.
3. Axetilen có tính chất hóa học sau: tham gia phản ứng cháy, phản ứng cộng.
4. Axetilen là nguyên liệu, nhiên liệu trong công nghiệp.
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
Danh sách các phiên bản khác của bài học này. Xem hướng dẫn
| ❤ ~~ Yến ~~ ❤ đã đóng góp một phiên bản khác cho bài học này (1 tháng 4 2021 lúc 18:18) | 1 lượt thích |