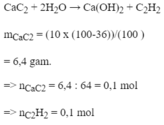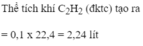tính thể tích khí \(C_2H_2\) (đktc) tạo ra khí cho 10 gam CaC\(_2\) (có 36% tạp chất ) tác dụng hết với H\(_2O\) (cho C=12, Ca=14)

Những câu hỏi liên quan
Tính thể tích khí C 2 H 2 (đktc) tạo ra khi cho 10 gam C a C 2 (có 36% tạp chất) tác dụng hết với H2O (cho C=12, Ca=14)
1.Tính thể tích khí ch4 tạo ra khi cho 14,4g al4c3 (có 30% tạp chất) tác dụng hết với h20.
2.một hỗn hợp gồm so2 và c2h4 có thể tích 5,6 lít khí (đktc) cho qua dung dịch br2 dư dung dịch này nặng thêm 12.4 g.tính thể tích mỗi khí trong hỗn hợp ban đầu
Xem chi tiết
1.
Al4C3 + 12H2O -> 4Al(OH)3 + 3CH4
khối lượng Al4C3 thực là 14,4 - 30%.14,4 = 10,08(g)
nAl4C3 = 0,07 (mol) -> nCH4 = 0,21 (mol)
-> VCH4 = 0,21 . 22,4 = 4,704 (l)
2. Gọi x, y lần lượt là số mol của C2H2 và C2H4 trong 5,6 lít hỗn hợp.
C2H2 + 2Br2 → C2H2Br4
x
C2H4 + Br2 → C2H2Br2
y
Ta có: x + y = 5,6/22,4 = 0,25
dd Br2 nặng thêm = mC2H2 + mC2H2 = 26x + 28y = 6,8
-> x = 0,1 mol; y = 0,15 mol
Vậy: VC2H2 = 0,1.22,4 = 2,24 (l)
VC2H2 = 0,15. 22,4 = 3,36 (l)
Đúng 1
Bình luận (0)
Cho 43,2 gam bột Al tác dụng vừa đủ với dung dịch HCl, sinh ra muối nhôm clorua và khí Hidro.
a. Tính thể tích khí H\(_2\) sinh ra sau phản ứng (ĐKTC)?
b. Dẫn toàn bộ lượng khí H\(_2\) thu được ở trên cho qua bình đựng 64 g CuO nung nóng thu được m gam chất rắn. Tìm m.
a) nAl = 43,2/27 = 1,6 mol
2Al + 6HCl → 2AlCl3 + 3H2
1,6 \(\dfrac{1,6\times3}{2}=2,4\)
→ nH2 = 2,4 mol → VH2 = 2,4 x 22, 4 = 53,76 lít
b) nCuO = 64/80 = 0,8 mol
nH2 = 2,4 mol
→ H2 dư, phương trình tính theo số mol của CuO
CuO + H2 → Cu + H2O
0,8 0,8 0,8 0,8
Chất rắn sau phản ứng có Cu
mCu = 0,8 x 64 = 51,2 gam
Đúng 3
Bình luận (0)
Cho 12 gam kim loại magie Mg tác dụng hết với dung dịch axit clohidric HCl
a. Lập PTHH. Tính tích thể hiđro tạo ra ( đktc )
b. Tính khối lượng HCl đã dùng.
c. Cho toàn bộ hidro sinh ra ở phản ứng trên tác dụng với 6,72 lít khí oxi (đktc).Tính khối lượng nước thu được.
a. \(PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
\(n_{Mg}=\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{12}{24}=0,5\left(mol\right)\)
- Mol theo PTHH : \(1:2:1:1\)
- Mol theo phản ứng : \(0,5\rightarrow1\rightarrow0,5\rightarrow0,5\)
\(\Rightarrow n_{H_2}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2}=n_{H_2}.22,4=0,5.22,4=11,2\left(l\right)\)
b. Từ a. \(\Rightarrow n_{HCl}=1\left(mol\right)\)
\(\Rightarrow m_{HCl}=n_{HCl}.M_{HCl}=1.\left(1+35,5\right)=36,5\left(g\right)\)
c. \(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(PTHH:2H_2+O_2\underrightarrow{t^o}2H_2O\)
- Mol theo PTHH : \(2:1:2\)
- Mol theo phản ứng : \(0,6\leftarrow0,3\rightarrow0,6\)
\(\Rightarrow n_{H_2O}=0,6\left(mol\right)\)
\(\Rightarrow m_{H_2O}=n_{H_2O}.M_{H_2O}=0,6.\left(2+16\right)=10,8\left(g\right)\)
Đúng 3
Bình luận (1)
Cho 2,7g nhôm tác dụng với dung dịch chứa 14,6g HCl.
a. Tính khối lượng muối tạo thành sau phản ứng?
b. Tính thể tích hiđro thu được (đktc)?
c. Nếu dùng thể tích khí hidro trên để khử 38,4g sắt (III) oxit có lẫn 20% tạp chất thì thu được bao nhiêu gam sắt?
a) nAl=2,7/27=0,1(mol)
nHCl=14,6/36,5= 0,4(mol)
PTHH: 2Al +6 HCl -> 2 AlCl3 +3 H2
Ta có: 0,1/2 < 0,6/4
=> HCl dư, Al hết, tính theo nAl
=> nAlCl3=nAl=0,1(mol)
=> mAlCl3=0,1.133,5=13,35(g)
b) nH2= 3/2. nAl=3/2. 0,1=0,15(mol)
=>V(H2,đktc)=0,15.22,4=3,36(l)
c) mFe2O3(nguyên chất)= 80%. 38,4=30,72(g)
=>nFe2O3= 30,72/160=0,192(mol)
PTHH: Fe2O3 + 3 H2 -to->2 Fe +3 H2O
Ta có: 0,192/1 > 0,15/3
=> H2 hết, Fe2O3 dư, tính theo nH2
=> nFe= 2/3. nH2= 2/3. 0,15=0,1(mol)
=>mFe=0,1.56=5,6(g)
Đúng 2
Bình luận (0)
a,\(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right);n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2
Mol: 0,1 0,1 0,15
Tỉ lệ:\(\dfrac{0,1}{2}< \dfrac{0,4}{6}\) ⇒ Al pứ hết,HCl dư
\(\Rightarrow m_{AlCl_3}=0,1.133,5=13,35\left(g\right)\)
b,\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
c,\(m_{Fe_2O_3\left(tinhkhiét\right)}=38,4.\left(100\%-20\%\right)=30,72\left(g\right)\)
⇒\(n_{Fe_2O_3}=\dfrac{30,72}{160}=0,192\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol : 0,15 0,1
Tỉ lệ:\(\dfrac{0,192}{1}>\dfrac{0,15}{3}\)⇒ Fe2O3 dư,H2 hết
=> mFe = 0,1.56 =5,6 (g)
Đúng 0
Bình luận (0)
Cho 11,2 gam Sắt tác dụng vừa đủ với axit clohiđric sinh ra Sắt (II) clorua (FeCl 2 ) và khí H 2 . a. Tính thể tích khí H 2 thoát ra (đktc). b. Tính khối lượng axit clohiđric (HCl) đã dùng cho phản ứng trên. c. Nếu cho hết thể tích khí H 2 trên phản ứng với khí oxi (O 2 ) tạo thành nước (H 2 O). Khối lượng nước thu được là bao nhiêu gam? MỌI NGƯỜI GIẢI GIÚP E PHẦN C BÀI NÀY VỚI AK
Xem chi tiết
a) $Fe + 2HCl \to FeCl_2 + H_2$
Theo PTHH :
$n_{H_2} = n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$V_{H_2} = 0,2.22,4 = 4,48(lít)$
b) $n_{HCl} = 2n_{Fe} = 0,4(mol)$
$m_{HCl} = 0,4.36,5 = 14,6(gam)$
c) $2H_2 + O_2 \xrightarrow{t^o}2H_2O$
Theo PTHH :
$V_{O_2} = \dfrac{1}{2}V_{H_2} = 2,24(lít)$
$n_{H_2O} = n_{H_2} = 0,2(mol)$
$m_{H_2O} = 0,2.18 = 9(gam)$
Đúng 2
Bình luận (0)
Hãy tính thể tích khí CO2 (đktc) tạo thành khi cho 252 gam NaHCO3 tác dụng với dd HCl vừa đủ. ?( Na =23, C=12, O=16, H= 1 )
\(NaHCO_3 + HCl \to NaCl + CO_2 + H_2O\\ n_{CO_2 } = n_{NaHCO_3} = \dfrac{252}{84} = 3(mol)\\ \Rightarrow V_{CO_2} = 3.22,4 = 67,2(lít)\)
Đúng 4
Bình luận (0)
nNaHCO3 = 252/84 = 3 (mol)
NaHCO3 + HCl => NaCl + CO2 + H2O
3______________________3
VCO2 = 3*22.4 = 67.2 (l)
Đúng 1
Bình luận (0)
PT: \(NaHCO_3+HCl\rightarrow NaCl+H_2O+CO_2\)
Ta có: \(n_{NaHCO_3}=\dfrac{252}{84}=3\left(mol\right)\)
Theo PT: \(n_{CO_2}=n_{NaHCO_3}=3\left(mol\right)\)
\(\Rightarrow V_{CO_2}=3.22,4=67,2\left(l\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Cho 10,8 gam nhôm tác dụng hết với dung dịch axit clohiđric . a) Viết PTHH và tính thể tích khí thoát ra (đktc) ? b). Dẫn thể tích khí trên đi qua Sắt (III) oxit dư nung nóng. Có bao nhiêu gam kim loại sắt được tạo ra sau phản ứng trên ?
a)
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$n_{Al} = \dfrac{10,8}{27} = 0,4(mol)$
Theo PTHH : $n_{H_2} = \dfrac{3}{2}n_{Al} = 0,6(mol)$
$V_{H_2} = 0,6.22,4 = 13,44(lít)$
b)
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O$
Theo PTHH : $n_{Fe} = \dfrac{2}{3}n_{H_2} = 0,4(mol)$
$m_{Fe} = 0,4.56 = 22,4(gam)$
Đúng 1
Bình luận (0)
Bài 10: Đốt cháy quặng kẽm sunfua (ZnS), chất này tác dụng với oxi tạo thành kẽm oxit và khí sunfurơ. Nếucho 19,4 gam ZnS tác dụng với 8,96 lít khí oxi (đktc) thì khí sunfurơ có thể tích sinh ra là bao nhiêu?
PT: \(2ZnS+3O_2\underrightarrow{t^o}2ZnO+2SO_2\)
Ta có: \(n_{ZnS}=\dfrac{19,4}{97}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,4}{3}\), ta được O2 dư.
Theo PT: \(n_{SO_2}=n_{ZnS}=0,2\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,2.22,4=4,48\left(l\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
\(n_{ZnS} = \dfrac{19,4}{97} = 0,2(mol)\\ n_{O_2} = \dfrac{8,96}{22,4} = 0,4(mol)\\ 2ZnS + 3O_2 \xrightarrow{t^o} 2ZnO + 2SO_2\\ \dfrac{n_{Zn}}{2} = 0,1 < \dfrac{n_{O_2}}{3} = 0,133\)
Do đó, oxi dư
\(n_{SO_2} = n_{ZnS} = 0,2(mol)\\ \Rightarrow V_{SO_2} = 0,2.22,4 = 4,48(lít)\)
Đúng 1
Bình luận (0)