cho 19,6 gam kim loại chưa rõ hóa trị tan trong HNO3 dư sau pu thu được 6,72 lít khi hỗn hợp khí NO và NO2 có tỷ khối so với Hidro bằng 17. Tìm M?
a) Zn
b)Mg
c) Fe
d) AI
cho a gam một kim loại có hóa trị II tan hết trong dung dịch HNO3 dư, sau phản ứng thu được 66,15 gam muối kim loại, axit dư và hỗn hợp khí X gồm NO và NO2 . Tỉ khối của X so với H2 bằng 20. Tìm kim loại đó
\(Đặt:n_A=x\left(mol\right),n_{NO}=a\left(mol\right),n_{NO_2}=b\left(mol\right)\)
\(Giảsử:n_{khí}=1\left(mol\right)\)
\(\Rightarrow a+b=1\left(mol\right)\left(1\right)\)
\(\overline{M_{khí}}=\dfrac{30a+46b}{a+b}=20\cdot2\)
\(\Leftrightarrow30a+46b=40\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.375,b=0.625\)
\(BTe:2n_A=3n_{NO}+n_{NO_2}\Rightarrow n_A=\dfrac{3\cdot0.375+0.625}{2}=0.875\left(mol\right)\)
\(m_{A\left(NO_3\right)_2}=0.875\cdot\left(A+124\right)=66.15\left(g\right)\\ \Rightarrow A=\)
Đến đây bạn xem lại đề nhé.
Đề có thiếu thể tích hỗn hợp khí không bạn ơi ?
Hòa tan hoàn toàn 32 gam kim loại M trong dung dịch HNO3 dư thu được 8,96 lít hỗn hợp khí B gồm NO và NO2 ở đktc. Tỉ khối của B so với hiđro bằng 17. Kim loại M là
A. Al
B. Cu
C. Fe
D. Mg
Đáp án B
Tính số mol các khí trong B:
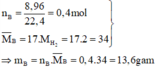
Đặt số mol các khí trong B là NO : a mol ; NO2 : b mol
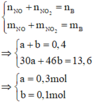
Số mol của M là: n M = 32 M m o l
Gọi n là hóa trị của M
Sơ đồ phản ứng:

Hỗn hợp M gồm Al, A l 2 O 3 , F e 3 O 4 ,CuO,Fe và Cu trong đó oxi chiếm 20,4255% khối lượng hỗn hợp. Cho 6,72 lít khí CO (đktc) đi qua 35,25 gam M nung nóng, sau một thời gian thu được hỗn hợp rắn N và hỗn hợp khí X có tỉ khối so H 2 với bằng 18. Hòa tan toàn bộ N trong lượng dư dung dịch H N O 3 loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa m gam muối (không có N H 4 N O 3 ) và 4,48 lít (đktc) hỗn hợp khí Z gồm N O v à N O 2 . Tỉ khối của Z so với H 2 là 16,75 lít Giá trị của m là
A. 96,25
B. 117,95
C. 80,75
D. 139,50
Hỗn hợp X gồm Fe và kim loại M hóa trị 3. Chia 38,6 gam X thành 2 phần bằng nhau. Phần 1 cho tan hoàn toàn trong dung dịch HNO3 loãng dư thu được 6,72 lít hỗn hợp khí Y gồm NO, N2O, d(Y/H2) = 17,8. Phần 2 cho vào dung dịch kiềm sau một thời gian thấy lượng H2 thoát ra vượt quá 6,72 lít. Tính % khối lượng kim loại M (khí đo ở đktc)
A. 58,03%
B. 41,97%
C. 56,12%
D. 43,08%
Hòa tan hoàn toàn m gam hỗn hợp gồm ba kim loại bằng dd HNO3 thu được 1,12 lít hỗn hợp khí D gồm NO2 và NO. Tỉ khối hơi của D so với hidro bằng 18,2. Tính thể tích tối thiểu dd HNO3 37,8% (d=1,242 g/ml) cần dùng
Cho m gam hỗn hợp P gồm Mg và Al có tỷ lệ mol 4:5 vào dung dịch HNO3 20%. Sau khi các kim loại tan hết có 6,72 lít hỗn hợp X gồm NO, N2O, N2 bay ra (đktc) và được dung dịch A. Thêm một lượng O2 vừa đủ vào X, sau phản ứng được hỗn hợp khí Y. Dẫn Y từ từ qua dung dịch KOH dư, có 4,48 lít hỗn hợp khí Z đi ra (đktc). Tỉ khối của Z đối với H2 bằng 20. Nếu cho dung dịch NaOH vào dung dịch A thì lượng kết tủa lớn nhất thu được là (m + 39,1) gam .Biết HNO3 dùng dư 20 % so với lượng cần thiết.Nồng độ % của Al(NO3)3 trong A gần nhất với
A. 9,5%
B. 9,6%
C. 9,4%
D. 9,7%
Đáp án : D
.nX = 0,3 mol ; nZ = 0,2 mol
Chỉ có NO phản ứng với O2 tạo NO2 bị hấp thụ vào nước
=> nNO = 0,3 – 0,2 = 0,1 mol
MZ= 40g (Z gồm N2 và N2O )
=> nN2 = 0,05 mol ; nN2O = 0,15 mol
.m(g) P : Mg,Al -> Kết tủa lớn nhất : Mg(OH)2 ; Al(OH)3 : (m + 39,1)g
=> mOH = (m + 39,1) – m = 39,1g => nOH = 2,3 mol = 2nMg + 3nAl
Lại có : nMg : nAl = 4 : 5 => nMg = 0,4 mol ; nAl = 0,5 mol
Bảo toàn e : 2nMg + 3nAl = 10nN2 + 8nN2O + 3nNO + 8nNH4NO3
=> nNH4NO3 = 0,0375 mol
=> Bảo toàn N : nHNO3 pứ = 2nMg + 3nAl + 2nN2 + nNO + 2nN2O + 2nNH4NO3
=> nHNO3 pứ = 2,875 mol
=> nHNO3 đầu = 3,45 mol => mdd HNO3 = 1086,75g
=> mdd sau = mP + mdd HNO3 - mkhí = 1098,85g
=> %CAl(NO3)3 = 9,69%
Cho m gam hỗn hợp P gồm Mg và Al có tỷ lệ mol 4:5 vào dung dịch HNO3 20%. Sau khi các kim loại tan hết có 6,72 lít hỗn hợp X gồm NO, N2O, N2 bay ra (đktc) và được dung dịch A. Thêm một lượng O2 vừa đủ vào X, sau phản ứng được hỗn hợp khí Y. Dẫn Y từ từ qua dung dịch KOH dư, có 4,48 lít hỗn hợp khí Z đi ra (đktc). Tỉ khối của Z đối với H2 bằng 20. Nếu cho dung dịch NaOH vào dung dịch A thì lượng kết tủa lớn nhất thu được là (m + 39,1) gam .Biết HNO3 dùng dư 20 % so với lượng cần thiết.Nồng độ % của Al(NO3)3 trong A gần nhất với :
A. 9,7%
B. 9,6%
C. 9,5%
D. 9,4%
Cho m gam hỗn hợp A gồm Mg và Al có tỷ lệ mol 4:5 vào dung dịch HNO3 20%. Sau khi các kim loại tan hết có 6,72 lít hỗn hợp X gồm NO, N2O, N2 bay ra (đktc) và được dung dịch X1. Thêm một lượng O2 vừa đủ vào X, sau phản ứng được hỗn hợp khí Y. Dẫn Y từ từ qua dung dịch KOH dư, có 4,48 lít hỗn hợp khí Z đi ra (đktc). Tỉ khối của Z đối với H2 bằng 20. Nếu cho dung dịch NaOH vào dung dịch X1 thì lượng kết tủa lớn nhất thu được là (m + 39,1) gam. Biết HNO3 dùng dư 20 % so với lượng cần thiết. Nồng độ % của Al(NO3)3 trong X1 gần nhất với giá trị nào sau đây?
A. 9,5%
B. 9,7%
C. 9,6%
D. 9,4%
Đáp án : B
n hh X = 6,72: 22,4 = 0,3 mol
n hh Z = 4,48 : 22,4 = 0,2 mol
M ¯ hh Z = 20.2 = 40
Z gồm N2 và N2O
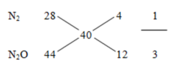
=> n N2 = 0,05 mol
n N2O = 0,15 mol
=> n NO = n X – n Z = 0,1 mol
Mặt khác, có hh A (Mg, Al) => Kết tủa chứa Al(OH)3 và Mg(OH)2
m → m+ 39,1
Gọi n Mg = a mol => n Al = 1,25a mol
m hh A = 24a + 33,75a = 57,75 a = m
m↓ = 58a + 97,5 a = 57,75a + 39,1
<=> a = 0,4 mol
=> n Mg = 0,4; n Al = 0,5 mol
Mg → Mg+2 + 2e
0,4 0,8
Al → Al+3 + 3e
0,5 1,5
N+5 + 10e → N2
0,5 0,05
N+5 + 8e → N-3
8a a
N+5 + 3e → N+2
0,3 0,1
2N+5 + 8e → N2O
1,2 0,15
Bảo toàn electron, ta có: 0,8 + 1,5 = 0,3 + 1,2 + 0,5 + 8a
<=> 8a = 0,3
<=> a = 0,0375 mol
=> ∑ n HNO3p.ư = n NO3 – (muối của KL) + n N(sp khử) + 2 n NH4NO3
= 2,3 + 0,1 + 0,15. 2 + 0,05. 2 + 0,0375. 2
= 2,875 mol
=> n HNO3 t.t = 3,45 mol => mdd HNO3 = (3,45. 63)/ 0,2 = 1086,75 g
=> m dd sau p.ư = m KL + m HNO3 – n khí
= 0,4. 24 + 0,5. 27 + 1086,75 – 0,1. 30 – 0,05. 28 – 0,15. 44
= 1098,85 gam
C% Al(NO3)3 = 106,5 : 1098,85 = 9,7%
Hòa tan m gam hỗn hợp X gồm Fe và Cu bằng dung dịch HNO3 dư thu được 6,72 lít (đktc) hỗn hợp khí B gồm NO và NO2 có khối lượng 12,2 gam. Tính số mol HNO3 phản ứng.
Gọi x, y lần lượt là số mol NO va NO2
\(\left\{{}\begin{matrix}x+y=0,3\left(mol\right)\\30x+46y=12,2\end{matrix}\right.\)
=> x= 0,1 (mol ) ; y=0,2 (mol)
\(n_{HNO_3}=4n_{NO}+2n_{NO_2}=4.0,1+2.0,2=0,8\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{NO}=x\left(mol\right)\\n_{NO_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{6,72}{22,4}=0,3\left(1\right)\)
Theo đề bài, có: 30x + 46y = 12,2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
Theo ĐLBT mol e, có: \(3n_{Fe}+2n_{Cu}=0,1.3+0,2=0,5\left(mol\right)\)
Muối thu được gồm: Fe(NO3)3 và Cu(NO3)2
BTNT Fe, Cu: nFe(NO3)3 = nFe và nCu(NO3)2 = nCu
BTNT N, có: nHNO3 = nNO + nNO2 + 3nFe(NO3)3 + 2nCu(NO3)2
= 0,1 + 0,2 + 0,5 = 0,8 (mol)
Bạn tham khảo nhé!