nhiệt phân 15,8 KMnO4 thu được lượng oxi. Đốt cháy 5,6 gam sát trong lượng oxi vừa thu đc thì sản phẩm sau phản ứng có bị hút vaò nam châm k

Những câu hỏi liên quan
nhiệt phân 15,8 gam KMnO4 thu được lượng khí õi, đốt cháy 5,6g sắt trong lượng khí oxi vừa thu được thì sản phẩm sau phản ứng có bị nam châm hút hay không ? hãy giả thích ?
2KMnO4 \(\xrightarrow[]{t^o}\) K2MnO4 + MnO2 + O2(1)
3Fe + 2O2 \(\xrightarrow[]{t^o}\) Fe3O4(2)
nKMnO4 = 15,8 : 158 = 0,1 mol
nFe = 5,6 : 56 = 0,1 mol
Theo pt 1 nO2 = \(\dfrac{1}{2}nKMnO_4=0,05mol\)
Lập tỉ lệ phương trình (2)
nFe : nO2 = \(\dfrac{0,1}{3}:\dfrac{0,05}{2}\)
Do 0,1/3 > 0,05/2 => Fe dư
Vậy sản phẩm thu được có Fe dư => bị nam châm hút
Đúng 1
Bình luận (0)
Nhiệt phân 15,8 gam KMnO4 thu được lượng khó O2,đốt cháy 5,6g Fe trong lượng khó O2 vừa thu được thì sản phẩm sau phản ứng có bị cục nam châm hút không? vì sao
không vì nó kết hợp vs O2 tạo ra oxit
Đúng 0
Bình luận (0)
Bài 1:
| Đơn chất | Hợp chất |
| S, O2 | NaCl, MgSO4, KCl, P2O5 |
Bài 2:
a) AgNO3
CTHH AgNO3 mang ý nghĩa:
- Là hợp chất tạo bởi 3 nguyên tố hóa học : Ag , N và O
- Tạo bởi 1 nguyên tử nguyên tố Ag, 1 nguyên tử nguyên tố N và 3 nguyên tử nguyên tố O.
- \(PTK_{AgNO_3}=NTK_{Ag}+NTK_N+3.NTK_O\\ =108+14+3.16=170\left(đ.v.C\right)\)
b) KHSO4
CTHH KHSO4 mang ý nghĩa:
- Là hợp chất cấu tạo từ 4 nguyên tố hóa học: K,H,S và O
- Cấu tạo bởi 1 nguyên tử nguyên tố K, 1 nguyên tử nguyên tố H, 1 nguyên tử nguyên tố A và 4 nguyên tử nguyên tố O.
- \(PTK_{KHSO_4}=NTK_K+NTK_H+NTK_S+4.NTK_O\\ =39+1+32+4.16=136\left(đ.v.C\right)\)
Bài tập 3:
a) Gọi CT ghi hóa trị của S(IV) và O là \(S_x^{IV}O_y^{II}\)(x,y : nguyên, dương)
Theo quy tắc hóa trị, ta có:
\(x.IV=y.II\\ =>\dfrac{x}{y}=\dfrac{II}{IV}=\dfrac{2}{4}=\dfrac{1}{2}\)
=> x=1; y=2
=> CTHH là SO2
b) Gọi CT ghi hóa trị của Al(III) và Cl(I) là \(Al_x^{III}Cl_y^I\) (x,y: nguyên, dương)
Theo quy tắc hóa trị ta có:
\(x.III=y.I\\ =>\dfrac{x}{y}=\dfrac{I}{III}=\dfrac{1}{3}\)
=> x=1; y=3
=> CTHH là AlCl3
Bài 4:
a) Gọi CT gọi hóa trị của hợp chất CuCl2 là \(Cu^aCl_2^b\)(a,b: nguyên, dương)
Theo Quy tắc hóa trị, ta có:
\(1.a=2.b\\ =>\dfrac{a}{b}=\dfrac{2}{1}=\dfrac{II}{I}\)
=> a= II, b=I
=> Trong hợp chất CuCl2 : Cu(II) và Cl(I)
b) Gọi CT kèm hóa trị của hợp chất Fe(NO3)2 là: \(Fe^a\left(NO_3\right)_2^b\) (a,b: nguyên, dương)
Theo quy tắc hóa trị, ta có:
\(1.a=2.b\\ =>\dfrac{a}{b}=\dfrac{2}{1}=\dfrac{II}{I}\\ =>a=II;b=I\)
=> Trong hợp chất Fe(NO3)2 : Fe(II) và nhóm nguyên tử NO3 (I)
Đúng 0
Bình luận (0)
Nhiệt phân 15,8gam KMnO₄ thu được lượng khí oxi, đốt cháy 5,6g sắt trong lượng khí oxi vừa thu được thì sản phẩm sau phản ứng có bin nam châm hút hay không ? Hãy giải thích?
nKMnO4=15,8/158=0,1 mol
2KMnO4 --> K2MnO4 + MnO2 + O2
0,1 0,05
nFe=5,6/56=0,1
3Fe + 2O2 -to--> Fe3O4
0,1 0,05 mol
ta thấy nFe/3=0,1/3 > nO2/2=0,05/2=0,025
=> Fe dư ,O2 hết => bin nam châm vẫn hút được hỗn hợp sau phản ứng
Đúng 0
Bình luận (0)
Nhiệt phân 15,8g K M n O 4 thu được lượng khí O 2 , đốt cháy 5,6g Fe trong lượng khí O 2 vừa thu được thì sản phẩm sau phản ứng có bị cục nam châm hút không? Hãy giải thích
Phương trình hóa học:
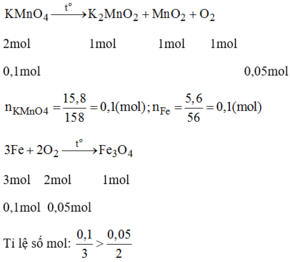
Vậy sắt còn dư nên khi đưa nam châm lại gần sản phẩm sau phản ứng thì nam châm bị hút.
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 15,8 g KMnO4 thu được v lít khí Oxi a Tính v b đốt cháy 5,6 gam sắt trong V lít khí Oxi nói trên sản phẩm thu được là oxit sắt từ fe3 o4 tính khối lượng chất rắn thu được sau phản ứng
PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
a. Theo PTHH: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=\dfrac{1}{2}0,1=0,05\left(mol\right)\)
\(\Rightarrow V_{O_2}=n_{O_2}.22,4=0,05.22,4=1,12\left(l\right)\)
b. PTHH: \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Ta có: \(\dfrac{1}{n_{O_2}}=\dfrac{1}{0,05}\)
\(\dfrac{1}{n_{Fe}}=\dfrac{1}{0,1}\)
\(\Rightarrow\dfrac{1}{n_{O_2}}>\dfrac{1}{n_{Fe}}\)
Vậy Fe dư
Theo PTHH: \(n_{Fe_3O_4}=\dfrac{0,1.1}{3}=\dfrac{1}{30}\left(mol\right)\)
\(\Rightarrow m_{Fe_3O_4}=n_{Fe_3O_4}.M_{Fe_3O_4}=\dfrac{1}{30}.232\approx7,73g\)
Đúng 2
Bình luận (0)
Nhiệt phân 15,8 gam KMnO4 thu đc lượng khí O2 . Đốt cháy 5,6 gam Fe trong lượng khí O2 vừa thu đc thì sản phẩm au phản ứng có bị cục nam châm hút ko? VÌ sao.
2KMnO4→→K2MnO4+MnO2+O2
\(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=\dfrac{1}{2}.\dfrac{15,8}{158}=0,05mol\\ n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ 3Fe+2O_2\rightarrow Fe_3O_4\\ \dfrac{0,1}{3}\approx0,33>\dfrac{0,05}{2}=0,25\)
Suy ra Fe dư=0,1-0,05.3:2=0,025 mol. Vậy sản phẩm gồm Fe3O4 và Fe dư nên nam châm vẫn hút.
Đúng 0
Bình luận (0)
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: \(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\uparrow\left(1\right)\)
Theo PTHH(1): \(n_{O_2}=\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
PTHH (2): \(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\left(2\right)\)
\(\left\{{}\begin{matrix}\dfrac{n_{Fe}}{3}=\dfrac{0,1}{3}=0,03\\\dfrac{n_{O_2}}{2}=\dfrac{0,05}{2}=0,025\end{matrix}\right.\) \(\Rightarrow\) Fe dư. O2 phản ứng hết
Vậy Fe còn dư nên sản phẩm sau ohanr ứng bị nam châm hút.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 13g kẽm , trong bình chứa khí oxi , thu được sản phẩm là kẽm oxit -a. Viết PTPỨ xảy ra -b.Tính thể tích oxi tham gia phản ứng -c.Tính khối lượng sản phẩm thu được -d.Tính khối lượng KMnO4 cần dùng để khi phân huỷ thì thu được 1 thể khí oxi ( ĐKTC ) bằng với thể tích khí oxi đã sử dụng với phản ứng trên
a, nZn = 13/65 = 0,2 (mol)
PTHH: 2Zn + O2 -> (t°) 2ZnO
Mol: 0,2 ---> 0,1 ---> 0,2
b, VO2 = 0,1 . 22,4 = 2,24 (l)
c, mZnO = 0,2 . 81 = 16,2 (g)
d, PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,1 . 2 = 0,2 (mol)
mKMnO4 = 0,2 . 158 = 31,6 (g)
Đúng 1
Bình luận (0)
2Zn+O2-to>2ZnO
0,2---0,1-----0,2
n Zn=\(\dfrac{13}{65}\)=0,2 mol
=>VO2=0,1.22,4=2,24l
=>m ZnO=0,2.81=16,2g
d)
2KMnO4-to>K2MnO4+MnO2+O2
0,2-----------------------------------0,1
=>m KMnO4=0,2.158=31,6g
Đúng 0
Bình luận (0)
a, nZn = 13/65 = 0,2 (mol)
PTHH: 2Zn + O2 -> (t°) 2ZnO
Mol: 0,2 ---> 0,1 ---> 0,2
b, VO2 = 0,1 . 22,4 = 2,24 (l)
c, mZnO = 0,2 . 81 = 16,2 (g)
d, PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,1 . 2 = 0,2 (mol)
mKMnO4 = 0,2 . 158 = 31,6 (g)
Đúng 1
Bình luận (0)
Câu 1. Muốn điều chế được 4,48 lít khí oxi (đktc) thì khối lượng KMnO4 cần nhiệt phân là bao nhiêu? (Cho nguyên tử khối: O 16, K 39, Mn 55)Câu 2. Đốt cháy 6,2 gam photpho với 6,4 gam oxi trong không khí, sản phẩm thu được là điphotpho pentaoxit (P2O5).a. Viết PTHH của phản ứng.b. Sau phản ứng chất nào còn dư và số mol chất còn dư là bao nhiêu?b. Tính khối lượng sản phẩm tạo thành.
Đọc tiếp
Câu 1. Muốn điều chế được 4,48 lít khí oxi (đktc) thì khối lượng KMnO4 cần nhiệt phân là bao nhiêu? (Cho nguyên tử khối: O = 16, K = 39, Mn = 55)
Câu 2. Đốt cháy 6,2 gam photpho với 6,4 gam oxi trong không khí, sản phẩm thu được là điphotpho pentaoxit (P2O5).
a. Viết PTHH của phản ứng.
b. Sau phản ứng chất nào còn dư và số mol chất còn dư là bao nhiêu?
b. Tính khối lượng sản phẩm tạo thành.
C1:
nO2 = 4,48/22,4 = 0,2 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,2 . 2 = 0,4 (mol)
mKMnO4 = 0,4 . 158 = 63,2 (g)
C2:
nP = 6,2/31 = 0,2 (mol)
nO2 = 6,4/32 = 0,2 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
LTL: 0,2/4 > 0,2/5 => P dư
nP2O5 = 0,2/5 . 2 = 0,08 (mol)
mP2O5 = 0,08 . 142 = 11,36 (g)
Đúng 3
Bình luận (0)
Đốt cháy 6,72 lít khí hiđro trong bình chứa 4,48 lít khí oxi.
a) Sau phản ứng, chất nào còn dư? Dư bao nhiêu gam?
b) Tính khối lượng sản phẩm thu được?
c) Tính khối lượng KMnO4 cần dùng để điều chế được lượng oxi dùng cho phản ứng trên?
(PTHH: KMnO4--->K2MnO4+MnO2+O2)
a, Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{2}< \dfrac{0,2}{1}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,05\left(mol\right)\Rightarrow m_{O_2\left(dư\right)}=0,05.32=1,6\left(g\right)\)
b, \(n_{H_2O}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,3.18=5,4\left(g\right)\)
c, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
_______0,3_______________________0,15 (mol)
\(\Rightarrow m_{KMnO_4}=0,3.158=47,4\left(g\right)\)
Bạn tham khảo nhé!
Đúng 4
Bình luận (0)




























