SĐ điều chế: FeS2 ----> SO2 ----> SO3 -----> H2SO4
Theo lí thuyết:120....................................................98...
Thực tế:............?..........................................................98..
=> mFeS2=120(kg)
Vì quặng chỉ chứa 80% FeS2 => m quặng =\(\frac{120}{80\%}=150\left(kg\right)\)
Gọi R là kim loại cần tìm => CT oxit của R: RO
PTHH: RO+H2SO4\(\rightarrow RSO_4+H_2O\)
Theo PT : \(n_{RO}=n_{H_2SO_4}=\frac{100.9,8\%}{98}=0,1\left(mol\right)\)
\(\Rightarrow\frac{8}{R+16}=0,1\Rightarrow R=64\left(Cu\right)\)
=> CT oxit : CuO
Gọi R là KL cần tìm
CTHH: RO
PTHH; RO+H2SO4--->RSO4+H2O
Ta có
n\(_{RO}=n_{H2SO4}=\frac{100.9,8}{98}=0,1\left(mol\right)\)
Theo bài ra ta có
\(\frac{8}{R+18}=0,1\Rightarrow R=64\)(Cu)
CTHH: CuO












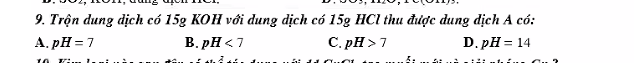












 giúp mình câu c với ạ, 2 câu trên mình biết làm rồi
giúp mình câu c với ạ, 2 câu trên mình biết làm rồi

