Fluorine được sử dụng làm chất oxi hóa cho nhiên liệu lỏng dùng trong tên lửa. Fluorine (F) là một nguyên tố hóa học có số hiệu nguyên tử bằng 9, thuộc chu kì 2, nhóm VIIA. Từ vị trí của fluorine trong bảng tuần hoàn, có thể dự đoán được tính chất hóa học cơ bản của fluorine không? Khả năng phản ứng của fluorine như thế nào?
Bài 7: Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hoá học
Mở đầu (SGK Chân trời sáng tạo trang 49)
Fluorine được sử dụng làm chất oxi hóa cho nhiên liệu lỏng dùng trong tên lửa. Fluorine (F) là một nguyên tố hóa học có số hiệu nguyên tử bằng 9, thuộc chu kì 2, nhóm VIIA. Từ vị trí của fluorine trong bảng tuần hoàn, có thể dự đoán được tính chất hóa học cơ bản của fluorine không? Khả năng phản ứng của fluorine như thế nào?
Đọc tiếp
Thảo luận (1)
Cậu hỏi 1 (SGK Chân trời sáng tạo trang 49)
Quan sát Bảng 7.1, hãy nhận xét về số electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm A trong cùng một chu kì và trong cùng một nhóm. 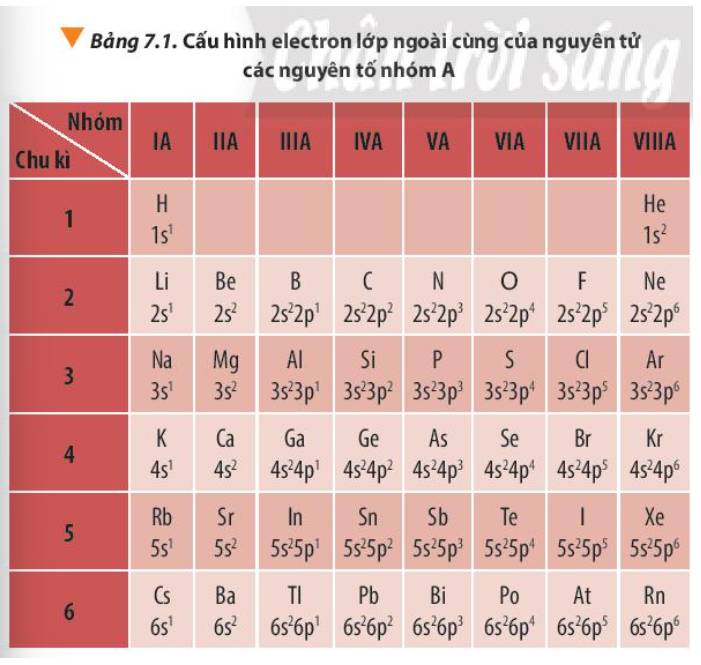
Thảo luận (1)Hướng dẫn giải- Số electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm `A` trong cùng `1` chu kì có xu hướng tăng dần từ trái qua phải và `2` nguyên tố cạnh nhau hơn kém `1 e.`
- Số electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm `A` trong cùng `1` nhóm thì có số electron lớp ngoài cùng bằng nhau.
(Trả lời bởi 2611)
Luyện tập (SGK Chân trời sáng tạo trang 50)
Hãy nêu xu hướng biến đổi một số tính chất của các nguyên tố, đơn chất và hợp chất của chúng để minh họa nội dung của định luật tuần hoàn.
Thảo luận (1)Hướng dẫn giảiXu hướng biến đổi một số tính chất của các nguyên tố, đơn chất:
- Tính oxi hóa, tính khử
+ Trong 1 chu kì, từ trái qua phải, tính oxi tăng dần, tính khử giảm dần
+ Trong 1 nhóm, từ trên xuống dưới, tính oxi hóa giảm dần, tính khử tăng dần
- Tính phi kim, kim loại
+ Trong 1 chu kì, từ trái qua phải, tính phi kim tăng dần, tính kim loại giảm dần
+ Trong 1 nhóm, từ trên xuống dưới, tính phi kim giảm dần, tính kim loại tăng dần
- Bán kính nguyên tử
+ Trong 1 chu kì, từ trái qua phải, bán kính nguyên tử giảm dần
+ Trong 1 nhóm, từ trên xuống dưới, bán kính nguyên tử tăng dần
Xu hướng biến đổi một số tính chất của hợp chất (oxide, hydroxide)
- Tính acid, base
+ Trong 1 chu kì, từ trái qua phải, tính acid tăng dần, tính base giảm dần
+ Trong 1 nhóm, từ trên xuống dưới, tính acid giảm dần, tính base tăng dần
(Trả lời bởi Mai Trung Hải Phong)
Cậu hỏi 2 (SGK Chân trời sáng tạo trang 50)
Dựa trên các kiến thức đã được học, hoàn thành những thông tin còn thiếu trong Bảng 7.2.

Thảo luận (1)Hướng dẫn giải
Luyện tập (SGK Chân trời sáng tạo trang 50)
a) Nguyên tố potassium thuộc ô 19 trong bảng tuần hoàn. Cho biết cấu tạo của nguyên tử này.
b) Nguyên tử của nguyên tố chlorine có 17 proton. Cho biết vị trí của nguyên tố này trong bảng tuần hoàn
c) Nguyên tử của nguyên tố sulfur thuộc ô 16 trong bảng tuần hoàn. Cho biết tính chất hóa học cơ bản của nguyên tố sulfur
Thảo luận (1)Hướng dẫn giảia) Nguyên tố potassium thuộc ô 19.
⇒ Số hiệu nguyên tử Z = 19 = số proton = số electron.
Cấu hình electron K (Z = 19): 1s22s22p63s23p64s1.
Số lớp electron: 4.
Số electron lớp ngoài cùng: 1.
b) Nguyên tử của nguyên tố chlorine có 17 proton.
⇒ Số thứ tự nguyên tố: 17
Cấu hình electron: 1s22s22p63s23p5
Số thứ tự chu kì = số lớp electron = 3
Số thứ tự nhóm VIIA (do 7 electron lớp ngoài cùng, nguyên tố p).
c) Nguyên tử của nguyên tố sulfur thuộc ô 16
⇒ Số hiệu nguyên tử Z = số proton = số electron = 16
Cấu hình electron: 1s22s22p63s23p4
Dựa vào cấu hình electron ta thấy nguyên tử nguyên tố sulfur có 6 electron lớp ngoài cùng
⇒ Là phi kim
Hóa trị cao nhất với oxygen là VI.
Công thức oxide cao nhất: SO3 là acidic oxide.
Công thức hydroxide tương ứng: H2SO4 là acid mạnh.
(Trả lời bởi Phía sau một cô gái)
Vận dụng (SGK Chân trời sáng tạo trang 51)
Potassium hydroxide (KOH) là một trong những hóa chất quan trọng của ngành công nghiệp. Chất này được sử dụng để sản xuất chất tẩy rửa gia dụng, thuốc nhuộm vải, phân bón,… Hãy dự đoán hydroxide này có tính base mạnh hay yếu.
Thảo luận (1)Hướng dẫn giảiKOH được sử dụng để làm chất tẩy rửa gia dụng
=> Khả năng tham gia phản ứng hóa học mạnh
=> Tính base mạnh
(Trả lời bởi Mai Trung Hải Phong)
Bài tập 1 (SGK Chân trời sáng tạo trang 51)
Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần
A. khối lượng nguyên tử
B. bán kính nguyên tử
C. số hiệu nguyên tử
D. độ âm điện của nguyên tử
Thảo luận (2)Hướng dẫn giải- Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần sô đơn vị điện tích hạt nhân
- Số đơn vị điện tích hạt nhân = số hiệu nguyên tử
=> Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần của số hiệu nguyên tử
Đáp án C
(Trả lời bởi Mai Trung Hải Phong)
Bài tập 2 (SGK Chân trời sáng tạo trang 51)
Nguyên tố Ca có số hiệu nguyên tử là 20. Phát biểu nào sau đây về Ca là không đúng?
A. Số electron ở vỏ nguyên tử của nguyên tố Ca là 20
B. Vỏ của nguyên tử Ca có 4 lớp electron và lớp ngoài cùng có 2 electron
C. Hạt nhân của nguyên tử nguyên tố Ca có 20 proton
D. Nguyên tố Ca là một phi kim
Thảo luận (1)Hướng dẫn giải
Bài tập 3 (SGK Chân trời sáng tạo trang 51)
Một nguyên tố kim loại được sử dụng làm vỏ lon nước giải khát. Nguyên tử của nguyên tố này có cấu hình electron: [Ne]3s23p1. Hãy xác định tên nguyên tố này và vị trí của nó trong bảng tuần hoàn. Nêu cấu tạo nguyên tử và tính chất của nguyên tố này.
Thảo luận (1)Hướng dẫn giảiCấu hình electron: [Ne] 3s2 3p1 -> Al
Vị trí: + Ô thứ 13
+ Chu kì 3
+ Nhóm IIIA
- Tính chất: Kim loại
(Trả lời bởi 9323)
Bài tập 4 (SGK Chân trời sáng tạo trang 51)
Nguyên tử của một nguyên tố có cấu hình electron: [Ar]4s2. Nguyên tố này là một trong những nguyên tố thiết yếu cho cơ thể, được bổ sung trong các sản phẩm sữa. Hãy xác định vị trí của nguyên tố này trong bảng tuần hoàn và cho biết tính chất của nó.
Thảo luận (1)Hướng dẫn giảiCấu hình khí hiếm Ar: 1s2 2s2 2p6 3s2 3p6
-> 1s2 2s2 2p6 3s2 3p6 4s2 => Ca (Cacium)
- Tính chất: Kim loại
(Trả lời bởi 9323)
