Từ các phản ứng của các oxide và hydroxide: Na2O, NaOH, Al2O3, Al(OH)3, SO3, H2SO4 với các dung dịch HCl, KOH, hãy nhận xét tính acid, base của các oxide và hydroxide trên.
Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm
Câu hỏi 7 (SGK Chân trời sáng tạo trang 46)
Thảo luận (2)
Câu hỏi 8 (SGK Chân trời sáng tạo trang 47)
Quan sát Bảng 6.2, hãy liên hệ xu hướng biến đổi tính acid, tính base của oxide và hydroxide tương ứng với tính kim loại, phi kim của các nguyên tố trong chu kì.
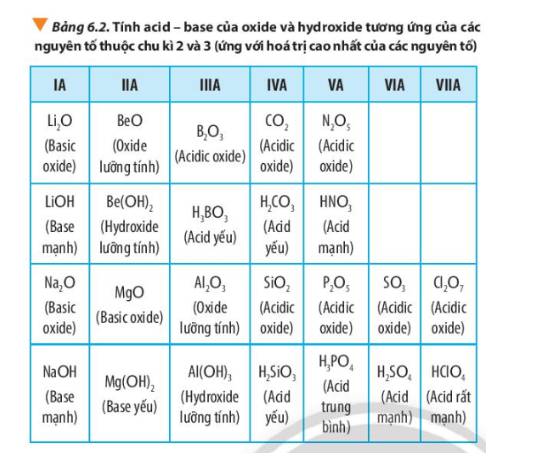
Thảo luận (1)Hướng dẫn giải- Trong 1 chu kì:
+ Tính kim loại giảm dần, tính phi kim tăng dần.
+ Tính base của oxide, hydroxide giảm dần; tính acid của oxide, hydroxide tăng dần
(Trả lời bởi GV Nguyễn Trần Thành Đạt)
Luyện tập (SGK Chân trời sáng tạo trang 47)
Dựa vào xu hướng biến đổi tính acid - base của oxide và hydroxide tương ứng của các nguyên tố trong bảng tuần hoàn, hãy sắp xếp các hợp chất sau đây theo chiều giảm dần tính acid của chúng: H2SiO3, HClO4, H2SO4, H3PO4.
Thảo luận (2)Hướng dẫn giải- Trong cùng 1 chu kì, tính từ trái trang phải, tính acid của hydroxide tương ứng của các nguyên tố trong bảng tuần hoàn tăng dần
=> Sắp xếp theo chiều giảm dần tính acid: HClO4 > H2SO4 > H3PO4 > H2SiO4
(Trả lời bởi Mai Trung Hải Phong)
Vận dụng (SGK Chân trời sáng tạo trang 47)
Aspartame là một chất làm ngọt nhân tạo, được sử dụng trong một số loại soda dành cho người ăn kiêng. Xác định vị trí của các nguyên tố tạo nên aspartame trong bảng tuần hoàn. Trong số các nguyên tố đó, nguyên tố nào có tính phi kim mạnh nhất?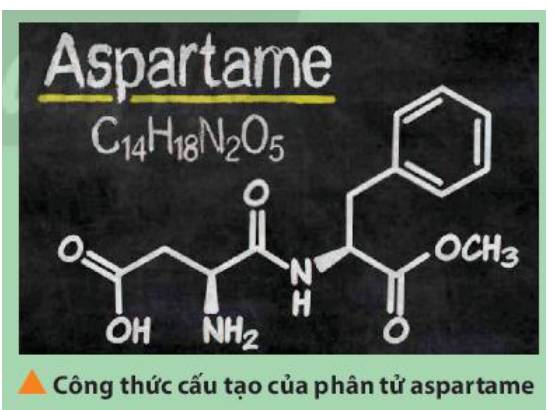
Thảo luận (1)Hướng dẫn giải- H: ô số 1, nhóm IA, chu kì 1
- C: ô số 6, nhóm IVA, chu kì 2
- N: ô số 7, nhóm VA, chu kì 2
- O: ô số 8, nhóm VIA, chu kì 2
- Trong cùng 1 chu kì, theo chiều tăng dần điện tích hạt nhân, tính phi kim tăng dần
=> Tính phi kim: C < N < O
- H có tính phi kim yếu
=> Nguyên tố O có tính phi kim mạnh nhất
(Trả lời bởi GV Nguyễn Trần Thành Đạt)
Bài tập 1 (SGK Chân trời sáng tạo trang 47)
Nguyên tử của nguyên tố nào sau đây có bán kính nhỏ nhất?
A. Si (Z = 14)
B. P (Z = 15)
C. Ge (Z = 32)
D. As (Z = 33)
Thảo luận (1)Hướng dẫn giải`@` Ta thấy `Si ; P` cùng ở chu kì `3` còn `Ge ; As` cùng ở chu kì `4`
Dựa vào BTHHH: `=>{(bk_[Si] < bk_P),(bk_[Ge] < bk_[As]):}` `(1)`
`@` Thấy `Si ; Ge` cùng ở nhóm `IV A` còn `P ; As` cùng ở nhóm `V A`
Dựa vào BTHHH: `=>{(bk_[Ge] < bk_[Si]),(bk_[As] < bk_[P]):}` `(2)`
Từ `(1);(2)=>bk_[Ge]` nhỏ nhất
`->bb C`
(Trả lời bởi 2611)
Bài tập 2 (SGK Chân trời sáng tạo trang 48)
Bốn nguyên tố D, E, M, Q cùng thuộc một nhóm A trong bảng tuần hoàn, có số hiệu nguyên tử lần lượt là 9, 17, 35, 53. Các nguyên tố này được sắp xếp theo chiều tính phi kim tăng dần theo dãy nào sau đây?
A. D, Q, E, M
B. Q, M, E, D
C. D, E, M, Q
D. D, M, E, Q
Thảo luận (1)Hướng dẫn giải`4` nguyên tố `D,E,M,Q` cùng thuộc nhóm `A` và có `Z` lần lượt là `9;17;35;53`
Mà ở mỗi nhóm thì tính phi kim giảm dần từ trên xuống dưới
`=>` Tính phi kim: `D > E > M > Q`
`->bb B`
(Trả lời bởi 2611)
Bài tập 3 (SGK Chân trời sáng tạo trang 48)
Xét ba nguyên tố có cấu hình electron lần lượt:X: 1s22s22p63s1Y: 1s22s22p63s2Z: 1s22s22p63s23p1Tính tăng dần của hydroxide làA. XOH Q(OH)2 Z(OH)3B. Z(OH)3 XOH Q(OH)2C. Z(OH)3 Q(OH)2 XOHD. XOH Z(OH)3 Q(OH)2
Đọc tiếp
Xét ba nguyên tố có cấu hình electron lần lượt:
X: 1s22s22p63s1
Y: 1s22s22p63s2
Z: 1s22s22p63s23p1
Tính tăng dần của hydroxide là
A. XOH < Q(OH)2 < Z(OH)3
B. Z(OH)3 < XOH < Q(OH)2
C. Z(OH)3 < Q(OH)2 < XOH
D. XOH < Z(OH)3 < Q(OH)2
Thảo luận (1)Hướng dẫn giải- X: 1s22s22p63s1: nhóm IA, chu kì 3
- Q: 1s22s22p63s2: nhóm IIA, chu kì 3
- Z: 1s22s22p63s23p1: nhóm IIIA, chu kì 3
- Trong cùng 1 chu kì, đi từ trái sang phải, tính base của hydroxide giảm dần
=> Z(OH)3 < Q(OH)2 < XOH
Đáp án C
(Trả lời bởi Mai Trung Hải Phong)
Bài tập 4 (SGK Chân trời sáng tạo trang 48)
Trong bảng tuần hoàn các nguyên tố hóa học, cho biết nguyên tố nào có tính phi kim mạnh nhất. Giải thích.
Thảo luận (1)Hướng dẫn giảiNguyên tố có tính phi kim mạnh nhất là `F`
Vì (không xét trường hợp của khí hiếm)
- Ở mỗi chu kì tính phi kim tăng dần từ trái qua phải `(1)`
- Ở mỗi nhóm tính phi kim giảm dần từ trên xuống dưới `(2)`
Từ `(1);(2)=>F` có tính phi kim mạnh nhất.
(Trả lời bởi 2611)
Bài tập 5 (SGK Chân trời sáng tạo trang 48)
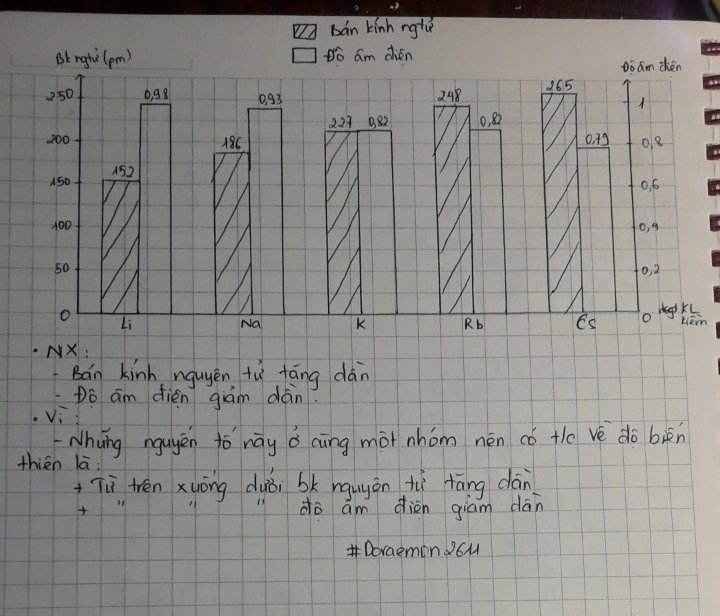
Cho bảng số liệu sau:
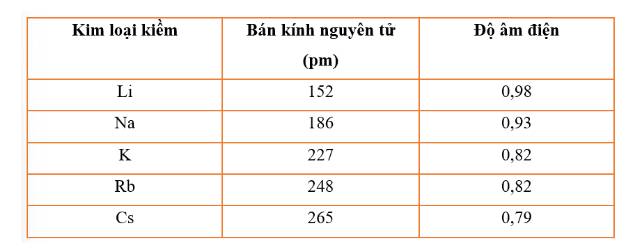
Hãy vẽ đồ thị hoặc biểu đồ với hai đại lượng bán kính nguyên tử và độ âm điện trong bảng số liệu trên. Quan sát và cho biết hai đại lượng này biến thiên như thế nào? Giải thích.
Thảo luận (1)Hướng dẫn giải