Hệ số nhiệt độ Van’t Hoff là tỉ số giữa tốc độ phản ứng tại nhiệt độ T và T+10 nên giá trị càng lớn thì ảnh hưởng của nhiệt độ đến phản ứng càng mạnh.
Bài 19: Tốc độ phản ứng
Đúng 1
Bình luận (0)
Các câu hỏi tương tự
Ở 20 oC, tốc độ một phản ứng là 0,05 mol/(L.min). Ở 30oC, tốc độ phản ứng này là 0,15 mol/(L.min).
a) Hãy tính hệ số nhiệt độ Van’t Hoff của phản ứng trên.
b) Dự đoán tốc độ phản ứng trên ở 40oC (giả thiết hệ số nhiệt độ γ trong khoảng nhiệt độ này không đổi).
Cho phản ứng của các chất ở thể khí: X + Y → XYBiết tốc độ phản ứng tỉ lệ thuận với nồng độ các chất tham gia và phản ứng với số mũ là hệ số tỉ lượng của chất đó trong phương trình hóa học.a) Hãy viết phương trình tốc độ của phản ứng này.b) Ở một nhiệt độ xác định, hằng số tốc độ của phản ứng này là 2,5.10-4L/(mol.s).Nồng độ đầu của X và Y lần lượt là 0,02 M và 0,03 M. Hãy tính tốc độ phản ứng:- Tại thời điểm đầu.- Tại thời điểm đã hết một nửa lượng X.
Đọc tiếp
Cho phản ứng của các chất ở thể khí: X + Y → XY
Biết tốc độ phản ứng tỉ lệ thuận với nồng độ các chất tham gia và phản ứng với số mũ là hệ số tỉ lượng của chất đó trong phương trình hóa học.
a) Hãy viết phương trình tốc độ của phản ứng này.
b) Ở một nhiệt độ xác định, hằng số tốc độ của phản ứng này là 2,5.10-4L/(mol.s).
Nồng độ đầu của X và Y lần lượt là 0,02 M và 0,03 M. Hãy tính tốc độ phản ứng:
- Tại thời điểm đầu.
- Tại thời điểm đã hết một nửa lượng X.
Hãy giải thích tại sao khi nhiệt độ tăng thì tốc độ phản ứng tăng.
Nêu mối liên hệ giữa nồng độ và áp suất của khí trong hỗn hợp.
Giải thích được tại sao nhiều phản ứng hoá học trong công nghiệp cần tiến hành ở nhiệt độ cao và sử dụng chất xúc tác.
Nghiên cứu ảnh hưởng của nhiệt độ đến tốc độ phản ứng:Mg + 2H2O → Mg(OH)2 + H2Chuẩn bị: Mg dạng phôi bào, dung dịch phenolphthalein, nước cất, 2 ống nghiệm, đèn cồn, kẹp gỗ.Tiến hành:Cho vào mỗi ống nghiệm khoảng 3 mL nước cất.Nhỏ vào mỗi ống nghiệm 1 – 2 giọt phenolphthalein và cho vào mỗi ống 1 mẫu phoi bào Mg.Đun nóng 1 ống nghiệm.Lưu ý: Làm sạch bề mặt Mg trước khi tiến hành thí nghiệm.Quan sát và trả lời câu hỏi:1. Sự thay đổi màu sắc trong ống nghiệm nào nhanh hơn?2. Nhiệt độ ảnh hưởng nh...
Đọc tiếp
Nghiên cứu ảnh hưởng của nhiệt độ đến tốc độ phản ứng:
Mg + 2H2O → Mg(OH)2 + H2
Chuẩn bị: Mg dạng phôi bào, dung dịch phenolphthalein, nước cất, 2 ống nghiệm, đèn cồn, kẹp gỗ.
Tiến hành:
Cho vào mỗi ống nghiệm khoảng 3 mL nước cất.
Nhỏ vào mỗi ống nghiệm 1 – 2 giọt phenolphthalein và cho vào mỗi ống 1 mẫu phoi bào Mg.
Đun nóng 1 ống nghiệm.
Lưu ý: Làm sạch bề mặt Mg trước khi tiến hành thí nghiệm.
Quan sát và trả lời câu hỏi:
1. Sự thay đổi màu sắc trong ống nghiệm nào nhanh hơn?
2. Nhiệt độ ảnh hưởng như thế nào đến tốc độ phản ứng?
Xét phản ứng H2 + Cl2 → 2HCl
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị sau:
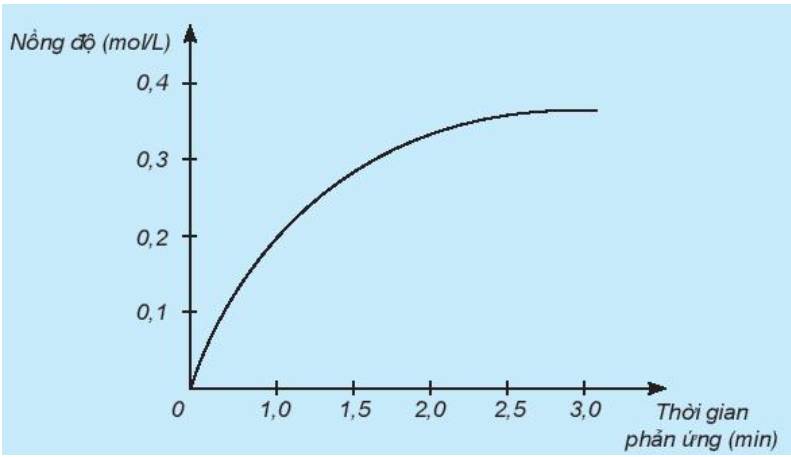 a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
b) Nêu đơn vị của tốc độ phản ứng trong trường hợp này.
Cho phản ứng của các chất ở thể khí:
2NO + 2H2 → N2 + 2H2O
Hãy viết biểu thức tính tốc độ trung bình theo sự biến đổi nồng độ chất đầu và chất sản phẩm của phản ứng trên.
Yếu tố nào đã được áp dụng để làm thay đổi tốc độ của các phản ứng trong Hình 19.7?






