Đây là phiên bản do Thảo Phương
đóng góp và sửa đổi vào 10 tháng 7 2021 lúc 21:47. Xem phiên bản hiện hành
Bài 3: Sự điện li của H2O - pH - Chất chỉ thị axit-bazo
Nội dung lý thuyết
Các phiên bản khác
0
2 gp
1. Tóm tắt lý thuyết
1.1. Nước là chất điện li rất yếu
a. Sự điện li của nước
- Nước là chất điện rất yếu.
- Phương trình điện li: H2O ⇔ H+ + OH-
b. Tích số ion của nước
- Ở 25OC, hằng số KH2O gọi là tích số ion của nước.
KH2O = [H+]. [OH -] = 10-14
→ [H+] = [OH -] = 10-7
- Nước là môi trường trung tính, nên môi trường trung tính là môi trường trong đó [H+] = [OH] = 10-7
c. Ý nghĩa tích số ion của nước
*Trong môi trường axit
Ví dụ: Tính [H+] và [OH -] của dung dịch HCl 10-3 M.
HCl → H+ + Cl-
10-3 M → 10-3 M
⇒ [H+] = [HCl] = 10-3 M
⇒
⇒ [H+] > [OH-] hay [H+] >10-7 M.
*Trong môi trường bazơ
Ví dụ: Tính [H+] và [OH-] của dung dịch NaOH 10-5 M
NaOH → Na+ + OH-
10-5 M → 10-5 M
⇒ [OH-] = [NaOH] = 10-5 M
⇒
⇒ [OH-] > [H+]
* Kết luận
Vậy [H+] là đại lượng đánh giá độ axít, độ bazơ của dung dịch.
Mt trung tính: [H+] = 10-7 M
Mt bazơ : [H+] <10-7 M
Mt axít: [H+] > 10-7 M
1.2. Khái niệm về pH, chất chỉ thị axit bazơ
a. Khái niệm pH
Dung dịch được sử dụng nhiều thường có [H+] trong khoảng 10 -1 à 10-14 M. Để tránh ghi giá trị [H+] với số mũ âm, người ta dùng pH.
Công thức: [H+] = 10-pH M hay pH= -lg [H+]
Nếu [H+] = 10-a M thì pH = a
Ví dụ:
[H+] = 10-3 M ⇒ pH=3 môi trường axít
[H+] = 10-11 M ⇒ pH = 11: môi trường bazơ
[H+]= 10-7 M ⇒ pH = 7 :môi trường trung tính.
b. Chất chỉ thị Axit - bazơ
- Là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch
- Ví dụ: Quỳ tím, phenolphtalein
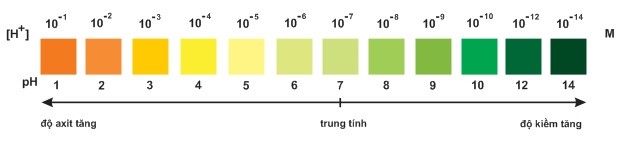
(Màu của chất chỉ thị vạn năng)
2.Bài tập trắc nghiệm
Câu 1: Trộn V1 ml dung dịch NaOH có pH = 13 với V2 ml dung dịch Ba(OH)2 có pH = 11, thu được dung dịch mới có pH = 12. Tỉ số V1 : V2 có giá trị là
A. 1/1
B. 2/1
C. 1/10
D. 10/1
Câu 2: Trộn V1 lít dung dịch H2SO4 có pH = 3 với 2 lít dung dịch NaOH có pH = 12, thu được dung dịch mới cố pH = 4. Tỉ số V1 : V2 có giá trị là
A. 8/1
B. 101/9
C. 10/1
D. 4/1
Câu 3: Trộn hai dung dịch Ba(HCO3)2 và NaHSO4 có cùng nồng độ mol với nhau theo tỉ lệ thể tích 1 : 1 thu được kết tủa và dung dịch. Bỏ qua sự thủy phân của các ion và sự điện li của nước, các ion có mặt trong dung dịch Y là
A. Na+ và SO42-
B. Ba2+, HCO32- và Na+
C. Na+, HCO32-
D. Na+, HCO32- và SO42-
Câu 4: Cho các dung dịch HCl, H2SO4 và CH3COOH có cùng giá trị pH. Sự sắp xếp nào sau đây đúng với giá trị nồng độ mol của các dung dịch trên?
A. HCl < H2SO4 < CH3COOH
B. H2SO4 < HCl < CH3COOH
C. H2SO4 < CH3COOH < HCl
D. CH3COOH < HCl < H2SO4
Câu 5: Chỉ dùng quỳ tím, có thể nhận biết ba dung dịch riêng biệt nào sau đây?
A. HCl, NaNO3, Ba(OH)2
B. H2SO4, HCl,KOH.
C. H2SO4, NaOH, KOH
D. Ba(OH)2, NaCl, H2SO4
Câu 6: Chọn câu trả lời đúng, khi nói về muối axit:
A. Dung dịch muối có pH < 7.
B. Muối có khả năng phản ứng với bazơ.
C. Muối vẫn còn hiđro trong phân tử.
D. Muối mà gốc axit vẫn còn hiđro có khả năng phân li tạo proton trong nước.
Câu 7: Cho 10 ml dung dịch X chứa HCl 1M và H2SO4 0,5M. thể tích dung dịch NaOH 1M cần để trung hòa dung dịch X là
A. 10 ml.
B. 15 ml.
C. 20 ml.
D. 25 ml.
Câu 8: Dung dịch A có chứa 5 ion :Mg2+ ,Ba2+ ,Ca2+ và 0,1 mol Cl- và 0,2 mol NO3. Thêm dần V ml dung dịch K2CO3 1M vào dung dịch A đến khi thu được lượng kết tủa lớn nhất. V có giá trị là
A. 150 ml.
B. 300 ml.
C. 200 ml.
D. 250 ml.
Câu 9: Trộn 200 ml dung dịch gồm HCl 0,1M và H2SO4 0,15M với 300 ml dung dịch Ba(OH)2 nồng độ aM, thu được m gam kết tủa và 500 ml dung dịch có pH = 1. Giá trị của a và m lần lượt là
A. 0,15 và 2,330
B. 0,10 và 6,990.
C. 0,10 và 4,660
D. 0.05 và 3,495
Câu 10: Cho 300 ml dung dịch chứa H2SO4 0,1M, HNO3 0,2M và HCl 0,3M tác dụng với V ml dung dịch NaOH 0,2 M và KOH 0,29M thu được dung dịch có pH = 2. Giá trị của V là
A. 134.
B. 147.
C. 114.
D. 169.
Đáp án Câu hỏi trắc nghiệm Hóa học 11
| 1 | C | 2 | B | 3 | C | 4 | B | 5 | A | 6 | D |
| 7 | C | 8 | A | 9 | D | 10 | A |
Câu 3: Ba(HCO3)2 + NaHSO4 → BaSO4 ↓ + NaHCO3 + CO2 ↑ + H2O
Vậy sau phản ứng, trong dung dịch còn lại Na+ và
Câu 7: H+ + OH- → H2O
Ta có: => V = 20 ml.
Câu 8: Khi thêm K2CO3 vào dung dịch A, khi lượng kết tủa thu được là lớn nhất tức là toàn bộ Mg2+, Ba2+, Ca2+ đã kết tủa, trong dung dịch còn lại KCl và KNO3
=> nK+ = nCl- = nNO3- = 0,3 mol
=> nK2CO3 = 0,15 mol
=> VK2CO3 = 150 ml
Câu 9: Sau phản ứng trung hòa pH = 1 => H+ dư
H+ + OH- → H2O
nH+bd = 0,08 mol; sau phản ứng pH = 1
=> nH+ sau p/ư = 0,05 mol
nH+p/ư = nOH- = 0,03 mol
=> nBa(OH)2 = 0,015 mol
=> CM Ba(HCO3)2 = 0,05 (mol/l)
nBaSO4 = nBa(OH)2 = 0,015 mol (H2SO4 dư) => mBaSO4 = 3,495g
Câu 10: Coi 300 ml dung dịch A gồm 100 ml H2SO4 0,1M 100 ml HNO3 0,2M và 100 ml HCl 0,3M trộn lại với nhau.
Vậy:
Phản ứng của dung dịch A và B là: H+ + OH- → H2O
nH+ p/ư = nOH- = 0,049.0,001V => nH+ p/ư = 0,01 (0,3 + 0,001V)
=> 0,07 = 0,49.0,001V + 0,010,3 + 0,001V) => V = 134 ml
Danh sách các phiên bản khác của bài học này. Xem hướng dẫn