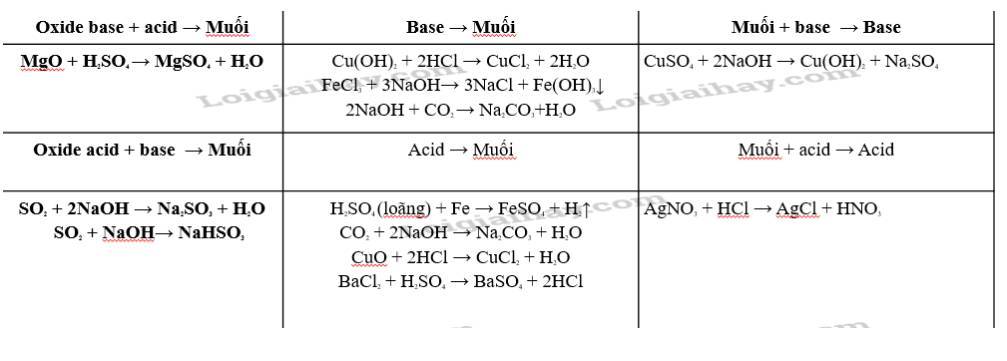
nhận dạng công thức hoá học base tan và base ko tan

Những câu hỏi liên quan
Dựa vào bảng tính tan dưới đây, hãy cho biết những base nào là base không tan và những base nào là base kiềm? Viết công thức hoá học và đọc tên các base có trong bảng.
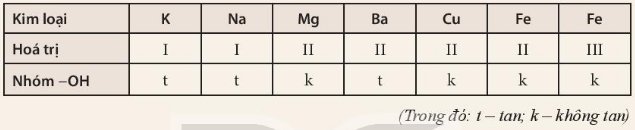
Base không tan:
Mg(OH)2: magnesium hydroxide.
Cu(OH)2: copper(II) hydroxide.
Fe(OH)3: iron(III) hydroxide.
Fe(OH)2: iron(II) hydroxide.
Base kiềm
KOH: potassium hydroxide.
Ba(OH)2:barium hydroxide
NaoOH:sodium hydroxide
Đúng 2
Bình luận (0)
Tìm hiểu khái niệm baseBảng 9.1. Tên một số base thông dụng, công thức hoá học và dạng tồn tại của base trong dung dịchQuan sát Bảng 9.1 và thực hiện các yêu cầu:1. Công thức hoá học của các base có đặc điểm gì giống nhau?2. Các dung dịch base có đặc điểm gì chung?3. Thảo luận nhóm và đề xuất khái niệm về base.4. Em hãy nhận xét về cách gọi tên base và đọc tên base Ca(OH)2.
Đọc tiếp
Tìm hiểu khái niệm base
Bảng 9.1. Tên một số base thông dụng, công thức hoá học và dạng tồn tại của base trong dung dịch
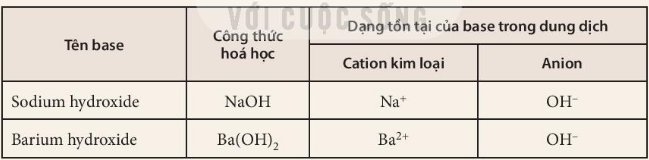
Quan sát Bảng 9.1 và thực hiện các yêu cầu:
1. Công thức hoá học của các base có đặc điểm gì giống nhau?
2. Các dung dịch base có đặc điểm gì chung?
3. Thảo luận nhóm và đề xuất khái niệm về base.
4. Em hãy nhận xét về cách gọi tên base và đọc tên base Ca(OH)2.
1. Có một hay nhiều nhóm OH-
2. Các dung dịch base gồm 1 cation kim loại và anion OH-
3. Base là những hợp chất trong phân tử có nguyên tử kim loại liên kết với nhóm hydroxide. Khi tan trong nước, base tạo ra ion OH-
4. Quy tắc gọi tên các base: Tên kim loại (kèm hoá trị đối với kim loại có nhiều hoá trị) + hydroxide.
Tên base Ca(OH)2: Calcium hydroxide.
Đúng 0
Bình luận (0)
Câu 1 tính tan của muối.Câu 2 nhận dạng loại phân bón hoá học từ công thức hóa học.Câu 3 nêu những kim loại dẫn điện tốt .Câu 4 ý nghĩa dãy hoạt động hoá học .Câu 5. Tính chất hoá học của kim loại .Câu 6. Tính chất hoá học của nhôm .Câu 7. Tính chất hoá học của sắt .Câu 8. Trong điều kiện thường, các phi kim tồn tại ở trạng thái khí có công thức hóa học là gì .Câu 9. Hiện tượng quan sát được khi nhúng giấy quỳ tím vào dung dịch nước chlorine là gì
Đọc tiếp
Câu 1 tính tan của muối.
Câu 2 nhận dạng loại phân bón hoá học từ công thức hóa học.
Câu 3 nêu những kim loại dẫn điện tốt .
Câu 4 ý nghĩa dãy hoạt động hoá học .
Câu 5. Tính chất hoá học của kim loại .
Câu 6. Tính chất hoá học của nhôm .
Câu 7. Tính chất hoá học của sắt .
Câu 8. Trong điều kiện thường, các phi kim tồn tại ở trạng thái khí có công thức hóa học là gì .
Câu 9. Hiện tượng quan sát được khi nhúng giấy quỳ tím vào dung dịch nước chlorine là gì
Câu 1: Để tính tan của một muối, cần biết công thức hóa học của muối đó và thông tin về độ tan của muối trong nước. Độ tan của muối được biểu thị bằng số gam muối tan trong một lượng nước nhất định. Ví dụ, nếu muối A có công thức hóa học là AB và độ tan của nó là 10g trong 100ml nước, ta có thể nói rằng muối A có độ tan là 10g/100ml.
Câu 2: Để nhận dạng loại phân bón hoá học từ công thức hóa học, cần xem xét các nguyên tố và tỷ lệ phần trăm của chúng trong công thức. Ví dụ, nếu công thức hóa học là NPK 15-15-15, ta biết rằng phân bón này chứa các nguyên tố Nitơ (N), Phốtpho (P) và Kali (K) với tỷ lệ phần trăm là 15-15-15.
Câu 3: Một số kim loại dẫn điện tốt bao gồm đồng (Cu), nhôm (Al), sắt (Fe), kẽm (Zn), và bạc (Ag). Những kim loại này có khả năng dẫn điện tốt do có cấu trúc tinh thể đặc biệt cho phép dòng điện chạy qua chúng dễ dàng.
Câu 4: Dãy hoạt động hoá học là một danh sách các nguyên tố hoặc hợp chất được sắp xếp theo thứ tự giảm hoạt tính hoá học. Dãy này cho phép dự đoán được khả năng oxi-hoá hay khử của các chất trong các phản ứng hoá học.
Câu 5: Tính chất hoá học của kim loại bao gồm khả năng tạo ion dương, khả năng dẫn điện, tính khử, tính oxi-hoá, tính tan trong axit, tính phản ứng với nước và các chất khác.
Câu 6: Nhôm là một kim loại nhẹ, có tính chất khá bền, không bị ăn mòn bởi không khí. Nhôm có khả năng tạo ion Al^3+ trong dung dịch axit, có khả năng tạo oxit nhôm (Al2O3) khi tiếp xúc với không khí.
Câu 7: Sắt là một kim loại có tính chất từ tính, có khả năng tạo ion Fe^2+ và Fe^3+ trong dung dịch axit. Sắt có khả năng oxi-hoá thành oxit sắt (Fe2O3) khi tiếp xúc với không khí và nước.
Câu 8: Trong điều kiện thường, các phi kim tồn tại ở trạng thái khí. Ví dụ, oxi (O2), nitơ (N2), hidro (H2), fluơ (F2), clo (Cl2) đều tồn tại ở trạng thái khí.
Câu 9: Hiện tượng quan sát được khi nhúng giấy quỳ tím vào dung dịch là thay đổi màu của giấy quỳ tím. Nếu dung dịch có tính axit, giấy quỳ tím sẽ chuyển sang màu đỏ. Nếu dung dịch có tính kiềm, giấy quỳ tím sẽ chuyển sang màu xanh.
Đúng 0
Bình luận (0)
1) Hãy trình bày phương pháp hóa học nhận biết các dung dịch sau: HCl, Ca(NO3)2, HNO3, BaCl2. Viết phương trình hóa học xảy ra trong quá trình nhận biết.
2)Từ những chất có sẵn là K, NaCl, H2O và các dung dịch CuCl2, Fe2(SO4)3, hãy viết các phương trình hóa học điều chế:
a/ 2 base tan b/ 2 base không tan
Bài 1:
- Thử với lượng nhỏ mỗi chất.
- Cho quỳ tím vào các mẫu thử, quan sát:
+) Qùy tím hóa đỏ => dd HCl và dd HNO3 => Nhóm (I)
+) Qùy tím không đổi màu => dd Ca(NO3)2 và dd BaCl2 => Nhóm (II)
- Cho vài giọt dd AgNO3 vào các mẫu thử nhóm (I), quan sát:
+) Có xuất hiện kết tủa trắng => Kết tủa đó là AgCl. => Mẫu thử ban đầu là dd HCl.
PTHH: HCl + AgNO3 -> AgCl (trắng) + HNO3
+) Không có kết tủa trắng => Mẫu thử ban đầu là dd HNO3.
- Cho vài giọt dd H2SO4 vào nhóm (II), quan sát:
+) Có xuất hiện kết tủa trắng => Kết tủa đó là BaSO4 => Mẫu thử ban đầu là dd BaCl2.
PTHH: BaCl2 + H2SO4 -> BaSO4 (trắng) + 2 HCl
+) Không xuất hiện kết tủa trắng => Mẫu thử ban đầu là dd Ca(NO3)2
Đúng 0
Bình luận (0)
Cho các chất: NaOH, KCl, HCl, HNO3, Cu(OH)2, Fe(OH)3, MgSO4, H2SO4, KOH, Ba(OH)2, C2H5OH, Mg(OH)2. (a) Cho biết trong các chất trên, chất nào là base tan? Chất nào là base không tan? (b) Gọi tên các base trên.
Cần lưu ý nhé: HCl, HNO3 và H2SO4 là axit chứ không phải là bazơ, KCl mang tính trung tính vì là chất này được tạo từ cả bazơ mạnh lẫn axit mạnh. C2H5OH là chất điện li nên cũng không phải là bazơ
a)
- Những chất là bazơ tan:
+ NaOH
+ KOH
+ Ba (OH)2
- Những chất là bazơ không tan:
+ Cu(OH)2
+ Fe(OH)3
+ Mg(OH)2
b)
NaOH: Natri Hidroxide
KCl: Kali Clohidric
HCl: Axit Clohidric
HNO3: Axit Nitric
Cu (OH)2: Đồng (II) Hidroxide
Fe(OH)3: Sắt (III) Hidroxide
MgSO4: Magiê Surfuric
H2SO4: Axit Surfuric
KOH: Kali Hidroxide
Ba(OH)2: Bari Hidroxide
C2H5OH: Ancol Etylic
Mg(OH)2: Magiê Hidroxide
#HT
Đúng 1
Bình luận (0)
Viết phương trình hoá học minh hoạ cho tính chất hoá học của oxide base và oxide acid. Lấy magnesium oxide và sulfur dioxide làm ví dụ.
- Tính chất hoá học của oxide base:
+ Tác dụng với oxide acid: MgO + CO2 -> MgCO3
+ Tác dụng với dung dịch acid: MgO + 2HCl -> MgCl2 + H2O
+ Tác dụng với nước tạo dung dịch base: MgO là oxide base không tan nên không có phản ứng với nước.
- Tính chất hoá học của oxide acid:
+ Tác dụng với oxide base: SO2 + K2O -> K2SO3
+ Tác dụng với dung dịch base: SO2 + 2 KOH -> K2SO3 + H2O
+ Tác dụng với nước tạo dung dịch acid: \(SO_2+H_2O⇌H_2SO_3\)
Đúng 0
Bình luận (0)
vẽ sơ đồ tư duy về các hợp chất vô cơ gồm acid, base,oxide,muối(chia thành nhiều nhánh gồm khái niệm, cách gọi tên, tính chất hóa học , ứng dụng . riêng base có thwm thang pH. oxide có thêm Phân loại. muối có thêm tính tan
Xem chi tiết
Cho các base: NaOH, Mg(OH)2, Cu(OH)2, KOH, Fe(OH)2, Fe(OH)3, Ba(OH)2, Ca(OH)2. Số base không tan làA. 2. B. 3. C. 4. D. 5.
Đọc tiếp
Cho các base: NaOH, Mg(OH)2, Cu(OH)2, KOH, Fe(OH)2, Fe(OH)3, Ba(OH)2, Ca(OH)2. Số base không tan là
A. 2. B. 3. C. 4. D. 5.
Đáp án: C
Base không tan: Mg(OH)2, Cu(OH)2, Fe(OH)2, Fe(OH)3.
Đúng 0
Bình luận (0)
C. 4
\(Mg\left(OH\right)_2,Cu\left(OH\right)_2,Fe\left(OH\right)_2,Fe\left(OH\right)_3\)
Đúng 0
Bình luận (0)
Tính chất hoá học của các hợp chất vô cơ được tóm tắt bằng sơ đồ dưới đây:
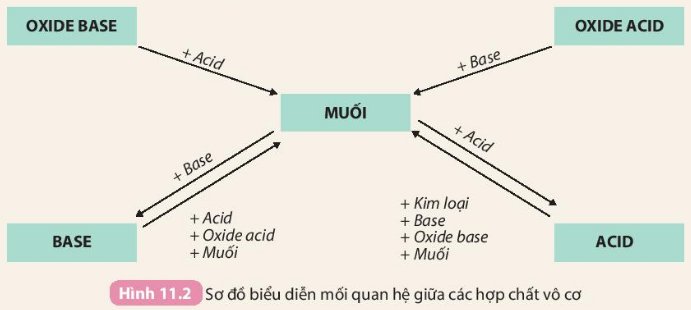
Dựa vào sơ đồ Hình 11.2 và cho biết tính chất của oxide, acid, base. Viết phương trình hoá học minh hoạ.