Trình bày cách phân biệt các dung dịch sau bằng phương pháp hoá học: ethanol, acetaldehyde, acetic acid và acrylic acid.

Những câu hỏi liên quan
Trình bày phương pháp hoá học để phân biệt các dung dịch sau: ethanol, glycerol, acetaldehyde và acetic acid.
Tham khảo
- Đánh số thứ tự cho từng dung dịch. Trích dung dịch làm mẫu thử đánh số thứ tự tương ứng.
- Nhúng mẩu quỳ tím vào các mẫu thử:
+ Mẫu thử chứa acetic acid làm quỳ tím hóa đỏ.
+ Ba mẫu thử chứa ethanol, glycerol, acetaldehyde không làm quỳ tím đổi màu.
- Tiếp tục trích mẫu thử của ba dung dịch không làm quỳ tím đổi màu.
- Cho vào mỗi mẫu thử vài giọt dung dịch copper(II) sulfate và 1 mL dung dịch sodium hydroxide, tạo kết tủa xanh lam Cu(OH)2.
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
- Lắc nhẹ các mẫu thử:
+ Mẫu thử chứa glycerol làm tan kết tủa xanh lam thành dung dịch màu xanh lam.
+ Hai mẫu thử chứa ethanol và acetaldehyde không làm tan kết tủa.
- Tiếp tục đun nóng nhẹ hai mẫu thử chứa ethanol và acetaldehyde và Cu(OH)2:
+ Mẫu thử chứa acetaldehyde xuất hiện kết tủa đỏ gạch Cu2O.
CH3CHO + 2Cu(OH)2 + NaOH CH3COONa + Cu2O + 3H2O
+ Mẫu thử không có hiện tượng là ethanol.
Đúng 0
Bình luận (0)
Trình bày cách phân biệt các dung dịch sau: acetic acid, acrylic acid, acetaldehyde.
Tham khảo
- Đánh số thứ tự cho từng dung dịch. Trích dung dịch làm mẫu thử đánh số thứ tự tương ứng.
- Nhúng mẩu quỳ tím vào các mẫu thử:
+ Mẫu thử chứa acetaldehyde không làm quỳ tím đổi màu.
+ Hai mẫu thử chứa acetic acid, acrylic acid làm quỳ tím hóa đỏ.
- Tiếp tục trích mẫu thử của hai dung dịch làm quỳ tím hóa đỏ.
- Nhỏ vài giọt nước bromine vào hai mẫu thử:
+ Mẫu thử chứa acrylic acid làm nước bromine mất màu.
+ Mẫu thử chứa acetic acid không làm nước bromine mất màu.
* Phương trình hóa học:
CH2=CH–COOH + Br2 → CH2Br – CHBr – COOH
Đúng 0
Bình luận (0)
Giúp mik nhé
Bằng phương pháp hoá học, em hãy trình bày cách phân biệt các dung dịch sau và viết PTHH minh hoạ
a) ethanol, giấm ăn, dầu ăn
b) ethanol, acetic acid, dầu dừa
C) ethanol, methane, carbonic
a, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ tím hóa hồng: giấm ăn.
+ Quỳ không đổi màu: ethanol, dầu ăn. (1)
- Hòa tan mẫu thử nhóm (1) vào nước, lắc đều.
+ Tạo dung dịch đồng nhất: ethanol.
+ Dung dịch phân lớp: dầu ăn.
- Dán nhãn.
b, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ tím hóa hồng: acetic acid.
+ Quỳ không đổi màu: athanol, dầu dừa. (1)
- Hòa tan mẫu thử nhóm (1) vào nước, lắc đều.
+ Tan tạo dd đồng nhất: ethanol.
+ Dd thu được phân lớp: dầu dừa.
- Dán nhãn/
c, - Trích mẫu thử.
- Dẫn từng mẫu thử qua Ca(OH)2.
+ Có tủa trắng: CO2.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
+ Không hiện tượng: ethanol, CH4. (1)
- Cho mẫu thử nhóm (1) pư với Na.
+ Có hiện tượng sủi bọt khí: ethanol.
PT: \(C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
+ Không hiện tượng: CH4.
- Dán nhãn.
Đúng 2
Bình luận (0)
Cho bốn hợp chất sau: ethanol, propanal, acetone, acetic acid.
a) Chất nào trong các chất trên có nhiệt độ sôi cao nhất?
b) Trình bày cách phân biệt các chất trên bằng phương pháp hoá học.
Tham khảo:
a) Trong 4 chất trên acetic acid có nhiệt độ sôi cao nhất. Do phân tử acetic acid chứa nhóm carbonyl phân cực, các phân tử carboxylic acid liên kết hydrogen với nhau tạo thành dạng dimer hoặc dạng liên phân tử.
b) Cách phân biệt: ethanol, propanal, acetone, acetic acid:
- Trích mẫu thử.
- Cho vào mỗi mẫu thử 1 mẩu quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → acetic acid (CH3COOH).
+ Quỳ tím không đổi màu → ethanol, propanal, acetone (nhóm I).
- Cho từng mẫu thử ở nhóm I tác dụng với Na:
+ Mẩu Na tan dần, có khí thoát ra → ethanol (C2H5OH).
Phương trình hoá học: 2C2H5OH + 2Na → 2C2H5ONa + H2.
+ Không hiện tượng → propanal, acetone (nhóm II).
- Cho từng mẫu thử ở nhóm II tác dụng với dung dịch bromine:
+ Dung dịch bromine nhạt dần đến mất màu → propanal.
Phương trình hoá học:
CH3 – CH2 – CHO + Br2 + H2O → CH3 – CH2 – COOH + 2HBr.
+ Không hiện tượng → acetone.
Đúng 0
Bình luận (0)
Cho biết sự thay đổi số oxi hoá của C và Br trong phương trình hoá học ở Ví dụ 4. Từ đó xác định chất oxi hoá và chất khử.
Ví dụ 4.
\(CH_3CH=O+Br_2+H_2O→CH_3COOH+2HBr\)
acetaldehyde acetic acid
\({\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 1} {\rm{H = O + }}{\mathop {{\rm{Br}}}\limits^0 _{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 3} {\rm{OOH + 2H}}\mathop {{\rm{Br}}}\limits^{ - 1} \)
Trong phản ứng trên, số oxi hoá của C (trong nhóm chức –CHO) tăng từ +1 lên +3, CH3CHO là chất oxi hóa. Số oxi hóa của Br giảm từ 0 xuống -1 , Br2 là chất oxi hóa.
Đúng 0
Bình luận (0)
Có 2 lọ đựng chất lỏng rượu etylic (c2h5oh) và acetic acid (ch3cooh). trình bày phương pháp hóa học khác nhau để phân biệt 2 chất lỏng đựng trong 2 bình trên.
Ta nhúm quỳ tím
-Quỳ chuyển đỏ là CH3COOH
-Quỳ ko chuyển màu là C2H5OH
Ta nhỏ NaOH có pha phenolpalein
-Mất màu khi nhỏ :CH3COOH
-ko hiện tượng C2H5OH
CH3COOH+NaOH->CH3COONa+H2O
Đúng 2
Bình luận (0)
Điều chế ethyl acetate bằng cách cho 6 gam acetic acid tác dụng với 5,2 gam ethanol có xúc tác là dung dịch sulfuric acid đặc và đun nóng thu được 5,28 gam ester. Tính hiệu suất của phản ứng.
\({{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = }}\frac{{\rm{6}}}{{{\rm{60}}}}{\rm{ = 0,1 (mol); }}{{\rm{n}}_{{{\rm{C}}_2}{{\rm{H}}_5}{\rm{OH}}}}{\rm{ = }}\frac{{{\rm{5,2}}}}{{46}}{\rm{ }} \approx {\rm{ 0,113 (mol)}}\)
Phương trình hóa học:
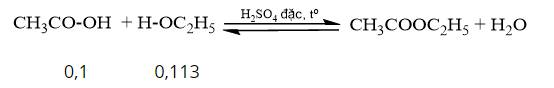
Ta có: \(\frac{{0,1}}{1} < \frac{{0,113}}{1}\) => acetic acid hết, ester tính theo acetic acid.
\(\begin{array}{l}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}}{\rm{ = }}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = 0,1 (mol) }}\\ \Rightarrow {{\rm{m}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}} = {\rm{0,1}} \times {\rm{88 = 8,8 (g)}}\\ \Rightarrow {\rm{H = }}\frac{{5,28}}{{8,8}} \times 100\% = 60\% \end{array}\)
Đúng 0
Bình luận (0)
Cho 50g dung dịch acetic acid CH3COOH tác dụng vùa đủ với 2,76 g Potassium carbonate K2CO3.
a. Tính nồng độ phần trăm dung dịch acetic acid đã dùng.
b. Nếu muốn thu được lượng acetic acid đã dùng ở trên thì càn len măn bao nhiều ml dung dịch ethanol 8 độ.
a, \(n_{K_2CO_3}=\dfrac{2,76}{138}=0,02\left(mol\right)\)
PT: \(2CH_3COOH+K_2CO_3\rightarrow2CH_3COOK+CO_2+H_2O\)
Theo PT: \(n_{CH_3COOH}=2n_{K_2CO_3}=0,04\left(mol\right)\)
\(\Rightarrow C\%_{CH_3COOH}=\dfrac{0,04.60}{50}.100\%=4,8\%\)
b, \(C_2H_5OH+O_2\underrightarrow{mengiam}CH_3COOH+H_2O\)
Theo PT: \(n_{C_2H_5OH}=n_{CH_3COOH}=0,04\left(mol\right)\Rightarrow m_{C_2H_5OH}=0,04.46=1,84\left(g\right)\)
\(\Rightarrow V_{C_2H_5OH}=\dfrac{1,84}{0,8}=2,3\left(ml\right)\)
\(\Rightarrow V_{C_2H_5OH\left(8^o\right)}=\dfrac{2,3}{8}.100=28,75\left(ml\right)\)
Đúng 4
Bình luận (0)
Đun hỗn hợp methanol và ethanol với dung dịch sulfuric acid đặc ở nhiệt độ thích hợp thì thu được những ether nào? Viết phương trình hoá học của các phản ứng xảy ra.
CH3OH \(\underrightarrow{H_2SO_{4đ}}\) CH3-O-CH3 + H2O
2C2H5OH \(\underrightarrow{H_2SO_{4đ}}\) C2H5-O-C2H5 + H2O
CH3OH + C2H5OH\(\underrightarrow{H_2SO_{4đ}}\) CH3-O-C2H5 + H2O
Đúng 0
Bình luận (0)












