Dựa vào bảng tính tan dưới đây, hãy cho biết những base nào là base không tan và những base nào là base kiềm? Viết công thức hoá học và đọc tên các base có trong bảng.
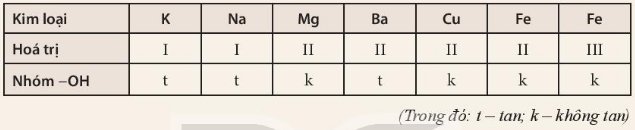
Dựa vào bảng tính tan, cho biết những base nào dưới đây là kiềm: KOH, Fe(OH)2, Ba(OH)2, Cu(OH)2.
Các base kiềm là: \(KOH,Ba\left(OH\right)_2\)
Tìm hiểu khái niệm base
Bảng 9.1. Tên một số base thông dụng, công thức hoá học và dạng tồn tại của base trong dung dịch
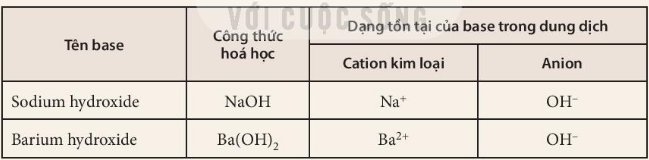
Quan sát Bảng 9.1 và thực hiện các yêu cầu:
1. Công thức hoá học của các base có đặc điểm gì giống nhau?
2. Các dung dịch base có đặc điểm gì chung?
3. Thảo luận nhóm và đề xuất khái niệm về base.
4. Em hãy nhận xét về cách gọi tên base và đọc tên base Ca(OH)2.
1. Có một hay nhiều nhóm OH-
2. Các dung dịch base gồm 1 cation kim loại và anion OH-
3. Base là những hợp chất trong phân tử có nguyên tử kim loại liên kết với nhóm hydroxide. Khi tan trong nước, base tạo ra ion OH-
4. Quy tắc gọi tên các base: Tên kim loại (kèm hoá trị đối với kim loại có nhiều hoá trị) + hydroxide.
Tên base Ca(OH)2: Calcium hydroxide.
nhận dạng công thức hoá học base tan và base ko tan
1. Bazơ tan: Là loại bazơ hoàn toàn tan trong nước, tạo ra các hydroxide (OH-) trong dung dịch.
VD: NaOH , KOH
2. Bazơ không tan: Là loại bazơ không hoàn toàn tan trong nước, chỉ tan một phần nhỏ và tạo ra các hydroxide (OH-) trong dung dịch.
VD: Ca(OH)2 , Ba(OH)2
Base tan là các base bị hòa tan trong nước, chỉ có 5 base tan là \(KOH;Ba\left(OH\right)_2;NaOH;Ca\left(OH\right)_2LiOH\)
Base không tan là các base không bị hòa tan trong nước, khác 5 base trên
Cho các chất: NaOH, KCl, HCl, HNO3, Cu(OH)2, Fe(OH)3, MgSO4, H2SO4, KOH, Ba(OH)2, C2H5OH, Mg(OH)2. (a) Cho biết trong các chất trên, chất nào là base tan? Chất nào là base không tan? (b) Gọi tên các base trên.
Cần lưu ý nhé: HCl, HNO3 và H2SO4 là axit chứ không phải là bazơ, KCl mang tính trung tính vì là chất này được tạo từ cả bazơ mạnh lẫn axit mạnh. C2H5OH là chất điện li nên cũng không phải là bazơ
a)
- Những chất là bazơ tan:
+ NaOH
+ KOH
+ Ba (OH)2
- Những chất là bazơ không tan:
+ Cu(OH)2
+ Fe(OH)3
+ Mg(OH)2
b)
NaOH: Natri Hidroxide
KCl: Kali Clohidric
HCl: Axit Clohidric
HNO3: Axit Nitric
Cu (OH)2: Đồng (II) Hidroxide
Fe(OH)3: Sắt (III) Hidroxide
MgSO4: Magiê Surfuric
H2SO4: Axit Surfuric
KOH: Kali Hidroxide
Ba(OH)2: Bari Hidroxide
C2H5OH: Ancol Etylic
Mg(OH)2: Magiê Hidroxide
#HT
So sánh được tính acid và base của các oxide và hydroxide dựa vào vị trí nguyên tố tạo nên chúng trong bảng tuần hoàn nguyên tố hóa học.
Để so sánh được tính acid và base của các oxide và hydroxide dựa vào vị trí nguyên tố tạo nên chúng trong bảng tuần hoàn nguyên tố hóa học cần ghi nhớ:
- Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, đồng thời tính acid của chúng tăng dần.
giúp mình với mai mình phải nộp rồi
Câu 44. Trong số các base sau đây, base nào sau đây không tan trong nước?
A. KOH B. Fe(OH)2. C. Ba(OH)2. D. NaOH.
Câu 45. Dãy các chất tác dụng được với dung dịch H2SO4 loãng tạo thành sản phẩm có chất khí?
A. Zn, Fe2O3, Na2SO3. B. BaO, Fe, CaCO3.
C. Al, MgO, KOH. D. Na2SO3, CaCO3, Zn.
Câu 46. Dãy gồm các kim loại đều tác dụng được với dung dịch HCl là:
A. Cu, Pb, Ag. B. Fe, Au, Cr. C. Cu, Fe, Al. D. Fe, Mg, Al.
Câu 47. Canxicacbonat được dùng sản xuất vôi, thủy tinh, xi măng. Công thức của nó là:
A. CaCl2. B. CaCO3. C. Ca(OH)2. D. CaO.
Câu 48. Chất phản ứng được với dung dịch HCl tạo ra một chất khí có mùi hắc, nặng hơn không khí và làm đục nước vôi trong?
A. Zn. B. Na2SO3. C. FeS. D. Na2CO3.
Câu 49. Chất làm quỳ tím hóa xanh là?
A. Na2SO4. B. NaOH. C. HCl. D. NaCl.
Câu 50. Cho dung dịch hydrochloric acid (HCl) tác dụng với muối (K2SO3) thu được khí nào sau đây?
A. Khí sulfur đioxide (SO2). B. Khí sulfur trioxide (SO3).
C. Khí hydrogen (H2). D. Khí oxygen (O2).
Câu 51. Phần trăm về khối lượng của nguyên tố N trong (NH2)2CO là:
A. 32,33%. B. 31,81%. C. 46,67%. D. 63,64%.
Câu 52. Thuốc thử dùng để nhận biết HCl và H2SO4 là:
A. AgNO3. B. BaCl2.
C. Quỳ tím. D. Phenolphthalein.
Câu 53. Cho hai dung dịch hydrochloric acid (HCl) và sulfuric acid (H2SO4) loãng. Thuốc thử dùng để phân biệt hai dung dịch trên là:
A. Dung dịch (Na2CO3). B. Dung dịch (NaOH).
C. (Fe(OH)2). D. Dung dịch (BaCl2).
Câu 54. Dãy các base bị nhiệt phân huỷ tạo thành basic oxide tương ứng và nước là:
A. Cu(OH)2; Zn(OH)2; Al(OH)3; Mg(OH)2. B. Cu(OH)2; Zn(OH)2; Al(OH)3; NaOH.
C. Fe(OH)3; Cu(OH)2; KOH; Mg(OH)2. D. Fe(OH)3; Cu(OH)2; Ba(OH)2; Mg(OH)2.
Câu 55. Oxide của một nguyên tố hóa trị (II) chứa 28,57% oxi về khối lượng. Nguyên tố đó là:
A. Ca. B. Mg. C. Fe. D. Cu.
Câu 56. Cặp chất tác dụng với nhau tạo thành sản phẩm có chất khí:
A. Bari clorua và Axit sulfuric loãng. B. Bải oxit và Axit sulfuric loãng.
C. Bải hdroxit và Acid sulfuric loãng. D. Bari cabonat và Axit sulfuric loãng.
Câu 57. Cho 100 ml dung dịch BaCl2 1M tác dụng vừa đủ 100 ml dung dịch K2CO3. Nồng độ mol của chất tan trong dung dịch thu được sau phản ứng là:
A. 0,1M. B. 1M. C. 2M. D. 0,2M.
Câu 58. Trộn lẫn một dung dịch có chứa 34 gam AgNO3 với một dung dịch chứa 17,55 gam NaCl. Khối lượng kết tủa thu được là:
A. 28,8 gam. B. 28,7 gam. C. 27,8 gam. D. 27 gam.
Câu 59. Để phân biệt hai dung dịch HCl và H2SO4 loãng ta có thể sử dụng dung dịch:
A. MgCl2. B. KCl. C. NaCl. D. BaCl2.
Câu 60. Sodium carbonate là hóa chất quan trọng trong công nghiệp thủy tinh, bột giặt, phẩm nhuộm, giấy, sợi. Công thức của natri carbonat là:
A. CaCO3. B. Na2CO3. C. NaHCO3. D. MgCO3.
Câu 61. Cho phương trình phản ứng Na2CO3 + 2HCl → 2NaCl + X + H2O. X là:
A. Cl2 B. CO C. CO2 D. H2
Câu 62. Một oxit của lưu huỳnh có thành phần phần trăm của O bằng 50%. Công thức hoá học của oxide là:
A. SO2. B. SO. C. SO3. D. SO3.
Câu 63. Fe(OH)2 có màu gì?
A. xanh lam. B. trắng xanh. C. trắng. D. nâu đỏ.
Câu 64. Phân superphosphate kép thực tế sản xuất được thường chỉ có 40% P2O5. Vậy % khối lượng Ca(H2PO4)2 trong phân bón đó là:
A. 56,94%. B. 65,92%. C. 75,83%. D. 78,56%.
Câu 65. Sản phẩm của phản ứng phân hủy caxicabonat bởi nhiệt là:
A. CaO và SO2. B. CaO và P2O5. C. CaO và CO. D. CaO và CO2.
Câu 66. Dùng NaOH để làm khô chất nào sau đây?
A. CO2. B. NO2. C. SO2. D. NO.
Câu 67. Thuốc thử để nhận biết dung dịch Ca(OH)2 là :
A. Na2CO3 B. KCl C. NaOH D. BaCl2
Câu 68. Công thức hoá học của oxide có thành phần % về khối lượng của Mn là 63,22%:
A. MnO2. B. MnO3. C. Mn2O7. D. M2O4.
Câu 69. Để nhận biết 3 ống nghiệm chứa dung dịch HCl, dung dịch H2SO4 và nước ta dùng:
A. Quì tím, dung dịch BaCl2. B. Quì tím, dung dịch NaNO3.
C. Quì tím, dung dịch Na2SO4. D. Quì tím, dung dịch NaCl.
Câu 70. Khi nhỏ từ từ H2SO4 đậm đặc vào đường chứa trong cốc hiện tượng quan sát được là:
A. Màu đen xuất hiện và có bọt khí sinh ra.
B. Màu đen xuất hiện, không có bọt khí sinh ra.
C. Sủi bọt khí, đường không tan.
D. Màu trắng của đường mất dần, không sủi bọt.
Câu 71. Phát biểu nào mô tả đúng về tính chất của CaO?
A. CaO tan rất kém trong nước. B. CaO có tên gọi là đá vôi.
C. CaO là chất rắn màu trắng. D. CaO là một oxit axit
Câu 72. Cặp chất tác dụng được với dung dịch NaOH là:
A. FeO, Fe2O3. B. NO, NO2. C. CO, SO2. D. SO2, SO3.
Câu 73. Chất nào sau đây không bền ở nhiệt độ thường?
A. HCl. B. H2SO3. C. Na2SO4. D. KCl.
Câu 74. Trung hoà 100 ml dung dịch H2SO4 1M bằng V (ml) dung dịch NaOH 1M. Giá trị của V là:
A. 50 ml. B. 200 ml. C. 300 ml. D. 400 ml.
Câu 75. Dãy các chất không tác dụng được với dung dịch HCl là
A. BaCl2, Na2SO4, CuSO4. B. Al2O3, Fe2O3, Na2O.
C. Al(OH)3, Fe(OH)3, Cu(OH)2. D. Al, Fe, Pb.
Câu 76. Dung dịch Ca(OH)2 và dung dịch NaOH có những tính chất hóa học của base tan vì:
A. Làm đổi màu chất chỉ thị, tác dụng với acid.
B. Làm đổi màu chất chỉ thị, tác dụng với oxide acid và acid.
C. Tác dụng với oxit axit và axit.
D. Làm đổi màu chất chỉ thị, tác dụng với oxide axit
Câu 77. Canxi hỉoxit được sử dụng rộng rãi trong nhiều ngành công nghiệp. Công thức của nó là:
A. CaSO4. B. CaCO3. C. Ca(OH)2. D. CaO.
Câu 78. Cặp chất đều làm đục nước vôi trong Ca(OH)2?
A. SO2, K2O. B. SO2, BaO. C. CO2, Na2O. D. CO2, SO2.
Câu 79. Hoà tan 7,18 gam muối NaCl vào 20 gam nước ở 20°C thì được dung dịch bão hoà. Độ tan của NaCl ở nhiệt độ đó là:
Hydroxide của nguyên tố T có tính base rất mạnh và tác dụng được với HCl theo tỉ lệ mol giữa hydroxide của T và HCl là 1 : 2. Hãy dự đoán nguyên tố T thuộc nhóm nào trong bảng tuần hoàn các nguyên tố hóa học.
- Vì hydroxide của T có tính base rất mạnh, tác dụng với HCl nên T là kim loại ⟹ T có thể thuộc nhóm IA hoặc IIA.
- Tỉ lệ mol giữa hydroxide của T và HCl là 1 : 2 ⟹ CTHH của muối tạo thành là TCl2 ⟹ T có hóa trị II.
⟹ T thuộc nhóm IIA, nhóm kim loại kiềm thổ nên hydroxide có tính base rất mạnh.
Tính chất hoá học của các hợp chất vô cơ được tóm tắt bằng sơ đồ dưới đây:
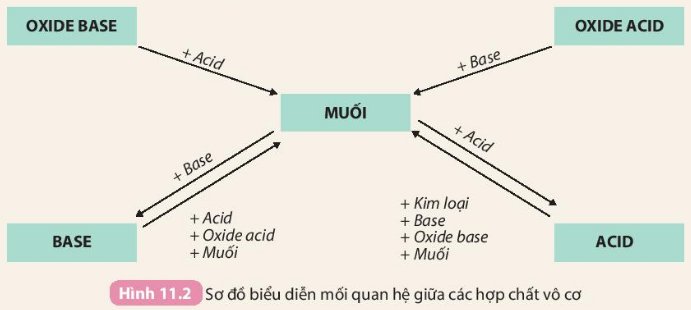
Dựa vào sơ đồ Hình 11.2 và cho biết tính chất của oxide, acid, base. Viết phương trình hoá học minh hoạ.
Bài 1. Viết công thức hóa học tạo bởi các thành phần tương ứng vào ô trống
Nguyên tố↓ | O | OH | NO3 | SO4 | CO3 | Cl |
Na |
|
|
|
|
|
|
Fe(III) |
|
|
|
|
|
|
K |
|
|
|
|
|
|
Ca |
|
|
|
|
|
|
Al |
|
|
|
|
|
|
Fe(II) |
|
|
|
|
|
|
Mg |
|
|
|
|
|
|
Phân loại các công thức mới viết trong bảng trên(basic oxide , muối ,base)
Bài 2. Viết công thức hóa học tạo bởi các thành phần tương ứng vào ô trống
| Cl | Br | I | F | NO3 | SO4 | CO3 | PO4 | S(II) |
H |
|
|
|
|
|
|
|
|
|
Các công thức mới viết thuộc loại hợp chất nào?
Bài 3.
a/Viết 5 công thức hóa học acidic oxide(oxit axit-vn)
b/Viết 5 công thức hóa học basic oxide(oxit bazơ-vn)
c/Viết 5 công thức hóa học acid.
d/Viết 5 công thức hóa học base tan trong nước (kiềm)và . 5 công thức hóa học base không tan trong nước.
e/ Viết 10 công thức hóa học muối.
Bài 4. Hoàn thành các phương trình sau
1/ K2O + H2O ![]() ...
...
2/ ........... + ..........![]() NaOH
NaOH
3/ ........... + ..........![]() Ca(OH)2
Ca(OH)2
4/ ........... + ..........![]() Ba(OH)2
Ba(OH)2
5/ K + H2O ![]()
6/ Na + H2O ![]()
7/ Ca + H2O ![]()
8/ Ba + H2O ![]()
9/ CO2 + H2O ![]()
10/ SO2 + H2O ![]()
11/ CO2 + H2O ![]()
12/ SO2 + H2O ![]()
13/ HCl + Fe ![]() ...............+ .........
...............+ .........
14/ HCl + Al ![]() ...............+ .........
...............+ .........
15/ H2SO4 + Mg ![]() ...............+ .........
...............+ .........
16/ H2SO4 + Zn ![]() ...............+ .........
...............+ .........
17/ H2SO4 + Al ![]() ...............+ .........
...............+ .........
18/ Ca + O2 ![]() ............
............
19/ Al + O2 ![]() ............
............
20/ Fe + O2 ![]() ............
............
21/ P + O2 ![]() ............
............
22/ CH4 + O2 ![]() ............+ .......
............+ .......
23/ H2 + CuO ![]() ............+ .......
............+ .......
24/ HCl + Fe2O3 ![]() ............+ .......
............+ .......
25/ HCl + FeO ![]() ............+ .......
............+ .......
Bài 5. Hoàn thành chuỗi phản ứng sau
1/ H2 ![]() H2O
H2O ![]() H2SO4
H2SO4 ![]() FeSO4
FeSO4
2/ H2 ![]() H2O
H2O ![]() H2SO4
H2SO4 ![]() Al2(SO4)3
Al2(SO4)3
3/ Na ![]() Na2O
Na2O ![]() NaOH
NaOH
4/ Ca ![]() CaO
CaO ![]() Ca(OH)2
Ca(OH)2
5/ Ba ![]() BaO
BaO ![]() Ba(OH)2
Ba(OH)2