Viết cấu hình electron nguyên tử của nguyên tố aluminium (Z = 13) và biểu diễn cấu hình electron của aluminium theo ô orbital. Từ đó, xác định số electron độc thân của nguyên tử này.

Những câu hỏi liên quan
Biểu diễn cấu hình theo ô orbital (chỉ với lớp ngoài cùng) các nguyên tử có Z từ 1 đến 20. Xác định số electron độc thân của mỗi nguyên tử.
Số hiệu nguyên tử Z | Orbital | Số electron độc thân |
1 | 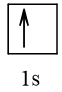 | 1 |
2 | 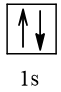 | 0 |
3 | 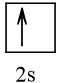 | 1 |
4 | 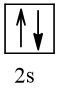 | 0 |
5 | 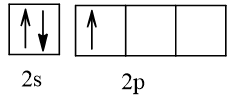 | 1 |
6 | 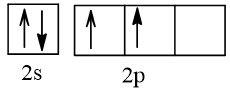 | 2 |
7 | 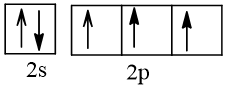 | 3 |
8 | 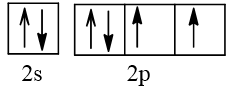 | 2 |
9 | 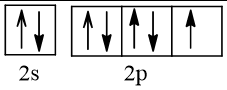 | 1 |
10 | 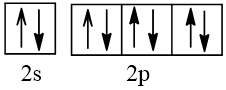 | 0 |
11 | 1 | |
12 | 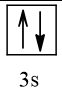 | 0 |
13 | 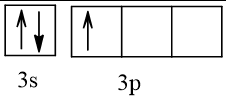 | 1 |
14 | 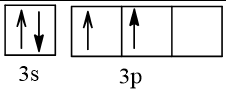 | 2 |
15 | 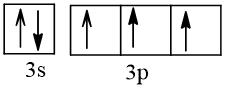 | 3 |
16 | 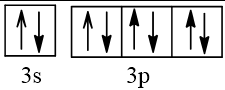 | 2 |
17 | 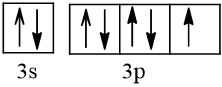 | 1 |
18 | 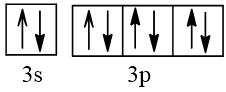 | 0 |
19 | 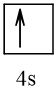 | 1 |
20 | 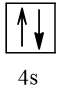 | 0 |
Đúng 0
Bình luận (0)
Cho ngtử K(Z=19) a) viết cấu hình electron nguyên tử và biểu diễn cấu hình theo ô orbital của nguyên tử Cl b)hãy cho biết Cl là nguyên tố s,p hay d?giải thích
Viết cấu hình electron nguyên tử và xác định số electron độc thân của các nguyên tố có Z = 7, , Z = 15, Z = 19, Z = 21, Z = 24, Z = 28, Z = 29 ?
Câu1:biễu diễn cấu hình của oxygen và potassium trong ô orbital. xác định số electron độc thân Câu 2: nêu các quy tắc dự đoán tính chất dựa vào cấu hình electron. Câu3: dự đoán tính chất hóa học cơ bản (tính kim loại, phi kim) của 20 nguyên tố có z từ 1 đến 20
Tổng số hạt proton, nơtron và electron trong nguyên tử của một nguyên tố là 13. Xác định tên nguyên tố và nguyên tử khối của nguyên tố đó. Viết cấu hình electron nguyên tử.
- Trong nguyên tử thì tỉ số N/Z ≥ 1 và N/Z ≤ 1,5
- Trong nguyên tử số proton bằng số electron.
Theo đầu bài tổng 3 loại hạt là 13. Ta có thể biện luận như sau :
+ Nếu số p = số e = 3 thì số n = 13 - (3 + 3) = 7.
Tỉ số N/Z = 7/3 = 2,3 > 1,5 (loại)
+ Nếu số p = số e = 4 thì số n = 13 - (4 + 4) = 5.
Tỉ số N/Z = 5/4 = 1,25 (phù hợp)
+ Nếu số p = số e = 5 thì số n = 13 - (5 + 5) = 3.
Tỉ số N/Z = 3/5 = 0,6 < 1 (loại)
Vậy nguyên tử đó có Z = 4. Đó là beri (Be).
Nguyên tử khối của nguyên tố đó là : 4 + 5 = 9 đvC.
Cấu hình electron nguyên tử : 1 s 2 2 s 2
Đúng 1
Bình luận (0)
Nguyên tố X có tổng số hạt cơ bản là 34, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10
a) Hãy viết kí hiệu nguyên tử của ngtố X
b) Việt cấu hình electron nguyên tử, cấu hình electron theo orbital của X
c) Từ cấu hình electron, dự đoán tính chất hoá học
d) Xác đinh vị trí của X trong bảng tuần hoàn
a, Ta có: P + N + E = 34
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 34 (1)
Theo đề, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
⇒ 2P - N = 10 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=11=Z\\N=12\end{matrix}\right.\) ⇒ A = 11 + 12 = 23
→ KH: \(^{23}_{11}X\)
b, Cấu hình e: 1s22s22p63s1
Cấu hình e theo orbital:
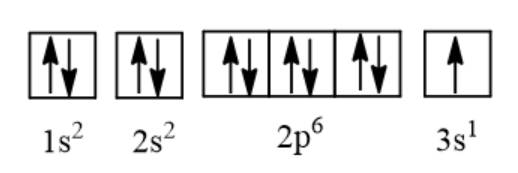
c, X có 1 e hóa trị → tính kim loại
d, - Z = 11 → ô số 11
- Có 3 lớp e → chu kỳ 3
- e cuối cùng phân bố ở phân lớp s, có 1 e hóa trị → nhóm IA
Vậy: X thuộc ô số 11, chu kỳ 3, nhóm IA
Đúng 0
Bình luận (0)
Tổng số hạt proton notron electron trong nguyên tử của nguyên tố là 18 Xác định nguyên tử khối viết cấu hình electron của nguyên tử đó
gọi p,n,e là số protn, notron, electron
ta có
p+n+e=18
2p+n=18 vì p=e
n=18-2p (1)
nguyên tử bền ta có
Đúng 0
Bình luận (0)
Nguyên tử của một nguyên tố có Z = 28. a) Hãy viết cấu hình lectron nguyên tử của nguyên tố đó. b) Xác định số lớp electron của nguyên tử.
\(Z=28\)
Cấu hình e: \(1s^22s^22p^63s^23p^63d^84s^2\)
Có 4 lớp electron của nguyên tử.
Đúng 1
Bình luận (0)
a, Z=28 -> Cấu hình: 1s22s22p63s23p63d84s2
b, Số lớp electron: 4
Đúng 1
Bình luận (0)
Một nguyên tố có số thứ tự z = 11.
Hãy viết cấu hình electron nguyên tử của nguyên tố đó và từ cấu hình electron hãy cho biết nguyên tố đó thuộc chu kì thứ mấy và thuộc nhóm nào ? Các nguyên tố thuộc nhóm này có tên chung là gì ?
Ứng với Z = 11, nguyên tử có 11 electron, do đó có cấu hình electron : 1 s 2 2 s 2 2 p 6 3 s 1
Nguyên tử có 3 lớp electron (lớp K, L, M), vậy nguyên tố đó thuộc chu kì 3. Lớp ngoài cùng có 1 electron, vậy nguyên tố đó thuộc nhóm IA. Các nguyên tố thuộc nhóm này (trừ hiđro) có tên chung là các kim loại kiềm.
Đúng 0
Bình luận (0)

















