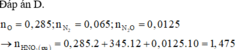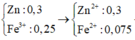Làm lạnh 500 gam dung dịch Fe2(SO4)3 40% ở aoC xuống boC thấy tách ra m gam tinh thể Fe2(SO4)3.10H2O. Biết độ tan của Fe2(SO4)3 ở boC là 45,45 gam. Tìm m.

Những câu hỏi liên quan
Cho 16g Fe2O3 phản ứng vừa đủ với dung dịch H2SO4 20% thu được dung dịch X.Tính nồng đọ % của dung dịch X.Sau đó hạ nhiệt độ dung dịch X xuống 0 C làm tách ra m gam Fe2(SO4)3.5H2O.Tính m
Cho dung dịch chứa 16,8 gam NaOH vào dung dịch X chứa 8 gam Fe2(SO4)3 và 13,68 gam Al2(SO4)3 thu được 500 ml dung dịch Y và m gam kết tủa. Tính nồng độ mol các chất trong dung dịch Y và tính m?
PTHH: \(Fe_2\left(SO_4\right)_3+6NaOH\rightarrow3Na_2SO_4+2Fe\left(OH\right)_3\downarrow\)
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\downarrow\)
Ta có: \(n_{NaOH\left(p/ứ\right)}=6n_{Fe_2\left(SO_4\right)_3}+6n_{Al_2\left(SO_4\right)_3}=6\cdot\left(\dfrac{8}{400}+\dfrac{13,68}{342}\right)=0,36\left(mol\right)\)
Mà \(\Sigma n_{NaOH}=\dfrac{16,8}{40}=0,42\left(mol\right)\) \(\Rightarrow n_{NaOH\left(dư\right)}=0,06\left(mol\right)\)
PTHH: \(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Al\left(OH\right)_3}=2n_{Al_2\left(SO_4\right)_3}=0,08\left(mol\right)\\n_{NaOH\left(dư\right)}=0,06\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) NaOH p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Na_2SO_4}=0,04\cdot3+0,02\cdot3=0,18\left(mol\right)\\n_{NaAlO_2}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{Na_2SO_4}}=\dfrac{0,18}{0,5}=0,36\left(M\right)\\C_{M_{NaAlO_2}}=\dfrac{0,06}{0,5}=0,12\left(M\right)\end{matrix}\right.\)
Đúng 2
Bình luận (1)
100 ml dung dịch Fe2(SO4)3 1M có thể hòa tan tối đa m gam Cu. Giá trị của m là
A. 9,6 gam
B. 3,2 gam
C. 6,4 gam
D. 12,8 gam
100 ml dung dịch Fe2(SO4)3 1M có thể hòa tan tối đa m gam Cu. Giá trị của m là
A. 9,6 gam.
B. 3,2 gam.
C. 6,4 gam.
D. 12,8 gam.
Cho 23,8 gam kim loại M tan hết trong dung dịch H2SO4 loãng tạo ra ion M2+. Dung dịch tạo thành có thể tác dụng vừa đủ với 200 ml dung dịch Fe2(SO4)3 1M để tạo ra ion M4+ và Fe2+. M là: A. Sn B. Pb C. Au D. Zn
Đọc tiếp
Cho 23,8 gam kim loại M tan hết trong dung dịch H2SO4 loãng tạo ra ion M2+. Dung dịch tạo thành có thể tác dụng vừa đủ với 200 ml dung dịch Fe2(SO4)3 1M để tạo ra ion M4+ và Fe2+. M là:
A. Sn
B. Pb
C. Au
D. Zn
Đáp án A
Nhận thấy M có thể tan trong dung dịch H2SO4 loãng → Loại Au, Pb
Ion M2+ + Fe3+ → M4+ + Fe2+ → chỉ có đáp án A thỏa mãn .
Sn + H2SO4 → SnSO4 + H2
SnSO4 + Fe2(SO4)3 → Sn(SO4)2 + 2FeSO4
Đúng 0
Bình luận (0)
Thêm 131,9 g Fe2(SO4)3 vào dung dịch D; khuấy đều thấy tách ra 28,1g tinh thể X. Biết độ tan của Fe2(SO4)3 tại nhiệt độ thí nghiệm là 1g/1ml H2O. Xác định công thức của X.
Cho dung dịch chứa 16,8 gam NaOH vào dung dịch hỗn hợp chứa 8 gam Fe2(SO4)3 và 13,68 gam Al2(SO4)3, sau các phản ứng xảy ra hoàn toàn thu được 500 ml dung dịch X và kết tủa. Nồng độ mol các chất trong dung dịch X là A. [Na2SO4 ] 0,12M; [Na[Al(OH)4]] 0,12M B. [NaOH] 0,12M; [Na[Al(OH)4]] 0,36M C. [NaOH] 0,6M]; [Na[Al(OH)4]] 0,12M D. [Na2SO4 ] 0,36M; [Na[Al(OH)4]] 0,12M
Đọc tiếp
Cho dung dịch chứa 16,8 gam NaOH vào dung dịch hỗn hợp chứa 8 gam Fe2(SO4)3 và 13,68 gam Al2(SO4)3, sau các phản ứng xảy ra hoàn toàn thu được 500 ml dung dịch X và kết tủa. Nồng độ mol các chất trong dung dịch X là
A. [Na2SO4 ] = 0,12M; [Na[Al(OH)4]] = 0,12M
B. [NaOH] = 0,12M; [Na[Al(OH)4]] = 0,36M
C. [NaOH] = 0,6M]; [Na[Al(OH)4]] = 0,12M
D. [Na2SO4 ] = 0,36M; [Na[Al(OH)4]] = 0,12M
Đáp án D
• 0,42 mol NaOH + 0,02 mol Fe2(SO4)3; 0,04 mol Al2(SO4)3 → 500ml X + ↓
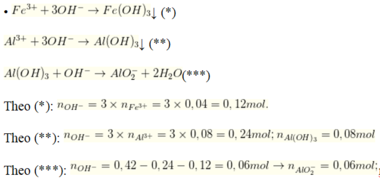
nAl(OH)3 = 0,08 - 0,06 = 0,02 mol
Vậy sau phản ứng 500ml dung dịch X gồm 0,06 mol Na[Al(OH)4]; 0,18 mol Na2SO4
→ CM các chất trong X là CMNa2SO4 = 0,06 : 0,5 = 0,12 M;
CMNa[Al(OH)4] = 0,18 : 0,5 = 0,36 M
Đúng 1
Bình luận (0)
Hoà tan 19,5 gam Zn vào 250 ml dung dịch chứa Fe2(SO4)3 0,5M. Sau khi phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là A. 8,4 B. 11,375 C. 11,2 D. 9,8
Đọc tiếp
Hoà tan 19,5 gam Zn vào 250 ml dung dịch chứa Fe2(SO4)3 0,5M. Sau khi phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 8,4
B. 11,375
C. 11,2
D. 9,8
Hoà tan 19,5 gam Zn vào 250 ml dung dịch chứa Fe2(SO4)3 0,5M. Sau khi phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 8,4
B. 11,375
C. 11,2
D. 9,8