Đốt cháy 6g hợp chất D cần dùng vừa đủ 10,08 lít Oxi ở đktc. Sản phẩm cháy thu được gồm CO2 và H2O theo tỉ lệ \(\dfrac{Vco_2}{Vh_2o}\)=\(\dfrac{3}{4}\). Xđ CTPT của D

Những câu hỏi liên quan
Đốt cháy hoàn toàn m gam hợp chất A hữu cơ cần dùng vừa đủ 13,44 lít khí O2 (ở ĐKTC) thu được sản phẩm là CO2 và H2O với tỉ lệ số mol lần lượt là 2:3. Xác định CTHH của A biết PTKA = 40
Đốt cháy 6g Y cần 4,48 lít Oxi (đktc) thu được CO2 và H2O(tỉ lệ mol 1:1).
a.Tính khối lượng mỗi sản phẩm tạo thành.
b.Hỏi Y có nguyên tố nào?Tìm CTPT của Y?MY=60g/mol.
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo ĐLBTKL: mY + mO2 = mCO2 + mH2O
=> mCO2 + mH2O = 6 + 0,2.32 = 12,4(g)
Mà nCO2 : nH2O = 1:1
=> nCO2 = 0,2; nH2O = 0,2
=> \(\left\{{}\begin{matrix}m_{CO_2}=0,2.44=8,8\left(g\right)\\m_{H_2O}=0,2.18=3,6\left(g\right)\end{matrix}\right.\)
b) Do sản phẩm có các nguyên tố C, H, O
=> Y có các nguyên tố C, H và có thể có O
Bảo toàn C: nC = 0,2
Bảo toàn H: nH = 0,4
=> \(n_O=\dfrac{6-0,2.12-0,4}{16}=0,2\left(mol\right)\)
Xét nC : nH : nO = 0,2 : 0,4 : 0,2 = 1:2:1
=> CTPT: (CH2O)n
Mà MY = 60g/mol
=> n = 2
=> CTPT: C2H4O2
Đúng 1
Bình luận (0)
Hợp chất A mạch hở có khối lượng mol là MA 200 gam/mol. Khi đốt cháy hoàn toàn 1,88 gam A, cần dùng vừa đủ 1,904 lít khí oxi (đktc), sản phẩm chỉ gồm CO2, H2O theo tỉ lệ số mol tương ứng là 4 : 3. Mặt khác, cho 1,88 gam A vào dung dịch NaOH dư, phản ứng tạo ra một rượu và hai muối của hai axit đơn chức. Cô cạn dung dịch, thu được chất rắn khan B nặng 2,56 gam. Nung nóng B trong oxi dư cho các phản ứng hoàn toàn, thu được 2,12 gam chất rắn khan C, được CO2 và H2O bay ra.Tìm công thức phân tử và...
Đọc tiếp
Hợp chất A mạch hở có khối lượng mol là MA < 200 gam/mol. Khi đốt cháy hoàn toàn 1,88 gam A, cần dùng vừa đủ 1,904 lít khí oxi (đktc), sản phẩm chỉ gồm CO2, H2O theo tỉ lệ số mol tương ứng là 4 : 3. Mặt khác, cho 1,88 gam A vào dung dịch NaOH dư, phản ứng tạo ra một rượu và hai muối của hai axit đơn chức. Cô cạn dung dịch, thu được chất rắn khan B nặng 2,56 gam. Nung nóng B trong oxi dư cho các phản ứng hoàn toàn, thu được 2,12 gam chất rắn khan C, được CO2 và H2O bay ra.
Tìm công thức phân tử và viết công thức cấu tạo có thể có của A.
Đốt cháy hoàn toàn một hợp chất A cần dùng vừa hết 10,08 lít oxi ở đktc, sau phản ứng thu được 4,72 lít CO2 ở đktc và 7,2 gam nước.
a) Tính số nguyên tử mỗi loại trong 1 mol A.
b) Tìm CTPT của A biết MA=60g/mol.
*Sửa đề: "6,72 lít CO2"
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\n_H=2n_{H_2O}=2\cdot\dfrac{7,2}{18}=0,8\left(mol\right)\end{matrix}\right.\)
Ta có: \(n_{O_2\left(p.ứ\right)}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
Ta thấy \(2n_{O_2}< 2n_{CO_2}+n_{H_2O}\) \(\Rightarrow\) Trong A có Oxi
Bảo toàn Oxi: \(n_{O\left(trong.A\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\) \(\Rightarrow n_O=0,1\left(mol\right)\)
Số nguyên tử C trong A là: \(0,3\cdot6\cdot10^{23}=1,8\cdot10^{23}\)
Số nguyên tử H trong A là: \(0,8\cdot6\cdot10^{23}=4,8\cdot10^{23}\)
Số nguyên tử O trong A là: \(0,1\cdot6\cdot10^{23}=6\cdot10^{22}\)
Xét tỉ lệ: \(C:H:O=0,3:0,8:0,1=3:8:1\)
\(\Rightarrow\) CTPT của A là (C3H8O)n
Mà \(M_A=60\) \(\Rightarrow n=1\)
Vậy CTPT của A là C3H8O
Đúng 1
Bình luận (0)
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết (∏) nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol nX : nY 1: 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây? A. 71%. B. 70%. C. 29%. D. 30%
Đọc tiếp
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết (∏) nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol nX : nY = 1: 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây?
A. 71%.
B. 70%.
C. 29%.
D. 30%
Đáp án B
nO2 = 7/22,4 = 0,3125 (mol)
Gọi số mol của X và Y lần lượt là a và 5a (mol)
BTKL: mZ + mO2 = mCO2 + mH2O + mN2
=> mCO2 + mH2O + mN2 = 3,17 + 0,3125.32 =13,17(g) (1)
Khối lượng dung dịch NaOH đặc tăng chính là khối lượng của CO2 và H2O
=> mCO2 + mH2O = 12,89 (g) (2)
Từ (1) và (2) => mN2 = 0,28 (g) => nN2 = 0,01 (mol)
BTNT N => nX = 2nN2 = 0,02 (mol)
=> nZ = 6nX = 0,12 (mol)
Gọi x và y lần lượt là số mol của CO2 và H2O
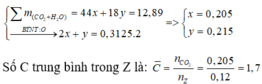
=> Y phải có CH4
TH1: Hidrocacbon còn lại trong Y không có liên kết pi
=> nH2O – nCO2 = 1,5namin + nY => ta thấy không thỏa mãn vì: 0,01 #0,08 => loại
TH2: Hidrocacbon còn lại trong Y không có 1 liên kết pi
=> nH2O – nCO2 = 1,5namin + nCH4 ( Vì đốt HC có 1 liên kết pi cho mol CO2 = H2O )
=> nCH4 = ( 0,215 – 0,205) – 1,5.0,02 = - 0,02 (mol) < 0 => loại
TH3: Hidrocacbon còn lại trong Y không có 2 liên kết pi
Gọi a và b lần lượt là số mol của CH4 và CmH2m-2 trong Y
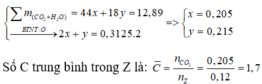
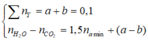
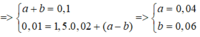
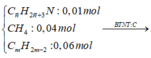
![]()
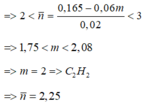
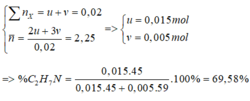
Đúng 0
Bình luận (0)
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết (π) nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol
n
X
:
n
Y
1
:
5
thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm
C
O
2
,...
Đọc tiếp
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết (π) nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol n X : n Y = 1 : 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm C O 2 , H 2 O v à N 2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây?
A. 71%
B. 70%
C. 29%
D. 30%.
n O 2 = 7 / 22 , 4 = 0 , 3125 m o l
Gọi số mol của X và Y lần lượt là a và 5a (mol)
B T K L : m Z + m O 2 = m C O 2 + m H 2 O + m N 2
= > m C O 2 + m H 2 O + m N 2 = 3 , 17 + 0 , 3125.32 = 13 , 17 g a m 1
Khối lượng dung dịch NaOH đặc tăng chính là khối lượng của C O 2 v à H 2 O
= > m C O 2 + m H 2 O = 12 , 89 g 2
Từ (1) và (2) => m N 2 = 0 , 28 g ⇒ n N 2 = 0 , 01 m o l
BTNT N = > n X = 2 n N 2 = 0 , 02 m o l
= > n Z = 6 n X = 0 , 12 m o l
Gọi x và y lần lượt là số mol của C O 2 v à H 2 O
∑ m ( C O 2 + H 2 O ) = 44 x + 18 y = 12 , 89 → BTNT : O 2 x + y = 0 , 3125.2 = > x = 0 , 205 y = 0 , 215
Số C trung bình trong Z là: = n C O 2 n Z = 0 , 205 0 , 12 = 1 , 7
=> Y phải có C H 4
TH1: Hiđrocacbon còn lại trong Y không có liên kết pi
= > n H 2 O − n C O 2 = 1 , 5 n a m i n + n Y = > ta thấy không thỏa mãn vì: 0,01 ≠ 0,08 => loại
TH2: Hiđrocacbon còn lại trong Y không có 1 liên kết pi
= > n H 2 O − n C O 2 = 1 , 5 n a m i n + n C H 4 (Vì đốt HC có 1 liên kết pi cho số mol C O 2 = H 2 O )
= > n C H 4 = (0,215 – 0,205) – 1,5.0,02 = - 0,02 (mol) < 0 => loại
TH3: Hiđrocacbon còn lại trong Y không có 2 liên kết pi
Gọi a và b lần lượt là số mol của C H 4 v à C m H 2 m − 2 trong Y
∑ n Y = a + b = 0 , 1 n H 2 O − n C O 2 = 1 , 5 n amin + a − b ⇒ a + b = 0 , 1 0 , 01 = 1 , 5.0 , 02 + a − b ⇒ a = 0 , 04 b = 0 , 06
Gọi CTPT chung của 2 amin là:
C H 2 + 3 N : 0 , 01 m o l CH 4 : 0 , 04 m o l C m H 2 m − 2 : 0 , 06 m o l → B T N T : C n C O 2 = 0,01 n ¯ + 0,04 + 0,06m = 0,205
= > 2 < n ¯ = 0 , 165 − 0 , 06 m 0 , 02 < 3
=> 1,75 < m < 2,08
=> m = 2 => C 2 H 2
= > n ¯ = 2 , 25
Gọi u và v lần lượt là số mol của C 2 H 7 N v à C 3 H 9 N
∑ n X = u + v = 0 , 02 = 2 u + 3 v 0 , 02 = 2 , 25 = > u = 0 , 015 m o l v = 0 , 005 m o l
=> % C 2 H 7 N = 0 , 015.45 0 , 015.45 + 0 , 005.59 .100 % = 69 , 58 %
Gần nhất với 70%
Đáp án cần chọn là: B
Đúng 0
Bình luận (0)
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết (∏) nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol nX : nY 1: 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây? A. 71%. B. 70%. C. 29%. D. 30%
Đọc tiếp
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết (∏) nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol nX : nY = 1: 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây?
A. 71%.
B. 70%.
C. 29%.
D. 30%
Đáp án B
nO2 = 7/22,4 = 0,3125 (mol)
Gọi số mol của X và Y lần lượt là a và 5a (mol)
BTKL: mZ + mO2 = mCO2 + mH2O + mN2
=> mCO2 + mH2O + mN2 = 3,17 + 0,3125.32 =13,17(g) (1)
Khối lượng dung dịch NaOH đặc tăng chính là khối lượng của CO2 và H2O
=> mCO2 + mH2O = 12,89 (g) (2)
Từ (1) và (2) => mN2 = 0,28 (g) => nN2 = 0,01 (mol)
BTNT N => nX = 2nN2 = 0,02 (mol)
=> nZ = 6nX = 0,12 (mol)
Gọi x và y lần lượt là số mol của CO2 và H2O
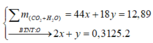
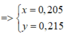
Số C trung bình trong Z là:
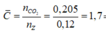
=> Y phải có CH4
TH1: Hidrocacbon còn lại trong Y không có liên kết pi
=> nH2O – nCO2 = 1,5namin + nY => ta thấy không thỏa mãn vì: 0,01 #0,08 => loại
TH2: Hidrocacbon còn lại trong Y không có 1 liên kết pi
=> nH2O – nCO2 = 1,5namin + nCH4 ( Vì đốt HC có 1 liên kết pi cho mol CO2 = H2O )
=> nCH4 = ( 0,215 – 0,205) – 1,5.0,02 = - 0,02 (mol) < 0 => loại
TH3: Hidrocacbon còn lại trong Y không có 2 liên kết pi
Gọi a và b lần lượt là số mol của CH4 và CmH2m-2 trong Y
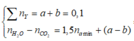
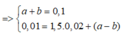
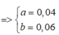
Gọi CTPT chung của 2 amin là:
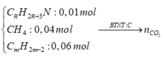
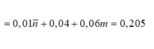
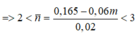
=> 1,75 < m < 2,08
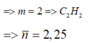
Gọi u và v lần lượt là số mol của C2H7N và C3H9N
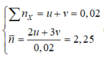
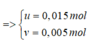
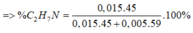
= 69,58%
Gần nhất với 70%
Đúng 0
Bình luận (0)
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết pi nhở hơn 3. Trộn X và Y theo tỉ lệ mol
n
X
:
n
Y
1
:
5
thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm
C
O
2
,
...
Đọc tiếp
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết pi nhở hơn 3. Trộn X và Y theo tỉ lệ mol n X : n Y = 1 : 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm C O 2 , H 2 O v à N 2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây?
A. 21%.
B. 70%
C. 79%.
D. 30%.
3 , 17 g Z C n H 2 n + 3 N : z C m H 2 m + 2 − 2 k : 5 z + O 2 : + 0 , 3125 m o l → C O 2 : a H 2 O : b N 2 : 0 , 5 z + N a O H → Δ m = 12 , 89 g a m
⇒ m C O 2 + m H 2 O = Δ m n C O 2 + n H 2 O = 2 n O 2 B T N T ⇒ 44 a + 18 b = 12 , 892 a + b = 2.0 , 3125 ⇒ a = 0 , 205 b = 0 , 215
m Z = m C + m H + m N ⇒ m N = , 17 - ( 12 . 0 , 205 + 2 . 0 , 215 ) = 0 , 28 g a m
⇒ n N = 0 , 02 m o l ⇒ z = 0 , 02 ⇒ n Y = 5 z = 0 , 1
n H 2 O − n C O 2 = 0 , 01 = 1 , 5 z + 5 z . ( 1 − k ¯ ) ⇒ k ¯ = 1 , 2
n Z = 6 z = 0 , 12 m o l ⇒ C ¯ = n C O 2 n Z = 1 , 708 ; H ¯ = n H n Z = 3 , 583
Vì X chứa 2 amin C 2 H 7 N v à C 3 H 9 N , đều có số nguyên tử C > 1,708 và H > 3,583
→ Y chứa một hiđrocacbon có số nguyên tử C < 1,708 → Y chứa C H 4 .
Hai hiđrocacbon trong Y có số liên kết pi nhỏ hơn 3, mà C H 4 (k=0) và = 1,2
→ hiđrocacbon còn lại Y2 có k = 2 và số nguyên tử H < 3,583 → Y2: C 2 H 2
k ¯ = 1 , 2 ⇒ n C H 4 k = 0 n Y 2 k = 2 = 2 − 1 , 2 0 − 1 , 2 = 2 3
⇒ n C H 4 = 2 z = 0 , 04 ; n Y 2 = 0 , 06 m o l
n C O 2 = 0 , 205 = n . x + n C H 4 + 2 n C 2 H 2 ⇒ n = 0 , 205 − 0 , 04 − 2.0 , 06 0 , 02 = 2 , 25
X C 2 H 7 N : x C 3 H 9 N : y ⇒ x + y = 0 , 02 2 x + 3 y = 2 , 25.0 , 02 = n C ⇒ x = 0 , 015 y = 0 , 005
⇒ % C 2 H 7 N X = 0 , 015.45 0 , 015.45 + 0 , 005.59 .100 % = 69 , 59 %
Đáp án cần chọn là: B
Đúng 0
Bình luận (0)
Hỗn hợp X gồm các amino axit (chỉ có nhóm chức –COOH và –NH2, không có nhóm chức khác). Trong hỗn hợp X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192 : 77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 220 ml dung dịch HCl 1M. Đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít O2 (đktc) thu được 27,28 gam CO2 (sản phẩm cháy gồm CO2, H2O, N2). Giá trị của V là A. 17,472 B. 16,464 C. 16,576 D. 16,686
Đọc tiếp
Hỗn hợp X gồm các amino axit (chỉ có nhóm chức –COOH và –NH2, không có nhóm chức khác). Trong hỗn hợp X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192 : 77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 220 ml dung dịch HCl 1M. Đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít O2 (đktc) thu được 27,28 gam CO2 (sản phẩm cháy gồm CO2, H2O, N2). Giá trị của V là
A. 17,472
B. 16,464
C. 16,576
D. 16,686
Đáp án B
Ta có tỉ lệ số mol O và N trong X là 24:11 hay tỉ lệ -COOH: NH2 là 12:11.
Đê tác dụng với 19,62 gam hỗn hợp X cần 0,22 mol HCl, do vậy trong X số mol NH2là 0,22 mol.
Số mol COOH trong X là 0,24 mol.
Đốt cháy hoàn toàn 19,62 gam hỗn hợp X thu được 0,62 mol CO2.
Vậy X chứa 0,62 mol C, 0,22 mol N, 0,48 mol O và H.
→ n H = 19 , 62 - 0 , 62 . 12 - 0 , 22 . 14 - 0 , 48 . 16 = 1 , 42 m o l → n O = 0 , 62 + 1 , 42 4 - 0 , 24 = 0 , 735 m o l → V = 16 , 464 l í t
Đúng 0
Bình luận (0)











