Nhiệt phân hoàn toàn 16,8 gam NaHCO 3 thu được m gam Na 2 CO 3 . Giá trị của m là
A. 12,4.
B. 13,2.
C. 10,6.
D. 21,2.
Nhiệt phân hoàn toàn m gam kali clorat (với xúc tác thích hợp) thu được V lít khí oxi (ở đktc). Biết V lít khí oxi này có thể đốt cháy hoàn toàn 16,8 gam sắt tạo sắt từ oxit.
a. Viết các phương trình hóa học xảy ra.
b. Tìm giá trị của m và V.
\(n_{Fe}=\dfrac{16,8}{56}=0,3(mol)\\ a,2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\\ 3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ b,n_{O_2}=\dfrac{2}{3}n_{Fe}=0,2(mol)\\ \Rightarrow V_{O_2}=0,2.22,4=4,48(l)\\ n_{KClO_3}=\dfrac{2}{3}n_{O_2}=\dfrac{2}{15}(mol)\\ \Rightarrow m_{KClO_3}=\dfrac{2}{15}.122,5\approx 16,33(g)\)
Ba chất hữu cơ X, Y, Z (50 < MX < MY < MZ) đều có thành phần nguyên tố C, H, O. Đốt cháy hoàn toàn m gam hỗn hợp T gồm X, Y, Z, thu được 13,20 gam CO2. Mặt khác m gam T phản ứng vừa đủ dung dịch NaHCO3 thu được 0,896 lit CO2 (đktc). Cho m gam T phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 56,16 gam Ag. Phần trăm khối lượng của Y trong hỗn hợp T
Hỗn hợp X gồm axit fomic, axit acrylic, axit oxalic và axit axetic. Cho m gam X phản ứng hết với dung dịch NaHCO3 thu được 1,344 lít CO2 (đktc). Đốt cháy hoàn toàn m gam X cần 2,016 lít O2 (đktc), thu được 4,84 gam CO2 và a gam H2O. Giá trị của a là
A.1,62.
B.1,44.
C.3,60.
D.1,80.
H+ + HCO3- ® H2O + CO2; nCO2(1) = 0,06 mol; nO2 = 0,09; nCO2(2) = 0,11;
® nH+ = nCO2(1) = 0,06 mol; Trong hh X ta có: nO = 2nH+ = 0,12mol.
{C,H,O} + O2 ® CO2 + H2O. Áp dụng bảo toàn nguyên tố O, ta có:
0,12 + 2.0,09 = 2.0,11 + x ® x = 0,08 mol ® a = 18.0,08 = 1,44gam.
Hỗn hợp X gồm Fe(NO3)2, Fe(NO3)3, Cu(NO3)2 và AgNO3 (trong đó nguyên tố nitơ chiếm 13,944% về khối lượng). Nhiệt phân 30,12 gam X, thu được rắn Y. Thổi luồng khí CO dư qua Y nung nóng, thu được m gam rắn Z. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 10,28.
B. 11,22.
C. 25,92.
D. 11,52.
Chọn đáp án D
X {Fe(NO3)2, Fe(NO3)3, Cu(NO3)2, AgNO3} → t o Y {Fe2O3, CuO, Ag} → C O m(g) Z {Fe, Cu, Ag}.
nNO3 = nN = 30,12 × 0,13944 ÷ 14 = 0,3 mol ⇒ mZ = mX - mNO3 = 30,12 - 0,3 × 62 = 11,52(g).
Hỗn hợp X gồm Fe(NO3)2, Fe(NO3)3, Cu(NO3)2 và AgNO3 (trong đó nguyên tố nitơ chiếm 13,944% về khối lượng). Nhiệt phân 30,12 gam X, thu được rắn Y. Thổi luồng khí CO dư qua Y nung nóng, thu được m gam rắn Z. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 10,28.
B. 11,22.
C. 25,92.
D. 11,52.
X {Fe(NO3)2, Fe(NO3)3, Cu(NO3)2, AgNO3} → t o Y {Fe2O3, CuO, Ag} → CO m(g) Z {Fe, Cu, Ag}.
nNO3 = nN = 30,12 × 0,13944 ÷ 14 = 0,3 mol ⇒ mZ = mX - mNO3 = 30,12 - 0,3 × 62 = 11,52(g).
Đáp án D
Nhiệt phân hoàn toàn 16,8 gam muối cacbonat của một kim loại hóa trị II. Toàn bộ khí thu được hấp thụ hoàn toàn vào 350 g dung dịch NaOH 4% được dung dịch chứa 20,1 gam chất tan. Kim loại đó là:
A. Ba
B. Ca
C. Cu
D. Mg
Đáp án D
Gọi công thức của muối cacbonat đem nhiệt phân là MCO3
Có phản ứng: M C O 3 → t 0 M O + C O 2
Có n N a O H = 350 . 4 % 40 = 0,35; gọi n C O 2 = x
Vì CO2 được hấp thụ hoàn toàn vào dung dịch NaOH nên có 2 trường hợp xảy ra:
+) Trường hợp 1: Sau phản ứng NaOH còn dư, sản phẩm thu được là Na2CO3.
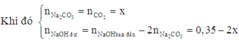
Mà dung dịch thu được có khối lượng chất tan là 20,1 gam
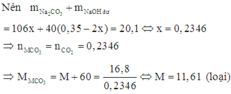
+) Trường hợp 2: Sản phẩm thu được trong dung dịch là Na2CO3 và NaHCO3
Khi đó

Mà dung dịch thu được có khối lượng chất tan là 20,1 gam nên
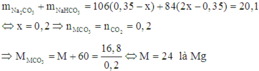
Vậy kim loại cần tìm là Mg.
Nhiệt phân hoàn toàn m gam NaHCO 3 thu được 10,6 gam Na 2 CO 3 . Giá trị của m là
A. 25,2.
B. 16,8
C. 23,2.
D. 8,40.
Cho 29,6 gam hỗn hợp Na 2 CO 3 và NaHCO 3 tác dụng với dung dịch HCl dư, sinh ra 6,72 lít khí (đktc). Khối lượng mỗi muối trong hỗn hợp ban đầu là (H = 1; C = 12; O = 16; Na = 23)
A. 12,8 gam và 16,8 gam
B. 21,2 gam và 8,4 gam.
C. 12 gam và 17,6 gam.
D. 20 gam và 9,6 gam.
\(n_{CO_2}=\dfrac{V_{CO_2}}{22,4}=\dfrac{6,72}{22,4}=0,3mol\)
Gọi \(n_{Na_2CO_3}\) là x \(\Rightarrow m_{Na_2CO_3}=106x\)
\(n_{NaHCO_3}\) là y \(\Rightarrow m_{NaHCO_3}=84y\)
\(Na_2CO_3+HCl\rightarrow2NaCl+H_2O+CO_2\)
x x ( mol )
\(NaHCO_3+HCl\rightarrow NaCl+H_2O+CO_2\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}106x+84y=29,6\\x+y=0,3\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\Rightarrow m_{Na_2CO_3}=106.0,2=21,2g\)
\(\Rightarrow m_{NaHCO_3}=84.0,1=8,4g\)
=> Chọn B
Hỗn hợp X gồm axit axetic, axit fomic và axit oxalic. Khi cho m gam X tác dụng với NaHCO3 dư thì thu được 15,68 lít khí CO2(đktc). Mặt khác, đốt cháy hoàn toàn m gam X cần 8,96 lít khí O2 (đktc), thu được 35,2 gam CO2 và y mol H2O. Giá trị của y là:
Ta có: \(n_{COOH\left(X\right)}=n_{CO_2}=0,7mol\)
Khi đốt X có: \(n_{CO_2}=0,4mol;n_{CO_2}=0,8mol\)
Theo ĐLBT oxi có \(n_O=2n_{COOH\left(X\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=y=0,6mol\)