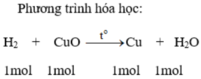
trong thí nghiệm khí hidro khử đồng ( II) oxit Em hãy cho biết sau khi đun nóng mạnh ở chỗ có CuO thì màu sắc của các chất sẽ chuyển đổi như thế nào? viết phương trình hóa học xảy ra

Những câu hỏi liên quan
Trong phòng thí nghiệm , người ta dùng hidro (H2) để khử 8 gam đồng (II) oxit (cuo) A. Viết phương trình hóa học của phản ứng xảy ra B. Tính khối lượng đồng (cu) thu được C. Tính thể tích hiđro đã dùng (ở đktc)
A. \(H_2+CuO\rightarrow Cu+H_2O\)
B. \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Cu}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)
C. Theo PTHH: \(n_{H_2}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Nêu hiện tượng và viết phương trình hóa học xảy ra (nếu có) trong các thí nghiệm sau:
Thí nghiệm 1:Dẫn khí hidro đi qua ống đựng bột đồng (II) oxit nung nóng
Thí nghiệm 2:Nhỏ dung dịch Na^2CO^3 vào ống nghiệm đựng nước vôi trong
Thí nghiệm 3:Nhỏ dung dịch HCL vào ống nghiện đựng CaCO^3
Thí nghiệm 4:Nhỏ dung dịch H^2SO^4 loãng vào ống nghiệm đựng kim loại đồng
Thí nghiệm 5:Nhỏ dung dịch HCL loãng vào ống nghiệm đựng kim lạo nhôm
Đọc tiếp
Nêu hiện tượng và viết phương trình hóa học xảy ra (nếu có) trong các thí nghiệm sau:
Thí nghiệm 1:Dẫn khí hidro đi qua ống đựng bột đồng (II) oxit nung nóng
Thí nghiệm 2:Nhỏ dung dịch Na^2CO^3 vào ống nghiệm đựng nước vôi trong
Thí nghiệm 3:Nhỏ dung dịch HCL vào ống nghiện đựng CaCO^3
Thí nghiệm 4:Nhỏ dung dịch H^2SO^4 loãng vào ống nghiệm đựng kim loại đồng
Thí nghiệm 5:Nhỏ dung dịch HCL loãng vào ống nghiệm đựng kim lạo nhôm
TN1: Hiện tượng: chất rắn màu đen chuyển thành màu nâu đỏ.
PTHH: H2 + CuO to→ Cu + H2O
TN2: Hiện tượng: xuất hiện kết tủa trắng.
PTHH: Na2CO3 + Ca(OH)2 → CaCO3↓ + 2NaOH
TN3: Hiện tượng: chất rắn tan, có bọt khí không màu bay ra.
PTHH: CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
TN4: Hiện tượng: không có hiện xảy ra.
TN5: Hiện tượng: chất rắn tan, có bọt khí không màu bay ra.
PTHH: 6HCl + 2Al → 2AlCl3 + 3H2↑
Đúng 1
Bình luận (0)
Nêu hiện tượng và viết phương trình hóa học xảy ra khi dẫn khí hidro H2 dư vào ống thủy tinh đựng đồng (II) oxit CuO đun nóng.
lúc này đồng(II)oxit chuyển dần từ màu đen sang màu đỏ và có một vài giọt nước xung quang bình. Bột đỏ đấy là đồng
\(PTHH:CuO+H_2-^{t^o}>Cu+H_2O\)
Đúng 1
Bình luận (2)
CuO+H2-to>Cu+H2O
HT : chất rắn dần chuyển từ đen sang đỏ
#yT
Đúng 0
Bình luận (1)
Một em học sinh làm thí nghiệm như sau : Cho một mẩu giấy quỳ tím vào ống nghiệm đựng nước cất, sau đó sục khí
CO
2
vào ống nghiệm. Màu của giấy quỳ tím có biến đổi không ? Nếu đun nóng nhẹ ống nghiệm thì màu của giấy quỳ tím biến đổi ra sao ? Hãy giải thích và viết các phương trình hoá học, nếu có.
Đọc tiếp
Một em học sinh làm thí nghiệm như sau : Cho một mẩu giấy quỳ tím vào ống nghiệm đựng nước cất, sau đó sục khí CO 2 vào ống nghiệm. Màu của giấy quỳ tím có biến đổi không ? Nếu đun nóng nhẹ ống nghiệm thì màu của giấy quỳ tím biến đổi ra sao ? Hãy giải thích và viết các phương trình hoá học, nếu có.
Khí CO 2 tan một phần vào nước tạo thành dung dịch H 2 CO 3 làm quỳ tím chuyển sang màu đỏ. Khi đun nóng nhẹ, độ tan của CO 2 trong nước giảm, CO 2 ) bay ra khỏi dung dịch, giấy quỳ trở lại màu tím ban đầu.
Đúng 0
Bình luận (0)
Có một bạn học sinh cho rằng: 1 Dùng khí Có hoặc H2 có thể khử các oxit nung nóng sau đây: Fe3O4, CuO,PbO,FexOy về dạng đơn chất 2 Dùng các chất giàu oxi:KCLO3,KMnO4, Hgo, H2O để điều chế O2 trong phòng thí nghiệm Hãy viết các phương trình hóa học mình họa, ghi rõ điều kiện phản ứng
Cho biết những hiện tượng nào dưới đây xảy ra trong thí nghiệm ( đường saccarozo và CuO, đun nóng) được mô phỏng qua hình vẽ: a) CuO từ màu đen chuyển sang màu đỏ. b) Bông từ màu trắng chuyển sang màu xanh. c) Dung dịch nước vôi trong bị vẩn đục. d) Dung dịch nước vôi trong bị vẩn đục, sau đó trở nên trong suốt. Viết phương trình hóa học xảy ra với mỗi hiện tượng quan sát được.
Đọc tiếp
Cho biết những hiện tượng nào dưới đây xảy ra trong thí nghiệm ( đường saccarozo và CuO, đun nóng) được mô phỏng qua hình vẽ:
a) CuO từ màu đen chuyển sang màu đỏ.
b) Bông từ màu trắng chuyển sang màu xanh.
c) Dung dịch nước vôi trong bị vẩn đục.
d) Dung dịch nước vôi trong bị vẩn đục, sau đó trở nên trong suốt.
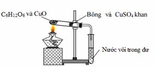
Viết phương trình hóa học xảy ra với mỗi hiện tượng quan sát được.
Các hiện tượng mô tả đúng với hiện tượng xảy ra trong thí nghiệm là:
b) Bông từ màu trắng chuyển sang màu xanh
c) Dung dịch nước vôi trong bị vẩn đục.
Vì khi đốt C12H22O11 xảy ra PTHH:
C12H22O11 + O2 → t ∘ 12CO2 + 11H2O
CuSO4( khan, màu trắng ) → h a p t h u n u o c CuSO4.5H2O (màu xanh)
CO2 + Ca(OH)2 dư → CaCO3↓ (trắng) + H2O
Đúng 0
Bình luận (0)
Cho khí hidro dư đi qua đồng (II) oxit nóng màu đen, người ta thu được 0,32g kim loại đồng màu đỏ và hơi nước ngưng tụ. Viết phương trình hóa học xảy ra.
câu 1:bằng phương phát hóa học hãy nhận bt các chất khí ko màu sau:khí hidro , khí oxy, ko khí?
câu 2:viết PTHH của các phản ứng hidro khử các oxy sau
a)sắt(III)oxit b)đồng (I)oxit
c)thủy ngân(II)oxit d)sắt(II)oxit
e)chì(II)oxit f)oxit sắt từ
C âu 1
Lấy mẫu thử và đánh dấu
Cho lần lượt các khí trên vào que đóm đang cháy
+ Nếu là khí hi đro thì que đóm cháy lửa có màu xanh
+ nếu là oxi thì que đóm cháy mạnh hơn
+ Nếu là ko khí thì nó vân cháy bình thường
Đúng 1
Bình luận (0)
Câu 1 :
Cho tàn que đốm đỏ vào các lọ khí :
- Khí cháy với màu xanh nhạt : H2
- Bùng cháy : O2
- Tắt hẳn : không khí
Câu 2 :
\(Fe_2O_3+3H_2\underrightarrow{t^0}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^0}Cu+H_2O\)
\(HgO+H_2\underrightarrow{t^0}Hg+H_2O\)
\(FeO+H_2\underrightarrow{t^0}Fe+H_2O\)
\(PbO+H_2\underrightarrow{t^0}Pb+H_2O\)
\(Fe_3O_4+4H_2\underrightarrow{t^0}3Fe+4H_2O\)
Đúng 1
Bình luận (0)
3\(H_2\)+ \(Fe_2O_3\) \(--^{t^o}->\) 2Fe + 3H2O
H2 + CuO ---t---> Cu + H2O
H2+ HgO---t---> Hg + H2O
H2 + FeO --t--> Fe+ H2O
H2 + PbO --t--> Pb + H2O
4H2 + Fe3O4 ---t--> 3Fe + 4H2O
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Trong phòng thí nghiệm, người ta dùng khí hidro (H2) để khử 40 gam sắt (III) Oxit (F*e_{2}*O_{3}) a/ Viết phương trình hóa học xãy ra? b/ Tinh khối lượng sắt thu được? c/ Nếu người ta dùng 0.3 mol khí hidro để khử , thì sau phản ứng chất Cho biết : Fe = 56 O = 16, H = 1 nào dư?
a. \(PTHH:3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\)
b. \(n_{Fe_2O_3}=\dfrac{m_{Fe_2O_3}}{M_{Fe_2O_3}}=\dfrac{40}{160}=0,25\left(mol\right)\)
- Mol theo PTHH : \(3:1:2:3\)
- Mol theo phản ứng : \(0,75\leftarrow0,25\rightarrow0,5\rightarrow0,75\)
\(\Rightarrow n_{Fe}=0,5\left(mol\right)\)
\(\Rightarrow m_{Fe}=n_{Fe}.M_{Fe}=0,5.56=28\left(g\right)\)
c. Ta có : \(n_{Fe_2O_3}=0,25\left(mol\right);n_{H_2}=0,3\left(mol\right)\)
Do \(0,25< 0,3\) ⇒ H2 dư.
Đúng 1
Bình luận (0)