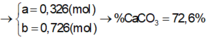Khi phân hủy bằng nhiệt 14,2 gam hỗn hợp CaCO3 và MgCO3 ta thu được 6,6 gam CO2 ( ở đktc). Tính thành phần phần trăm các chất trong hỗn hợp.

Những câu hỏi liên quan
khi phân hủy bằng nhiệt 14,2 gam hỗn hợp X gồm CaCO3 và MgCO3 ta thu được chất rắn Y gồm CaO và MgO và 6,6 gam CO2. Tính thành phần % khối lượng các chất trong hỗn hợp X.
Gọi số mol CaCO3, MgCO3 là a, b (mol)
=> 100a + 84b = 14,2 (1)
\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
a-------------------->a
MgCO3 --to--> MgO + CO2
b---------------------->b
=> a + b = 0,15
=> a = 0,1; b = 0,05
=> \(\left\{{}\begin{matrix}\%m_{CaCO_3}=\dfrac{100.0,1}{14,2}.100\%=70,42\%\\\%m_{MgCO_3}=\dfrac{0,05.84}{14,2}.100\%=29,58\%\end{matrix}\right.\)
Đúng 4
Bình luận (0)
\(n_{CO_2}=\dfrac{6,6}{44}=0,15mol\)
\(CaCO_3\underrightarrow{t^o}CO_2+CaO\)
\(x\) \(\rightarrow\) \(x\)
\(MgCO_3\underrightarrow{t^o}MgO+CO_2\)
\(y\) \(\rightarrow\) \(y\)
\(\Rightarrow\left\{{}\begin{matrix}100x+84y=14,2\\x+y=0,15\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\%m_{CaCO_3}=\dfrac{0,1\cdot100}{14,2}\cdot100\%=70,42\%\)
\(\%m_{MgCO_3}=100\%-70,42\%=29,57\%\)
Đúng 4
Bình luận (0)
Khi phân hủy bằng nhiệt 14,2 gam CaC
O
3
và MgC
O
3
ta thu được 3,36 lít C
O
2
ở đktc. Thành phần phần trăm về khối lượng các chất trong hỗn hợp đầu lần lượt là: A. 29,58% và 70,42% B. 70,42% và 29,58% C. 65% và 35% D. 35% và 65%
Đọc tiếp
Khi phân hủy bằng nhiệt 14,2 gam CaC O 3 và MgC O 3 ta thu được 3,36 lít C O 2 ở đktc. Thành phần phần trăm về khối lượng các chất trong hỗn hợp đầu lần lượt là:
A. 29,58% và 70,42%
B. 70,42% và 29,58%
C. 65% và 35%
D. 35% và 65%
Chọn B
![]()
Gọi số mol của CaC O 3 và MgC O 3 lần lượt là x và y mol

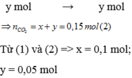
![]()
![]()
Đúng 0
Bình luận (0)
Khi phân hủy bằng nhiệt 14,2g CaCO3 và MgCO3 ta thu được 3,36 lít CO2 ở đktc. Thành phần phần trăm về khối lượng các chất trong hỗn hợp đầu là:
A. 29,58% và 70,42%.
B. 70,42% và 29,58%.
C. 65% và 35%.
D. 35% và 65%
\(n_{CaCO_3}=a\left(mol\right),n_{MgCO_3}=b\left(mol\right)\)
\(m=100a+84b=14.2\left(g\right)\left(1\right)\)
\(n_{CO_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(MgCO_3\underrightarrow{^{^{t^0}}}MgO+CO_2\)
\(\Rightarrow a+b=0.15\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
\(\%CaCO_3=\dfrac{0.1\cdot100}{14.2}\cdot100\%=70.42\%\)
\(\%MgCO_3=29.58\%\)
Đúng 2
Bình luận (0)
Gọi số mol của \(CaCO_3\) và \(MgCO_3\) lần lượt là x và y => \(^m\)hỗn hợp = PT (1)
Phương trình hóa học:
\(CaCO_3\)→→ \(CaO+CO_2\)
x mol → x mol
\(MgCO_3\) →→ \(MgO+CO_2\)
y mol → y mol
=>\(n_{CO_2}\)=PT (2)
Đáp án là B
Đúng 1
Bình luận (1)
Nhiệt phân hoàn toàn 1,84 gam hỗn hợp X gồm MgCO3 và CaCO3 thu được 0,448 lít khí ở đktc. Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp X ban đầu.
Gọi số mol MgCO3, CaCO3 là a, b (mol)
=> 84a + 100b = 1,84 (1)
PTHH: MgCO3 --to--> MgO + CO2
a-------------------->a
CaCO3 --to--> CaO + CO2
b-------------------->b
=> a + b = \(\dfrac{0,448}{22,4}=0,02\) (2)
(1)(2) => a = 0,01 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{0,01.84}{1,84}.100\%=45,65\%\\\%m_{CaCO_3}=\dfrac{0,01.100}{1,84}.100\%=54,35\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Câu 1. Khi nhiệt phân 14,2 gam hỗn hợp CaCo3 và MgCO3 ta thu được 3,36L khí CO2(đktc).Tính thành phần phần trăm khối lượng các chất trong hỗn hợp ban đầu?
Câu 2. Nhiệt phân 40g CaCO3 thì sau phản ứng thu được 5,6L khí ở (đktc).Tính khối lượng các chất thu được sau phản ứng?
Câu 3. Cho 1,6g Đồng 2 oxit tác dụng với 11,76 gam dung dịch H2SO4 có nồng độ 25%.Nồng độ phần trăm của dung dịch muối thu được sau phản ứng?
Đọc tiếp
Câu 1. Khi nhiệt phân 14,2 gam hỗn hợp CaCo3 và MgCO3 ta thu được 3,36L khí CO2(đktc).Tính thành phần phần trăm khối lượng các chất trong hỗn hợp ban đầu?
Câu 2. Nhiệt phân 40g CaCO3 thì sau phản ứng thu được 5,6L khí ở (đktc).Tính khối lượng các chất thu được sau phản ứng?
Câu 3. Cho 1,6g Đồng 2 oxit tác dụng với 11,76 gam dung dịch H2SO4 có nồng độ 25%.Nồng độ phần trăm của dung dịch muối thu được sau phản ứng?
Câu 1:
PTHH: \(CaCO_3\underrightarrow{to}CaO+CO_2\\ xmol:xmol\rightarrow xmol\)
\(MgCO_3\underrightarrow{to}MgO+CO_2\\ymol:ymol\rightarrow ymol\)
Gọi x và y lần lượt là số mol của \(CaCO_3\) và \(MgCO_3\)
\(m_{hh}=m_{CaCO_3}+m_{MgCO_3}\)
\(\Leftrightarrow100x+84y=14,2\left(g\right)\left(1\right)\)
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Leftrightarrow x+y=0,15\left(mol\right)\left(2\right)\)
Giải phương trình (1) và (2) ta được: \(\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m_{CaCO_3}=100.0,1=10\left(g\right)\\m_{MgCO_3}=14,2-10=4,2\left(g\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}\%m_{CaCO_3}=\dfrac{10}{14,2}.100\%=70,4\%\\\%m_{MgCO_3}=100\%-70,4\%=29,6\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
câu 2 :
nCaCO3 = \(\dfrac{40}{100}\) = 0,4 mol
nCO2 = \(\dfrac{5,6}{22,4}\) = 0,25 mol
CaCO3 \(^{to}\rightarrow\)CaO + CO2 \(\uparrow\)
0,25 \(\leftarrow\)0,25
- các chất sau phản ứng : CaO ; CaCO3 dư
mCaO = 0,25 . 56 = 14 g
mCaCO3 = (0,4 - 0,25 ) . 100 = 15 g
Đúng 0
Bình luận (0)
câu 3 :
nCuO = \(\dfrac{1,6}{80}\) = 0,02 mol
nH2SO4 = \(\dfrac{25.11,76}{100.98}\) = 0,03 mol
CuO + H2SO4\(\rightarrow\) CuSO4 + H2O
0,02 \(\rightarrow\)0,02 \(\rightarrow\)0,02
- các dd sau phản ứng gồm : CuSO4 ; H2SO4 dư
C%CuSO4 = \(\dfrac{0,02.160}{1,6+11,76}.100\%\) \(\approx\) 23,95 %
C%H2SO4 = \(\dfrac{\left(0,03-0,02\right).98}{1,6+11,76}.100\%\) \(\approx\) 7,33 %
Đúng 0
Bình luận (2)
Xem thêm câu trả lời
chia một lượng hỗn hợp gồm MgCO3 và CaCO3 làm hai phần bằng nhau.
Phần 1:nhiệt phân hoàn toàn thu được 3.36lít CO2(đktc)
phần 2:hòa tan hết trong dung dịch HCl rồi cô cạn dung dịch sau phản ứng thu được 15,85g hỗn hợp muối khan.
Tính thành phần phần trăm của các chất trong hỗn hợp.
MgCO3 ----> MgO + CO2
CaCO3 -----> CaO + CO2
0,15 (mol) <------------ 0,15 (mol) (1) đây ý nói là tổng lượng mol CO2 = tổng lượng hỗn hợp muối
MgCO3 + HCl -------> MgCl2 + CO2 + H20
CaCO3 + HCl --------> CaCl2 + CO2 + H20
=> n(MgCO3,CaCO3) = n(MgCl2,CaCl2) = 0,15 (mol)
=> M(MgCl2,CaCl2) = 317/3
Sau đó, ta đặt: C (là phần trăm của CaCl2 trong hỗn hợp muối)
1-C (là phần trăm của MgCl2 trong hỗn hợp muối)
Với C là 100% trong hỗn hợp đó
=> 111C + 95x(1-C) = 317/3
Từ đó suy ra: C= 2/3
Vì lượng muối trong hỗn hợp tác dụng với HCl bằng lượng từng muối trong hỗn hợp ban đầu nên
%CaCO3 = 2/3x100% = 66,667%
%MgCO3 = 1/3x100% = 33,33%
Đúng 0
Bình luận (1)
nhiệt phân hoàn toàn 142 gam hỗn hợp X gồm 2 muối CaCO3 và MgCO3. Sau phản ứng thu được 76g chất rắn Y và V ml khí a) Tính giá trị V b) tính thành phần phần trăm theo khối lượng các chất trong chất rắn Y
Áp dụng định luật BTKL :
\(m_{CO_2}=142-76=66\left(g\right)\)
\(n_{CO_2}=\dfrac{66}{44}=1.5\left(mol\right)\)
\(V_{CO_2}=1.5\cdot22.4=33.6\left(l\right)\)
\(n_{CaCO_3}=a\left(mol\right),n_{MgCO_3}=b\left(mol\right)\)
\(m_X=100a+84b=142\left(g\right)\left(1\right)\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(MgCO_3\underrightarrow{^{^{t^0}}}MgO+CO_2\)
\(m_Y=56a+40b=76\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=1,b=0.5\)
\(\%CaO=\dfrac{56\cdot1}{76}\cdot100\%=73.68\%\)
\(\%MgO=100-73.68=26.32\%\)
Đúng 2
Bình luận (0)
PTHH: \(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\uparrow\)
a_______a_____a (mol)
\(MgCO_3\xrightarrow[]{t^o}MgO+CO_2\uparrow\)
b_______b_____b (mol)
Ta lập hệ phương trình: \(\left\{{}\begin{matrix}100a+84b=142\\56a+40b=76\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=1\\b=0,5\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CaO}=\dfrac{56}{76}\cdot100\%\approx73,68\%\\\%m_{MgO}=26,32\%\\V_{CO_2}=\left(1+0,5\right)\cdot22,4=33,6\left(l\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Nhiệt phân hoàn toàn m gam hỗn hợp X gồm CaCO3 và Na2CO3 thu được 11,6 gam chất rắn và 2,24 lít khí (đktc). Thành phần phần trăm khối lượng CaCO3 trong X là A. 6,25%. B. 8,62%. C. 50,2% D. 62,5%.
Đọc tiếp
Nhiệt phân hoàn toàn m gam hỗn hợp X gồm CaCO3 và Na2CO3 thu được 11,6 gam chất rắn và 2,24 lít khí (đktc). Thành phần phần trăm khối lượng CaCO3 trong X là
A. 6,25%.
B. 8,62%.
C. 50,2%
D. 62,5%.
Na2CO3 không bị nhiệt phân, nên 2,24 lít khí sinh ra chính là CO2 do CaCO3 bị nhiệt phân theo phản ứng
![]()
Cách 1:
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
m X = m c h ấ t r ắ n + m C O 2 = 11,6 + 0,1.44 = 16 (gam)
Vậy phần trăm khối lượng của CaCO3 trong hỗn hợp X là:
![]()
Cách 2:
Ta có:
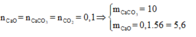
Hỗn hợp rắn thu được gồm CaO và Na2CO3
![]()
![]()
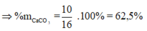
Đáp án D
Đúng 0
Bình luận (0)
Hỗn hợp X gồm MgCO3 và CaCO3. Nung m gam hỗn hợp X ở nhiệt độ cao, thu được chất rắn Y và khí CO2. Cho Y vào nước, thu được chất rắn Z và dung dịch E. Hấp thụ hết lượng khí CO2 trên vào dung dịch E thu được 0,4 m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Thành phần % theo khối lượng của CaCO3 trong hỗn hợp gần nhất với giá trị nào sau đây? A. 60,0% B. 64,8% C. 40% D. 72,6%
Đọc tiếp
Hỗn hợp X gồm MgCO3 và CaCO3. Nung m gam hỗn hợp X ở nhiệt độ cao, thu được chất rắn Y và khí CO2. Cho Y vào nước, thu được chất rắn Z và dung dịch E. Hấp thụ hết lượng khí CO2 trên vào dung dịch E thu được 0,4 m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Thành phần % theo khối lượng của CaCO3 trong hỗn hợp gần nhất với giá trị nào sau đây?
A. 60,0%
B. 64,8%
C. 40%
D. 72,6%