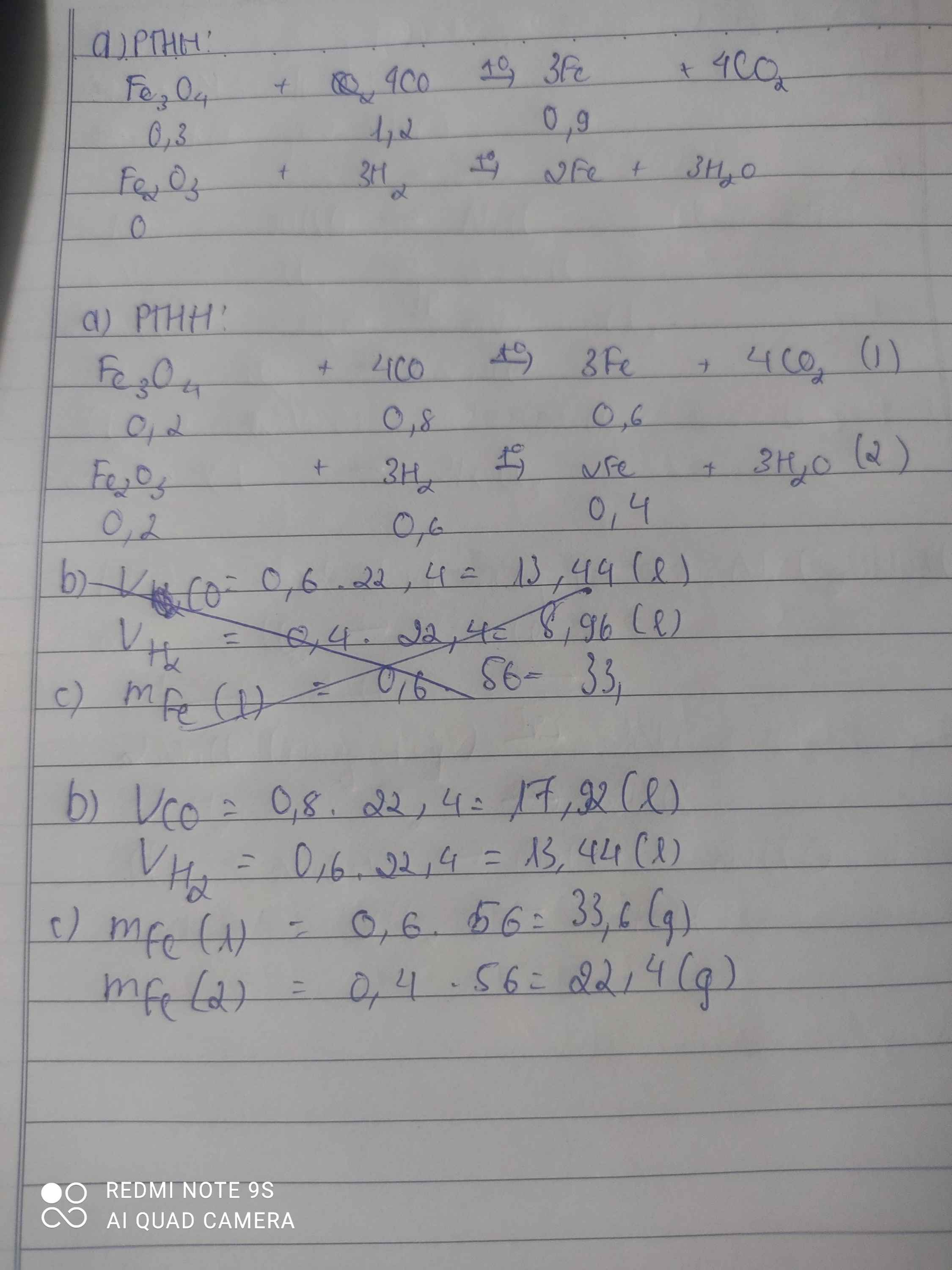Khử 8g oxit sắt bằng khí CO thì người ta dã dùng 4,48l CO ở đktc sau pư thu đc hh khí có tỉ khối so vs khí H2 là 20.tìm ct oxits sắt

Những câu hỏi liên quan
Trong phòng thí nghiệm , người ta dã dùng cacbon oxit CO đẻ khử 0,2 mol FE3O4 cs dùng hidro để khử 0,2 mol FE2O3 ở nhiệt độ cao
a)Viết PTHH
b)Tính số lít khí CO vs H2 ở đktc cần dùng cho mỗi pư;
c)Tính số gam sắt thu được ở mỗi pư hoá học?
(mn giúp mk nha mk đg cần gấp)
a) PTHH:
\(4CO+Fe_3O_4\rightarrow3Fe+4CO_2\left(1\right)\)
\(3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\left(2\right)\)
b) Theo PTPƯ trên ta có:
Muốn khử 1 mol \(Fe_3O_4\) cần 4 mol CO
Muốn khử 0,2 mol \(Fe_3O_4\) cần x mol CO
\(\Rightarrow x=0,2.4=0,8\left(mol\right)\)
\(V_{CO}=0,8.22,4=17,92\left(l\right)\)
Muốn khử 1 mol \(Fe_2O_3\) cần 3 mol H2
Muốn khử 0,2 mol \(Fe_2O_3\) cần y mol H2
\(\Rightarrow y=0,2.3=0,6\left(mol\right)\)
\(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
c) (1): \(n_{Fe}=3n_{Fe_3O_4}=3.0,2=0,6\left(mol\right)\)
\(m_{Fe}=0,6.56=33,6\left(g\right)\)
(2): \(n_{Fe}=2n_{Fe_2O_3}=2.0,2=0,4\left(mol\right)\)
\(m_{Fe}=0,4.56=22,4\left(g\right)\)
Đúng 1
Bình luận (1)
Cho V lít khí CO (đktc) từ từ đi qua ống sứ nung nóng đựng 8g oxit săt đến khi phản ứng xảy ra hoàn toàn thu đc hh khí A có tỉ khối so với hidro = 22. Dẫn hh khí A đi qua dd nước vôi trong dư thu đc 15g kết tủa. Tìm CTHH của oxit sắt và tính V
Đặt CTHH oxit sắt: \(Fe_xO_y\)
\(Fe_xO_y+yCO\rightarrow\left(t^o\right)xFe+yCO_2\)
hh khí A gồm: khí CO2 và có thể có CO (dư)
\(d_{\dfrac{A}{H_2}}=22\) \(\Rightarrow M_A=22.2=44\) \((g/mol)\)
\(\Leftrightarrow\dfrac{44n_{CO_2}+28n_{CO\left(dư\right)}}{n_{CO_2}+n_{CO\left(dư\right)}}=44\)
\(\Leftrightarrow16n_{CO\left(dư\right)}=0\)
\(\Leftrightarrow n_{CO\left(dư\right)}=0\left(mol\right)\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,15 0,15 ( mol )
\(n_{CaCO_3}=\dfrac{15}{100}=0,15\left(mol\right)\)
Bảo toàn O: \(n_{O\left(Fe_xO_y\right)}=n_{CO_2}=0,15\left(mol\right)\)
\(\Rightarrow n_{Fe\left(Fe_xO_y\right)}=\dfrac{8-0,15.16}{56}=0,1\left(mol\right)\)
\(\dfrac{x}{y}=\dfrac{0,1}{0,15}=\dfrac{2}{3}\) \(\Rightarrow\) CTHH: \(Fe_2O_3\)
\(V_{CO}=V_{CO_2}=0,15.22,4=3,36\left(l\right)\)
Đúng 1
Bình luận (0)
Dùng khí CO để khử oxit sắt từ và hidro để khử sắt (III) oxit,khối lượng sắt thu đc là 266g .Khí sinh ra từ các phản ứng trên đc dẫn vào bình đựng nước vôi trong dư thấy xuất hiện 200g kết tủa trắng
a.Tính V các khí CO và H2(đktc) đã tham gia phản ứng
b.Tính khối lượng mỗi oxit đã tham gia phản ứng
Dùng khí CO để khử oxit sắt từ và hidro để khử sắt (III) oxit,khối lượng sắt thu đc là 266g .Khí sinh ra từ các phản ứng trên đc dẫn vào bình đựng nước vôi trong dư thấy xuất hiện 200g kết tủa trắng
a.Tính V các khí CO và H2(đktc) đã tham gia phản ứng
b.Tính khối lượng mỗi oxit đã tham gia phản ứng
\(a,n_{CaCO_3}=\dfrac{200}{100}=2\left(mol\right)\\ Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
2 2
\(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
\(\dfrac{1}{6}\) 2 \(\dfrac{2}{3}\) 2
\(n_{Fe\left(thu.được\right)}=\dfrac{266}{56}=4,75\left(mol\right)\)
\(\rightarrow n_{Fe\left(H_2\right)}=4,75-\dfrac{2}{3}=\dfrac{49}{12}\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(\dfrac{49}{24}\) 6,125 \(\dfrac{49}{12}\)
\(\rightarrow\left\{{}\begin{matrix}V_{CO}=2.22,4=44,8\left(l\right)\\V_{H_2}=6,125.22,4=137,2\left(l\right)\\m_{Fe_2O_3}=\left(\dfrac{1}{6}+\dfrac{49}{24}\right).160=\dfrac{1060}{3}\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
khử 8g sắt (iii) oxit bằng khí hiđro.
a) tính thể tích khí hiđro cần dùng (ở đktc) ? b) tính khối lượng sắt thu được sau phản ứng ?giúp vs ạa, PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
\(n_{H_2}=3n_{Fe_2O_3}=0,15\left(mol\right)\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b, \(n_{Fe}=2n_{Fe_2O_3}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
Đúng 4
Bình luận (0)
a)n\(_{Fe_2O_3}\)=\(\dfrac{m_{Fe_2O_3}}{M_{F_2O_3}}\)=\(\dfrac{8}{160}\)=0,05(m)
PTHH : F\(_2\)O\(_3\) + 3H\(_2\) ➝ 2Fe + 3H\(_2\)O
tỉ lệ :1 3 2 3
số mol: 0,05 0,15 0,1 0,15
V\(_{H_2}\)=n\(_{H_2}\).22,4=0,15.22,4=3,36(l)
b) m\(_{Fe}\)=n\(_{Fe}\).M\(_{Fe}\)=0,1.56=5,6(g)
Đúng 1
Bình luận (0)
\(n_{Fe_2O_3}=\dfrac{m}{M}=\dfrac{8}{56.2+16.3}=0,05\left(mol\right)\)
\(PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
1 3 2 3
0,05 0,15 0,1 0,15
a) \(V_{H_2}=n.24,79=0,15.24,79=3,7185\left(l\right)\)
b) \(m_{Fe}=n.M=0,1.56=5,6\left(g\right).\)
Đúng 0
Bình luận (0)
Khử hoàn toàn 24g hh oxit CuO và FexOy bằng H2 thu được 17,6g 2 kim loại cho hoàn toàn bộ 2 kim loại vào ddHCl dư thu được 4,48l khí H2 ở đktc . Xác định CT của oxi sắt
Gọi số mol CuO, FexOy là a, b (mol)
=> 80a + (56x + 16y)b = 24 (1)
PTHH: CuO + H2 --to--> Cu + H2O
a--------------->a
FexOy + yH2 --to--> xFe + yH2O
b----------------->bx
=> 64a + 56bx = 17,6 (2)
PTHH: Fe + 2HCl --> FeCl2 + H2
bx------------------->bx
=> bx = \(\dfrac{4,48}{22,4}=0,2\) (3)
(2)(3) => a = 0,1 (mol)
(1) => 56bx +16by = 16
=> by = 0,3 (mol)
=> \(\dfrac{bx}{by}=\dfrac{0,2}{0,3}\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH: Fe2O3
Đúng 3
Bình luận (5)
Cho 4,48 khí CO ở đktc từ từ đi qua ống sứ nung nóng đưng 8g một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Hỗn hợp khí thu được sau phản ứng có tỉ khối so với hidro là 20. Tình CTHH của oxit sắt và tính % về thể tích khí CO2 trong hỗn hợp khí sau phản ứng
Cho hỏi chỗ sơ đồ đường chéo 4 và 12 là như nào đấy ạ .___.
Còn cả chỗ suy ra 42x-28y=0
Đúng 0
Bình luận (0)
cho mình hỏi một tẹo nha :trộn khí H2 và khiO2 có tỉ lệ về thể tích là 1:2 hỏi sau phản ứng chất nào hết chất nào đủ thể tích chất du là bao nhiêu mililit
Đúng 0
Bình luận (1)
trong phòng thí nghiệm, ngta dùng khí Hidro(H2) để khử sắt (III) oxit (Fe2O3) và thu đc 22,4 g sắt a) Viết PTHH xảy rab) tính khối lượng sắt (III) oxit đã phản ứng? c) tính thể tích khí hiđro đã tiêu dùng cho PƯ trên(ở đktc)d) để dốt cháy hoàn toàn lượng khí hiđro dùng chơ PƯ trên cần dungfbao nhiêu lít không khí(ở đktc).Biết khí õi chiếm 20%thể tích kkgiúp mik vs mik đag cần gấp mik c.ơn trước
Đọc tiếp
trong phòng thí nghiệm, ngta dùng khí Hidro(H2) để khử sắt (III) oxit (Fe2O3) và thu đc 22,4 g sắt
a) Viết PTHH xảy ra
b) tính khối lượng sắt (III) oxit đã phản ứng?
c) tính thể tích khí hiđro đã tiêu dùng cho PƯ trên(ở đktc)
d) để dốt cháy hoàn toàn lượng khí hiđro dùng chơ PƯ trên cần dungfbao nhiêu lít không khí(ở đktc).Biết khí õi chiếm 20%thể tích kk
giúp mik vs mik đag cần gấp ![]()
![]() mik c.ơn trước
mik c.ơn trước
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,2\left(mol\right)\Rightarrow m_{Fe_2O_3}=0,2.160=32\left(g\right)\)
c, \(n_{H_2}=\dfrac{3}{2}n_{Fe}=0,6\left(mol\right)\Rightarrow V_{H_2}=0,6.22,4=13,44\left(l\right)\)
d, \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=0,3\left(mol\right)\Rightarrow V_{O_2}=0,3.22,4=6,72\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=33,6\left(l\right)\)
Đúng 3
Bình luận (1)
a)
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O$
b) $n_{Fe} = \dfrac{22,4}{56} = 0,4(mol)$
Theo PTHH : $n_{Fe_2O_3} = \dfrac{1}{2}n_{Fe} = 0,2(mol)$
$m_{Fe_2O_3} = 0,2.160 = 32(gam)$
c) $n_{H_2} = \dfrac{3}{2}n_{Fe} = 0,6(mol)$
$V_{H_2} = 0,6.22,4 = 13,44(lít)$
d) $2H_2 + O_2 \xrightarrow{t^o} 2H_2O$
$V_{O_2} = \dfrac{1}{2}V_{H_2} = 6,72(lít)$
$V_{kk} = 6,72 : 20\% = 33,6(lít)$
Đúng 2
Bình luận (1)
Dùng khí CO để khử oxit sắt từ và hidro để khử sắt (III) oxit,khối lượng sắt thu đc là 266g .Khí sinh ra từ các phản ứng trên đc dẫn vào bình đựng nước vôi trong dư thấy xuất hiện 200g kết tủa trắng a.Tính V các khí CO và H2(đktc) đã tham gia phản ứng b.Tính khối lượng mỗi oxit đã tham gia phản ứng
TL:
Tham khảo nhé:

@@@@@@@@@@@@@@@@@@@@
@tuantuthan
HT
TL:
Bạn vào trang cá nhân của mình nhé
@@@@@@@@@@@@@@@@@
@tuantuthan
HT
Xem thêm câu trả lời