Khi cho 0,2 mol kẽm tác dụng với dung dịch có chứa 49 g axit sunfuric
a Viết phương trình phản ứng
B sau phản ứng chất nào còn dư
c Tính thể tích khí Hiđro thu được ở điều kiện tiêu chuẩn
Cho 0,2 mol kẽm tác dụng với dung dịch có chứa 49 g axit sùnuric.
a) Viết phương trình hoá học.
b) Sau phản ứng chất nào còn dư ?
c)Tính thể tích khí hiđro thu được (đktc).
a) \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
b) \(n_{H_2SO_4}=\dfrac{m_{H_2SO_4}}{M_{H_2SO_4}}=\dfrac{49}{98}=0,5\left(mol\right)\)
Theo PTHH ta thấy:
\(\dfrac{n_{Zn}}{1}=\dfrac{0,2}{1}\)
\(\dfrac{n_{H_2SO_4}}{1}=\dfrac{0,5}{1}\)
\(\Rightarrow\dfrac{n_{Zn}}{1}< \dfrac{n_{H_2SO_4}}{1}\)
Vậy axit sunfuric dư
c) Theo PTHH: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=n_{H_2}.22,4=0,2.22,4=4,48\)
a)\(PTHH:Zn+H_{ 2}SO_4\xrightarrow[]{}ZnSO_4+H_2\)
b)\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(m\right)\)
\(PTHH:Zn+H_2SO_4\xrightarrow[]{}ZnSO_4+H_2\)
tỉ lệ :1 1 1 1
số mol bđ :0,2 0,5
ta có tỉ lệ : \(\dfrac{0,2}{1}< \dfrac{0,5}{1}=>H_2SO_4\) \(dư\)
vậy sau phản ứng \(H_2SO_4\) \(dư\)
c)\(PTHH:Zn+H_2SO_4\xrightarrow[]{}ZnSO_4+H_2\)
tỉ lệ :1 1 1 1
số mol :0,2 0,2 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Khi cho 0.2 mol kẽm tác dụng với dung dịch có chứa 49g axit sunfuric. a) Viết phương trính phản ứng? b) Sau phản ứng chất nào còn dư? c) Tính thể tích khí hiđro thu được (ở đktc)?
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\\
pthh:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\
LTL:\dfrac{0,2}{1}< \dfrac{0,5}{1}\)
=> H2SO4 dư
\(n_{H_2}=n_{Zn}=0,2\left(mol\right)\\
V_{H_2}=0,2.22,4=4,48\left(l\right)\)
`a)PTHH:`
`Zn + H_2 SO_4 -> ZnSO_4 + H_2`
`0,2` `0,2` `0,2` `(mol)`
`b)n_[H_2 SO_4]=49/98=0,5(mol)`
Ta có:`[0,2]/1 < [0,5]/1`
`=>H_2 SO_4` dư
`c)V_[H_2]=0,2.22,4=4,48(l)`
cho 2,5 gam nhôm vào bình chứa 0,5 mol dung dịch axit sunfuric loãng
a,Viết phương trình phản ứng
b,chất nào còn dư sau phản ứng Tính khối lượng chất dư
c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
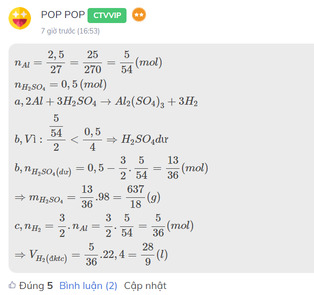
\(n_{Al}=\dfrac{2,5}{27}=\dfrac{25}{270}=\dfrac{5}{54}\left(mol\right)\\ n_{H_2SO_4}=0,5\left(mol\right)\\ a,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b,Vì:\dfrac{\dfrac{5}{54}}{2}< \dfrac{0,5}{4}\Rightarrow H_2SO_4dư\\ b,n_{H_2SO_4\left(dư\right)}=0,5-\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{13}{36}\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=\dfrac{13}{36}.98=\dfrac{637}{18}\left(g\right)\\ c,n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{5}{36}\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=\dfrac{5}{36}.22,4=\dfrac{28}{9}\left(l\right)\)
Tóm tắt:
mAl= 2,5(g)
\(n_{H_2SO_4}=0,5\left(mol\right)\)
---
a) PTHH?
b) Chất dư? m?
c) Thể tích khí sau phản ứng?
Anh ít tóm tắt lắm nên không biết tóm tắt như ri ổn không, vì em cần nên anh tóm tắt ra thử
cho 2,5 gam nhôm vào bình chứa 0,25 mol dung dịch axit sunfuric loãng a,Viết phương trình phản ứng b,chất nào còn dư sau phản ứng Tính khối lượng chất dư c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Mình thấy bạn Thịnh tính lượng dư sai
Đây là bài mình từng làm, bạn tham khảo nhé!
Cho 32,5g kẽm hoàn toàn phản ứng với dung dịch axit clohiddric thu được dung dịch muối kẽm clorua a) Viết Phương Trình phản ứng xảy ra b) Tính thể tích khí hiđro ở điều kiện tiêu chuẩn c) Tính khối lượng muối kẽm sau phản ứng
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có: \(n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,5.22,4=11,2\left(l\right)\)
c, Theo PT: \(n_{ZnCl_2}=n_{Zn}=0,5\left(mol\right)\)
\(\Rightarrow m_{ZnCl_2}=0,5.136=68\left(g\right)\)
Cho 13 g kẽm tác dụng với dung dịch có chứa 49 g axit sunfuric.
a/ Viết PTHH ?
b/ Sau phản ứng chất nào còn dư ? Tính khối lượng chất còn dư ?
c/ Tính thể tích khí hidro thu được ( đktc)?
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,2\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\\m_{H_2SO_4\left(dư\right)}=0,3\cdot98=29,4\left(g\right)\end{matrix}\right.\)
nH2SO4=0,5(mol)
nZn=0,2(mol)
a) PTHH: Zn + H2SO4 -> ZnSO4 + H2
ta có: 0,5/1 > 0,2/1
=> Zn hết, H2SO4 dư, tính theo nZn
b) m(H2SO4 dư)= (0,5-0,2).98=29,4(g)
c) nH2= nZn=0,2(mol)
=>V(H2,đktc)=0,2.22,4=4,48(l)
Cho 2,4 g kim loại Mg tác dụng vừa đủ với 400 ml dung dịch axit clohiđric ? a, viết phương trình hóa học xảy ra b, tính thể tích khí Hiđro thu được trong điều kiện tiêu chuẩn c, tính nồng độ mol của dung dịch muối tạo thành sau khi phản ứng biết rằng thể tích của dung dịch thay đổi không đáng kể
Cho 19,5g tác dụng hết với 200ml dung dịch HCl
a) Viết phương trình phản ứng
b) TÍnh thể tích khí hiđro thu được ở điều kiện tiêu chuẩn
c) Tính C% của dung dịch axit đã dùng
19,5g gì :) ?, với cả đề cho Vdd thì sao tính đuợc C% :))
cho kẽm tác dụng với dung dịch HCl dư sau phản ứng thu được ZnCl2 và 2,24 lít khí hiđro ở điều kiện tiêu chuẩn. viết phương trình phản ứng xảy ra và tính khối lượng muối tạo thành sau phản ứng
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,1<--0,1
=> mZnCl2 = 0,1.136 = 13,6 (g)