oxi hóa hoàn toàn 5,4g kim loại A(III) thu được 10,2g oxit. Xác định kim loại A, viết công thức hóa học của oxit.

Những câu hỏi liên quan
Bài 7: Đốt cháy hết 5,4g một kim loại hóa trị (III) trong khí oxi dư, thu được 10,2g oxit. Xác định công thức hóa học và gọi tên oxit trên?
Gọi kim loại cần tìm là R
\(n_R=\dfrac{5,4}{M_R}\left(mol\right)\)
PTHH: 4R + 3O2 --to--> 2R2O3
\(\dfrac{5,4}{M_R}\)--------------->\(\dfrac{2,7}{M_R}\)
=> \(\dfrac{2,7}{M_R}\left(2.M_R+48\right)=10,2\)
=> MR = 27 (g/mol)
=> R là Al
CTHH của oxit: Al2O3 (Nhôm oxit)
Đúng 4
Bình luận (1)
Cho 3,36 lit khí oxi (ở đktc) phản ứng hoàn toàn với 1 kim loại hóa trị III thu được 10,2g oxit. Xác định tên kim loại.
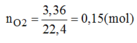
Gọi A là kí hiệu của kim loại có hóa trị III, M A là nguyên tử khối của A.
Ta có PTHH:

Theo PTHH trên ta có:
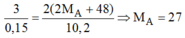
Vậy A là nhôm.
Đúng 0
Bình luận (0)
Câu 1: Cho 5,4g một kim loại R(hóa trị III) tác dụng với Oxi thu được 10,2g. Xác định khối lượng R và CTHH của oxit
Câu 2: Oxit hóa 16,8 lít khí SO2(ĐKTC) a) Viết PTHH b) Tính VO2 c)Tìm hiệu suất của phản ứng
Bài 1 :
\(m_{O_2}=10.2-5.4=4.8\left(g\right)\)
\(n_{O_2}=\dfrac{4.8}{32}=0.15\left(mol\right)\)
\(4R+3O_2\underrightarrow{^{^{t^0}}}2R_2O_3\)
\(0.2......0.15\)
\(M_R=\dfrac{5.4}{0.2}=27\left(\dfrac{g}{mol}\right)\)
=> R là : Al
CTHH : Al2O3
Đúng 3
Bình luận (0)
Câu 2:
a) nSO2=0,75(mol)
PTHH: \(SO2+\dfrac{1}{2}O2⇌\left(to,xt\right)SO3\)
nO2=nSO2/2=0,75/2=0,375(mol)
=>V(O2,ĐKTC)=0,375.22,4=8,4(l)
c) Tìm hiệu suất là sao em?
Đề chưa chặt chẽ
Đúng 0
Bình luận (0)
BÀI 1 CÁCH KHÁC:
PTHH: 4 R + 3 O2 -to-> 2 R2O3
Theo PT: 4M(R)________4M(R)+96(g)
Theo đề): 5,4__________10,2(g)
Theo PTHH và đề bài ta có:
10,2.4M(R)=5,4.(4M(R)+96)
<=>19,2M(R)=518,4
<=>M(R)=27(g/mol)
=>R(III) cần tím là Nhôm (Al=27)
=> CTHH oxit: Al2O3
Chúc em học tốt!
Đúng 1
Bình luận (0)
cho một kim loại R hóa trị 3 tác dụng hoàn toàn với 3,36l khí oxi (đktc) thu được 10,2g oxit . xác định kim loại R
PTHH : 4R + 3O2 ---> 2R2O3
nO2 = 0,15 ( mol )
nR = 4/3 . nO2 = 0,2 ( mol )
nR2O3 = 0,1 ( mol )
=> M = 10,2 : 0,1 = 102 ( đvC )
Ta có:
R.2 + 16.3 = 102
-> R = 27 ( Al )
Đúng 1
Bình luận (0)
\(n_{O2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(4R+3O_2\underrightarrow{t^o}2R_2O_3|\)
4 3 2
0,2 0,15
Theo định luật bảo toàn khối lượng :
\(m_R+m_{O2}=m_{R2O3}\)
\(m_R+\left(0,15.32\right)=10,2\)
⇒ \(m_R=10,2-4,8=5,4\left(g\right)\)
\(n_R=\dfrac{0,15.4}{3}=0,2\left(mol\right)\)
⇒ \(M_R=\dfrac{5,4}{0,2}=27\) (g/mol)
Vậy kim loại R là nhôm
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Gọi công thức là R
n O2=\(\dfrac{3,36}{22,4}\)=0,15 mol
4R +3O2-to>2R2O3
4--------3-------2(2MR+48)
0,15mol----10,2g
=>\(\dfrac{3}{0,15}\dfrac{2\left(2MR+48\right)}{10,2}\)
=>MR=27 đvC
=>R là nhôm (Al)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Khử hoàn toàn 16g một oxit kim loại có hóa trị III bằng hidro thì thu được một chất rắn X và 5,4g nước a. Viết ptpư và xác định CTPT của oxit kim loại có hóa trị III đó
b. Cho 10g hỗn hợp gồm X và Cu tác dụng với dd HCl dư thu được2,24lit khí ĐKC. Tính % khối lượng Cu có trong hỗn hợp?
Cho 5,4g kim loại có hóa trị không đổi phản ứng với O2 tạo ra 10,2g oxit. Xác định tên của kim loại và công thức oxit của nó?
Đốt cháy hoàn toàn 19,2 g đồng?
a) tính thể tích oxi cần dùng (đktc)
b) cho kim loại sắt chưa rõ hóa trị vào lượng khí Oxi trên thu được 16 g oxit,xác định công thức hóa học của oxit
a, \(n_{Cu}=\dfrac{19,2}{64}=0,3\left(mol\right)\)
PT: \(2Cu+O_2\underrightarrow{t^o}2CuO\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Cu}=0,15\left(mol\right)\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)
b, Gọi CTHH của oxit là FexOy.
Có: nO (trong oxit) = 2nO2 = 0,3 (mol)
⇒ mFe = 16 - mO = 16 - 0,3.16 = 11,2 (g) \(\Rightarrow n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
⇒ x:y = 0,2:0,3 = 2:3
Vậy: CTHH cần tìm là Fe2O3.
Đúng 2
Bình luận (0)
TD1: để oxi hóa hoàn toàn một kim loại M hóa trị II thành oxit phải dung một lượng oxi bằng 40% lượng kim loại đã dung. Xác định kim loại M và viết công thức của oxit. TD 3: Đốt cháy hoàn toàn 2,3 gam hợp chất A người ta thu được 4,4 gam CO2 và 2,7 gam nước. Lập CTHH của A biết CTHH của A trùng với công thức đơn giản. TD4: Đốt cháy hoàn toàn khí A ( có 2 nguyên tố ) trong kh...
Đọc tiếp
TD1: để oxi hóa hoàn toàn một kim loại M hóa trị II thành oxit phải dung một lượng oxi bằng 40% lượng kim loại đã dung. Xác định kim loại M và viết công thức của oxit. TD 3: Đốt cháy hoàn toàn 2,3 gam hợp chất A người ta thu được 4,4 gam CO2 và 2,7 gam nước. Lập CTHH của A biết CTHH của A trùng với công thức đơn giản. TD4: Đốt cháy hoàn toàn khí A ( có 2 nguyên tố ) trong không khí , sau phản ứng thu được khí P2O5và nước . Biết rằng khí A nặng hơn khí oxi 1,0625 lần. Xác định công thức của A. TD5: Nhiệt phân 79 gam thuốc tím. Sau phản ứng thu được hỗn hợp chất rắn X có khối lượng là 72,6 gam. a) Tính hiệu suất của phản ứng. b) Tính thành phần % khối lượng mỗi chất trong X. TD7: Hỗn hợp X gồm CO2và CO, với thành phần % về số mol của CO2 là 75% . Tính tỉ khối hơi của của hỗn hợp khí X so với khí hiđro. TD8: Hỗn hợp A gồm N2 và O2 . Tìm tỉ khối của A đối với H2 nếu: a) N2 và O2 có cùng thể tích. b) N2 và O2 có cùng khối lượng. (đàn anh , đàn chị giúp e làm hết đk ạ )
Bài 1 :
Coi $m_{O_2} = 32(gam) \Rightarrow m_M = \dfrac{32}{40\%} = 80(gam)$
$n_{O_2} = 1(mol)$
$2M + O_2 \xrightarrow{t^o} 2MO$
$n_M = 2n_{O_2} = 2(mol)$
$M_M = \dfrac{80}{2} = 40$
Vậy M là kim loại Canxi
CTHH oxit là CaO
Đúng 2
Bình luận (0)
TD4 :
Đặt : CTHH là : \(H_xP_y\)
\(M_A=1.0625\cdot32=34\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow xH+yP=34\)
\(\Rightarrow x+31y=34\)
Chỉ có duy nhất một cặp nghiệm thỏa mãn :
\(x=3,y=1\)
\(CT:PH_3\)
Đúng 4
Bình luận (0)
TD3 :
\(n_{CO_2}=\dfrac{4.4}{44}=0.1\left(mol\right)\Rightarrow n_C=0.1\left(mol\right)\)
\(n_{H_2O}=\dfrac{2.7}{18}=0.15\left(mol\right)\Rightarrow n_H=2\cdot0.15=0.3\left(mol\right)\)
\(m_O=m_A-m_C-m_H=2.3-0.1\cdot12-0.3=0.8\left(g\right)\)
\(\Rightarrow n_O=\dfrac{0.8}{16}=0.05\left(mol\right)\)
Ta có :
\(n_C:n_H:n_O=0.1:0.3:0.05=2:6:1\)
CTHH của A là : \(C_2H_6O\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
1.Đốt cháy hoàn toàn 10,8g môt kim loại chưa rõ hóa trị, sau phản ứng thu đươhc 20,4g một oxit. Hãy xác định công thức hóa học của kim loại.2.Đốt cháy hoàn toàn 8,4g môt kim loại chưa rõ hóa trị, sau phản ứng thu được 16,6 g một oxit. Hãy xác định công thức hóa học của kim loại3.Cho 2,7g Al vào đung dịch có chứa 16,1g HCla.Viết PTHH của phản ứngb.Chất nào dư? Tính khối lượng dư.c.Nếu dùng toàn bộ thể tích khí H2 trên để khử 30g Đồng(II) oxit, hãy tính khối lượng chất rắn thu được sau phản ứng.gi...
Đọc tiếp
1.Đốt cháy hoàn toàn 10,8g môt kim loại chưa rõ hóa trị, sau phản ứng thu đươhc 20,4g một oxit. Hãy xác định công thức hóa học của kim loại.
2.Đốt cháy hoàn toàn 8,4g môt kim loại chưa rõ hóa trị, sau phản ứng thu được 16,6 g một oxit. Hãy xác định công thức hóa học của kim loại
3.Cho 2,7g Al vào đung dịch có chứa 16,1g HCl
a.Viết PTHH của phản ứng
b.Chất nào dư? Tính khối lượng dư.
c.Nếu dùng toàn bộ thể tích khí H2 trên để khử 30g Đồng(II) oxit, hãy tính khối lượng chất rắn thu được sau phản ứng.
giúp em sáng 6h nộp rồi ạ
Câu 1:
Giả sử KL là A có hóa trị n.
PT: \(4A+nO_2\underrightarrow{t^o}2A_2O_n\)
Ta có: \(n_A=\dfrac{10,8}{M_A}\left(mol\right)\), \(n_{A_2O_n}=\dfrac{20,4}{2M_A+16n}\left(mol\right)\)
Theo PT: \(n_A=2n_{A_2O_3}\Rightarrow\dfrac{10,8}{M_A}=\dfrac{2.20,4}{2M_A+16n}\Rightarrow M_A=9n\left(g/mol\right)\)
Với = 3 thì MA = 27 (g/mol) là thỏa mãn.
Vậy: A là Al.
Câu 2:
Giả sử KL cần tìm là A có hóa trị n.
PT: \(4A+nO_2\underrightarrow{t^o}2A_2O_n\)
Ta có: \(n_A=\dfrac{8,4}{M_A}\left(mol\right)\), \(n_{A_2O_n}=\dfrac{16,6}{2M_A+16n}\left(mol\right)\)
Theo PT: \(n_A=2n_{A_2O_n}\Rightarrow\dfrac{8,4}{M_A}=\dfrac{2.16,6}{2M_A+16n}\Rightarrow M_A=\dfrac{336}{41}n\)
→ vô lý
Bạn xem lại đề câu này nhé.
Câu 3:
a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{16,1}{36,5}=\dfrac{161}{365}\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{\dfrac{161}{365}}{6}\), ta được HCl dư.
THeo PT: \(n_{HCl\left(pư\right)}=3n_{Al}=0,3\left(mol\right)\)
\(\Rightarrow n_{HCl\left(dư\right)}=\dfrac{161}{365}-0,3=\dfrac{103}{730}\left(mol\right)\Rightarrow m_{HCl\left(dư\right)}=\dfrac{103}{365}.36,5=5,15\left(g\right)\)
c, \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\), \(n_{CuO}=\dfrac{30}{80}=0,375\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,375}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{CuO\left(pư\right)}=n_{Cu}=n_{H_2}=0,15\left(mol\right)\Rightarrow n_{CuO\left(dư\right)}=0,375-0,15=0,225\left(mol\right)\)
⇒ m chất rắn = mCu + mCuO (dư) = 0,15.64 + 0,225.80 = 27,6 (g)
Đúng 1
Bình luận (0)
























