Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2 g lưu huỳnh kết hợp với 3 g oxi.

Những câu hỏi liên quan
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2g lưu huỳnh kết hợp với 3g oxi.
Số mol của nguyên tử lưu huỳnh là: 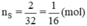
Số mol của nguyên tử oxi là: 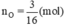
Ta có: 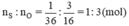
⇒ Trong một phân tử lưu huỳnh trioxit có 1 nguyên tử S và có 3 nguyên tử O.
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3.
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2 g lưu huỳnh kết hợp với 3 g oxi.
Số mol của nguyên tử lưu huỳnh là: nS = (mol)
Số mol của nguyên tử oxi là: =
mol
Ta có: =
:
=
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3
Đúng 0
Bình luận (1)
Số mol của nguyên tử lưu huỳnh là: nS = (mol)
Số mol của nguyên tử oxi là: =
mol
Ta có: =
:
=
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3
Đúng 1
Bình luận (1)
Gọi công thức lưu huỳnh oxi là: SxOy
Ta có tỉ lệ:
x ÷ y = 2/32÷3/16=0,0625:0,1825=1:3
-> Công thức hóa học là: SO3
Đúng 1
Bình luận (2)
Xem thêm câu trả lời
hãy tìm công thức đơn giản nhất của một loại lưu huỳnh oxit biết rằng trong oxit này có 2g lưu huỳnh kết hợp vs 3g oxi
Gọi công thức của oxit là SxOy.
PTHH: \(2xS+yO_2\underrightarrow{t^o}2S_xO_y\)
Ta có: nS = 2/32 = 0,0625 mol; nO2 = 3/32 = 0,09375
\(\Rightarrow\dfrac{x}{y}=\dfrac{n_S}{2n_{O2}}=\dfrac{0,0625}{0,1875}=\dfrac{1}{3}\)
Công thức của oxit là SO3.
Đúng 0
Bình luận (0)
Hãy tìm công thức đơn giản nhất của một loại lưu huỳnh oxit, biết rằng trong oxit này có 2g lưu huỳnh kết hợp vs 3g oxi
Gọi CTHH lưu huỳnh oxit là SxOy
nS=2/32=1/16(mol)
nO=3/16(mol)
=>tỉ lệ nS/nO=1/16:3/16=1:3
=>CTHH:SO3
Đúng 0
Bình luận (0)
Bài 4: hãy tìm CTHH đơn giản nhất của một loại lưu huỳnh oxit, biết rằng trong oxit này có 2g lưu huỳnh kết hợp với 3g oxi
Gọi công thức là SxOy (x,y \(\in\) N*)
x : y = \(\dfrac{2}{32}:\dfrac{3}{16}\)
= 0,0625 : 0,1875
= 1 : 3
\(\rightarrow\) x = 1, y = 3
Vậy công thức là SO3
Đúng 0
Bình luận (0)
Gọi CTHH dạng chung là SxOy
Ta có x:y=\(\dfrac{2}{32}:\dfrac{3}{16}=1:3\)
=>x=1;y=3
Vậy CTHH:SO3
Chúc bạn học tốt![]()
Đúng 0
Bình luận (0)
Câu 4 (1 điểm): Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%. Biết oxit này có khối lượng mol phân tử là 64 g/mol. Hãy tìm công thức hóa học của oxit đó.
Cho nguyên tử khối: O=16, Cu=64, Mg=24, Fe=56, Cl=35,5, Ag =108, N=14
\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=\dfrac{64.50}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2
Đúng 0
Bình luận (2)
Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%.Biết oxit này có khối lượng mol phân tử là 64g/mol.Hãy tìm công thức hóa học của oxit đó.
Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)
Đúng 2
Bình luận (2)
Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%.Hãy tìm công thức hóa học của oxit đó.
Gọi CTHH của oxit là $S_xO_y$
Ta có :
$\dfrac{32x}{50} = \dfrac{16y}{50} \Rightarrow \dfrac{x}{y} = \dfrac{1}{2}$
Vậy CTHH là $SO_2$
Đúng 0
Bình luận (0)
hãy tìm cthh đơn giản nhất của một loại lưu huỳnh oxit, biết rằng trong oxit này có 2 gam s kết hợp với 3 gam oxi
mai mình nộp rồi
Gọi CTHH của oxit là SxOy
Ta có: x: y = \(\dfrac{2}{32}:\dfrac{3}{16}=1:3\)
=> x = 1; y = 3
Vậy CTHH: SO3
Đúng 0
Bình luận (0)
Gọi CTHH của oxit là SxOy
Ta có: x: y = 232:316=1:3232:316=1:3
=> x = 1; y = 3
Vậy CTHH: SO3
Đúng 0
Bình luận (0)


























