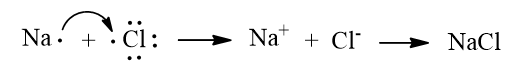Trong tự nhiên, một số phi kim như carbon, nitrogen, oxygen tồn tại ở cả dạng đơn chất và hợp chất, còn các halogen đều chỉ tồn tại ở dạng hợp chất. Vì sao có sự khác biệt này?
Bài 21: Nhóm halogen
Mở đầu (SGK Kết nối tri thức và cuộc sống trang 104)
Thảo luận (2)
Câu hỏi 1 (SGK Kết nối tri thức và cuộc sống trang 105)
Kể tên một số hợp chất phổ biến của halogen trong tự nhiên.
Thảo luận (2)Hướng dẫn giải
Hoạt động 1 (SGK Kết nối tri thức và cuộc sống trang 105)
Tra cứu số liệu Bảng 6.1, Bảng 6.2 và Hình 6.2 để hoàn thành bảng mô tả một số đặc điểm cấu tạo của các nguyên tử halogen theo mẫu sau:Nguyên tửLớp electron ngoài cùngBán kính nguyên tửĐộ âm điệnFluorine???Chlorine???Bromine???Iodine???Từ bảng số liệu thu được, hãy:a) Giải thích tại sao nguyên tử halogen có xu hướng nhận 1 electron từ nguyên tử kim loại, hoặc góp chung 1 electron với nguyên tử phi kim, để hình thành liên kết.b) Nêu và giải thích xu hướng biến đổi bán kính nguyên tử, độ âm điện c...
Đọc tiếp
Tra cứu số liệu Bảng 6.1, Bảng 6.2 và Hình 6.2 để hoàn thành bảng mô tả một số đặc điểm cấu tạo của các nguyên tử halogen theo mẫu sau:
Nguyên tử | Lớp electron ngoài cùng | Bán kính nguyên tử | Độ âm điện |
Fluorine | ? | ? | ? |
Chlorine | ? | ? | ? |
Bromine | ? | ? | ? |
Iodine | ? | ? | ? |
Từ bảng số liệu thu được, hãy:
a) Giải thích tại sao nguyên tử halogen có xu hướng nhận 1 electron từ nguyên tử kim loại, hoặc góp chung 1 electron với nguyên tử phi kim, để hình thành liên kết.
b) Nêu và giải thích xu hướng biến đổi bán kính nguyên tử, độ âm điện của các nguyên tử halogen. Từ đó dự đoán xu hướng biến đổi tính oxi hóa từ F đến I
c) Dựa vào cấu hình electron lớp ngoài cùng và độ âm điện, giải thích tại sao nguyên tử fluorine chỉ có số oxi hóa -1 trong các hợp chất?
Thảo luận (1)Hướng dẫn giải
Nguyên tử
Lớp electron ngoài cùng
Bán kính nguyên tử
Độ âm điện
Fluorine
2s22p6
73
3,98
Chlorine
3s23p6
103
3,16
Bromine
4s24p6
119
2,96
Iodine
5s25p6
142
2,66
a)
- Nguyên tử halogen có 7 electron ở lớp ngoài cùng, dễ nhận thêm 1 electron để đạt được cấu hình electron bền cùng khí hiếm gần nhất.
+ Khi nguyên tử halogen liên kết với kim loại => Khi đó kim loại sẽ nhường electron và nguyên tử halogen sẽ nhận 1 electron để trở thành ion mang điện tích âm
+ Khi nguyên tử halogen liên kết với phi kim => 2 phi kim kết hợp với nhau tạo thành phân tử, chúng sẽ góp electron để tạo thành các cặp electron dùng chung => Halogen sẽ góp chung 1 electron để đạt cấu hình electron bền vững
b)
- Bán kính nguyên tử: Đi từ trên xuống dưới, số lớp electron tăng => Lực hút giữa hạt nhân và lớp electron ngoài cùng giảm dần => Bán kính tăng dần
- Độ âm điện: Đi từ trên xuống dưới, số lớp electron tăng => Lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm nên độ âm điện giảm
- Từ F đến I, độ âm điện giảm dần => Khả năng hút (nhận) electron giảm dần => Tính oxi hóa giảm dần
c)
- Nguyên tử fluorine có 7 electron ở lớp ngoài cùng và có độ âm điện lớn nhất
=> Khi tham gia liên kết hóa học, fluorine chỉ nhận 1 electron từ các nguyên tử khác
=> Fluorine chỉ có số oxi hóa -1 trong các hợp chất
(Trả lời bởi Mai Trung Hải Phong)
Hoạt động 2 (SGK Kết nối tri thức và cuộc sống trang 105)
Tham khảo Bài 12 (Liên kết cộng hóa trị) hãy:
a) Mô tả sự hình thành liên kết trong phân tử halogen bằng công thức electron
b) Liên kết trong phân tử halogen là liên kết cộng hóa trị phân cực hay không phân cực?
c) Dựa vào bán kính nguyên tử (Hình 6.2), hãy dự đoán xu hướng biến đổi độ dài liên kết trong dãy các phân tử halogen.
Thảo luận (1)Hướng dẫn giảia) Khi 2 nguyên tử halogen liên kết với nhau, mỗi nguyên tử sẽ góp 1 electron tạo thành 1 cặp electron dùng chung
b)
- Trong phân tử halogen, liên kết hình thành giữa 2 nguyên tử giống nhau
=> Hiệu độ âm điện = 0, cặp electron dùng chung không bị hút lệch về phía nguyên tử nào
=> Liên kết cộng hóa trị không phân cực
c)
- Độ dài liên kết là khoảng cách giữa 2 hạt nhân của 2 nguyên tử
- Đi từ F đến I, bán kính nguyên tử tăng dần
=> Khoảng cách giữa 2 hạt nhân tăng dần
=> Độ dài liên kết trong dãy các phân tử halogen tăng dần
(Trả lời bởi Mai Trung Hải Phong)
Câu hỏi 1 (SGK Kết nối tri thức và cuộc sống trang 106)
Xác định số oxi hóa của chlorine trong các chất sau: Cl2, HCl, HClO, HClO2, HClO3, HClO4.
Thảo luận (2)Hướng dẫn giải
Câu hỏi 2 (SGK Kết nối tri thức và cuộc sống trang 107)
Trong tự nhiên, các nguyên tố halogen tồn tại ở dạng hợp chất. Viết công thức một vài hợp chất của halogen thường được dùng trong thực tế.
Thảo luận (2)Hướng dẫn giải
Câu hỏi 3 (SGK Kết nối tri thức và cuộc sống trang 106)
Nguyên tử halogen có thể nhận 1 electron từ nguyên tử kim loại hoặc góp chung electron với nguyên tử phi kim.
Mô tả sự hình thành liên kết trong phân tử NaCl và HCl để minh họa.
Thảo luận (2)Hướng dẫn giảiMô tả sự hình thành liên kết trong phân tử NaCl: Nguyên tử Na sẽ nhường 1 electron để tạo thành \(Na^+\), nguyên tử Cl sẽ nhận 1 electron để tạo thành \(Cl^-\)
=>Na+ và Cl- sẽ kết hợp với nhau để tạo thành liên kết ion
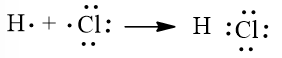
Mô tả sự hình thành liên kết trong phân tử HCl: Nguyên tử H và nguyên tử Cl liên kết với nhau bằng cách mỗi nguyên tử góp 1 electron. Khi đó, nguyên tử hidro có 2e(thỏa mãn cấu hình khí hiếm gần nhất của H là Heli), nguyên tử Cl có 8e(thỏa mãn cấu hình khí hiếm gần nhất của Cl là Ar), thỏa mãn quy tắc bát tứ
(Trả lời bởi Nguyễn Lê Phước Thịnh)
Câu hỏi 4 (SGK Kết nối tri thức với cuộc sống trang 107)
Từ Bảng 21.2, nhận xét xu hướng biến đổi nhiệt độ nóng chảy, nhiệt độ sôi của các halogen và giải thích.
Thảo luận (1)Hướng dẫn giảiNhiệt độ nóng chảy, nhiệt độ sôi tăng từ F2 đến I2 do:
- Tương tác van der Waals giữa các phân tử tăng.
- Khối lượng phân tử tăng.
(Trả lời bởi Người Già)
Câu hỏi 5 (SGK Kết nối tri thức và cuộc sống trang 108)
Xác định chất oxi hóa, chất khử trong phản ứng sodium và iron với chlorine, dùng mũi tên chỉ rõ sự nhường electron từ chất khử sang chất oxi hóa.
Thảo luận (1)Hướng dẫn giải\(2Na+Cl_2\rightarrow2NaCl\)(ĐK: t độ)
Chất khử: Na
Chất oxi hóa: Cl2
=>Na nhường electron sang Cl
\(2Fe+3Cl_2\rightarrow3FeCl_2\)
Chất khử: Fe
Chất oxi hóa: Cl2
=>Fe nhường electron sang Cl2
(Trả lời bởi Nguyễn Lê Phước Thịnh)
Hoạt động 3 (SGK Kết nối tri thức và cuộc sống trang 108)
Xét các phản ứng hóa học: H2(g) + X2(g) → 2HX(g) (X là các halogen)Tra số liệu trong Bảng 12.2 để:1. Giải thích xu hướng phản ứng của các đơn chất halogen với hydrogen theo khả năng hoạt động của các halogen2. Dựa vào số liệu năng lượng liên kết H-X, giải thích xu hướng phản ứng giảm dần từ F2 đến I2
Đọc tiếp
Xét các phản ứng hóa học: H2(g) + X2(g) → 2HX(g) (X là các halogen)
Tra số liệu trong Bảng 12.2 để:
1. Giải thích xu hướng phản ứng của các đơn chất halogen với hydrogen theo khả năng hoạt động của các halogen
2. Dựa vào số liệu năng lượng liên kết H-X, giải thích xu hướng phản ứng giảm dần từ F2 đến I2

Thảo luận (1)Hướng dẫn giải1.
- Từ F2 đến I2, tính oxi hóa của các halogen giảm dần
=> Khả năng hoạt động của các đơn chất halogen giảm dần
=> Xu hướng phản ứng với hydrogen giảm dần
2.
- Dựa vào Bảng 12.2 ta nhận thấy: Từ F đến I, năng lượng liên kết của halogen với hydrogen giảm dần
=> Khả năng halogen liên kết với hydrogen giảm dần
=> Xu hướng phản ứng của các đơn chất halogen với hydrogen giảm dần từ F2 đến I2
(Trả lời bởi Mai Trung Hải Phong)