- Các nguyên tố nhóm halogen có 7 electron ở lớp ngoài cùng
=> Có xu hướng nhận 1 electron (liên kết ion) hoặc bỏ ra 1 electron để góp chung (liên kết cộng hóa trị) để có cấu hình electron bền vững của khí hiếm
- Các nguyên tố nhóm halogen có 7 electron ở lớp ngoài cùng
=> Có xu hướng nhận 1 electron (liên kết ion) hoặc bỏ ra 1 electron để góp chung (liên kết cộng hóa trị) để có cấu hình electron bền vững của khí hiếm
Từ cấu tạo phân tử halogen và đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, nhận xét xu hướng hình thành liên kết của nguyên tử halogen trong các phản ứng hóa học.
Viết cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen.
Trong phản ứng với kim loại, nhận xét sự biến đổi số oxi hóa của nguyên tử các nguyên tố halogen và viết các quá trình khử xảy ra.
Dựa vào điều kiện phản ứng với hydrogen và giá trị năng lượng liên kết của phân tử H – X, giải thích khả năng phản ứng của các halogen với hydrogen.
Nhận xét vai trò của halogen trong đời sống, sản xuất và y tế.
Trong đèn halogen, bao quanh dây tóc làm bằng wolfram là các khí hiếm như krypton, xenon và một lượng nhỏ halogen như bromine hoặc iodine, giúp tăng tuổi thọ và duy trì độ trong suốt của vỏ bóng đèn. Đèn halogen được sử dụng trong các máy sưởi, lò nướng, bếp halogen hồng ngoại,… do đặc điểm tỏa nhiều nhiệt.
Nhu cầu về nước sạch là thiết yếu và cấp bách của con người, nước sạch được dùng cho sinh hoạt, ăn uống và sản xuất. Cách xử lí nước phổ biến hiện nay là sử dụng nước chlorine hoặc các chất có chứa chlorine để khử trùng nước
Nhóm halogen gồm những nguyên tố nào? Halogen có những tính chất và ứng dụng trong lĩnh vực nào?

Từ các thông tin và quan sát Hình 17.2, nhận xét dạng tồn tại của các nguyên tố halogen trong tự nhiên.
Tìm hiểu thêm những ứng dụng khác của halogen trong thực tế.
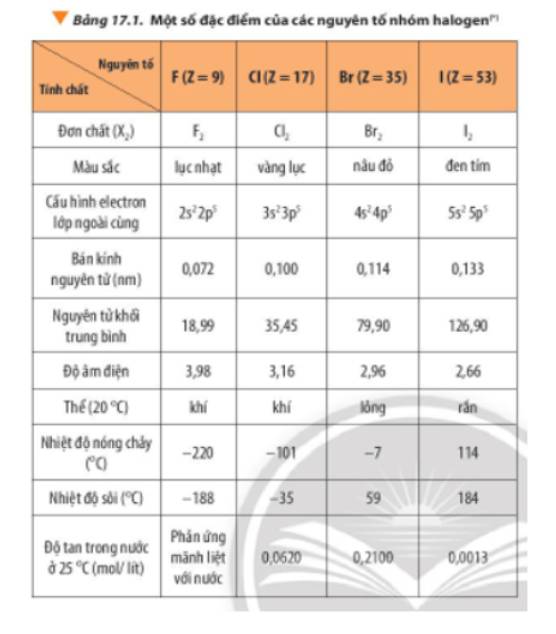
Dựa vào Bảng 17.1, nhận xét sự biến đổi về màu sắc, thể các chất ở điều kiện thường, nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen.