- Nguyên tử Cl có 7 electron ở lớp ngoài cùng => Có xu hướng nhận thêm 1 electron để đạt cấu hình electron bền vững của khí hiếm Ar
=> Khi hình thành phân tử Cl2, mỗi nguyên tử sẽ góp 1 electron để tạo thành 1 cặp electron chung
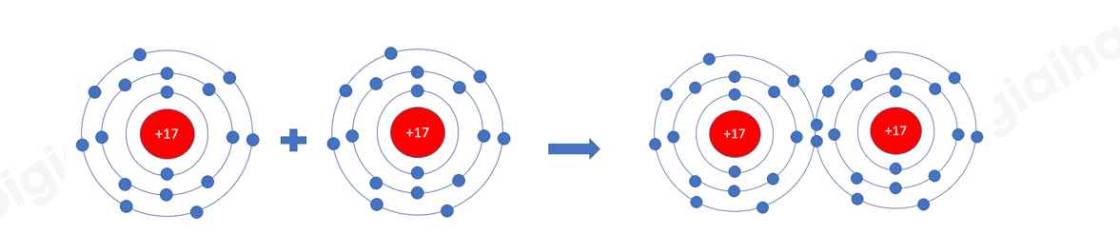
- Nguyên tử Cl có 7 electron ở lớp ngoài cùng => Có xu hướng nhận thêm 1 electron để đạt cấu hình electron bền vững của khí hiếm Ar
=> Khi hình thành phân tử Cl2, mỗi nguyên tử sẽ góp 1 electron để tạo thành 1 cặp electron chung

Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.
Liên kết cộng hóa trị trong phân tử dạng A2 luôn là liên kết cộng hóa trị phân cực hay không phân cực? Giải thích.
Vì sao liên kết cộng hóa trị trong các phân tử Cl2, O2, N2 là liên kết cộng hóa trị không phân cực?
Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Nêu thêm ví dụ về phân tử có liên kết cộng hóa trị không phân cực và liên kết cộng hóa trị phân cực. Viết công thức electron của chúng để minh họa.
Mô tả sự tạo thành liên kết trong phân tử chlorine bằng sự xen phủ của các AO.
Trình bày sự hình thành liên kết cho – nhận trong phân tử sulfur dioxide (SO2)
Căn cứ giá trị năng lượng liên kết H-H và N-N đã cho, liên kết trong phân tử nào dễ bị phá vỡ hơn?
Giải thích sự hình thành liên kết trong các phân tử HCl, O2 và N2.