- Phân tử có liên kết cộng hóa trị không phân cực: Cl2, O2, H2, N2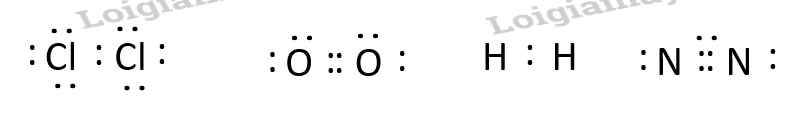
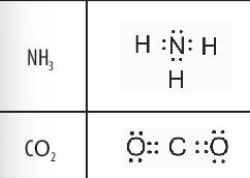
- Phân tử có liên kết cộng hóa trị phân cực là: HCl, NH3, CO2
- Phân tử có liên kết cộng hóa trị không phân cực: Cl2, O2, H2, N2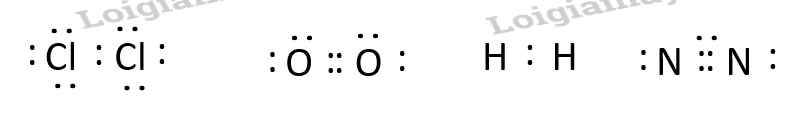
- Phân tử có liên kết cộng hóa trị phân cực là: HCl, NH3, CO2

Liên kết cộng hóa trị trong phân tử dạng A2 luôn là liên kết cộng hóa trị phân cực hay không phân cực? Giải thích.
Vì sao liên kết cộng hóa trị trong các phân tử Cl2, O2, N2 là liên kết cộng hóa trị không phân cực?
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử Cl2.
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.
Biết phân tử CO cũng có liên kết cho – nhận. Viết công thức electron và công thức cấu tạo của CO.
Trong việc hình thành liên kết hóa học, không phải lúc nào các nguyên tử cũng cho, nhận electron hóa trị với nhau như trong liên kết ion. Thay vào đó, chúng có thể cùng nhau sử dụng chung các electron hóa trị để cùng thỏa mãn quy tắc octet. Trong trường hợp này, một loại liên kết hóa học mới được hình thành. Đó là loại liên kết gì?
Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Em có nhận xét gì khi cặp electron chung trong liên kết lệch hẳn về một phía nguyên tử?
Căn cứ giá trị năng lượng liên kết H-H và N-N đã cho, liên kết trong phân tử nào dễ bị phá vỡ hơn?